Une insuffisance cardiaque droite particulière

CAS CLINIQUE
La Lettre du Cardiologue - n° 368 - octobre 2003
30
n homme de 70 ans a été hospitalisé pour une tam-
ponade au début du mois d’août 1999 dans la région
où il séjournait pour ses vacances. Un drainage péri-
cardique a permis l’évacuation de 700 ml de liquide séro-héma-
tique, dont l’examen cytologique n’a pas montré d’anomalie. Les
suites opératoires ont été marquées par des troubles rythmiques
et conductifs qui ont conduit à l’implantation d’un stimulateur
cardiaque double chambre. Au mois de septembre 1999 ont été
mises en évidence des adénopathies périphériques dont la biop-
sie a conclu à un lymphome non hodgkinien centroblastique B.
La biopsie osseuse a montré un envahissement médullaire. Le
scanner abdominal était normal. Le patient a alors été transféré
près de son domicile et hospitalisé dans le service d’hématologie
de notre institution. À son arrivée, on constatait une insuffisance
cardiaque droite avec hépatomégalie, turgescence et reflux
hépato-jugulaire, œdèmes des membres inférieurs, faisant évo-
quer initialement la possibilité d’une récidive d’épanchement
péricardique.
L’échocardiogramme transthoracique ne montrait pas d’épan-
chement péricardique, mais une masse de 4 à 5 cm prolabant au
travers de l’orifice tricuspide et gênant le remplissage du ventri-
cule droit (figure 1). On notait aussi une hypertrophie concen-
trique du ventricule gauche avec un aspect anormalement écho-
gène des parois. L’échocardiogramme transœsophagien (ETO)
montrait en coupe transversale une masse polylobée intéressant
le septum interauriculaire et les deux oreillettes (figure 2). La
masse intra-auriculaire droite était très volumineuse, mesurant
9 cm x 3 cm, enclavée dans l’orifice tricuspide, avec un aspect
turbulent et comprimé du flux de remplissage tricuspide en dop-
pler couleur témoignant d’une gêne majeure au remplissage du
ventricule droit (figures 3 et 4). En coupe longitudinale, la masse
intra-auriculaire gauche intéressait aussi la paroi postérieure de
l’aorte, où elle mesurait 2,5 cm d’épaisseur (figure 5).
Le diagnostic de lymphome cardiaque secondaire était retenu, et
une chimiothérapie de type CHOP était instaurée. L’échocardio-
gramme transthoracique et l’ETO réalisés deux semaines après
le début du traitement montraient une importante régression de
la masse intracardiaque (figures 6 et 7). L’évolution secondaire
était marquée par une rémission totale avec une disparition com-
plète de la masse intracardiaque, mais une rechute du lymphome
survenait en mars 2002 au niveau testiculaire, sans atteinte
cardiaque associée, nécessitant une orchidectomie gauche et la
reprise d’une chimiothérapie.
Une insuffisance cardiaque
droite particulière
●
B. Gallet, M. Goudjil, C. Adams*
* Service de cardiologie, centre hospitalier Victor-Dupouy, 95100 Argenteuil.
U
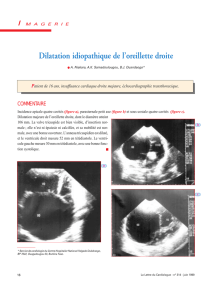
Figure 1. Échocardiogramme transthoracique : coupe apicale 4 cavités -
Masse de 4,6 cm x 3,4 cm enclavée au travers de l’orifice tricuspide
(OD : oreillette droite, OG : oreillette gauche, VD : ventricule droit,
VG : ventricule gauche).
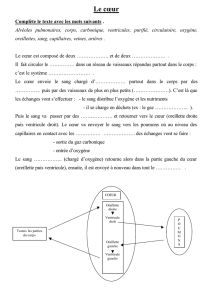
Figure 2. ETO, incidence transversale : volumineuse masse intéressant
le septum interauriculaire et les deux oreillettes (OD : oreillette droite,
OG : oreillette gauche).

DISCUSSION
Cette observation rappporte un cas de localisation cardiaque
secondaire d’un lymphome non hodgkinien, particulière par la
taille volumineuse des masses intracardiaques observées et par
une évolution favorable sous chimiothérapie. Malgré l’absence
de preuve histologique, le diagnostic peut raisonnablement être
retenu en raison du lymphome ganglionnaire d’une part et de la
régression complète de la masse intracardiaque sous chimiothé-
rapie d’autre part.
Une localisation cardiaque secondaire est assez fréquente en cas
de lymphome et survient dans 10 % à 25 % des cas, alors que les
lymphomes cardiaques primitifs sont rares (1, 2). La dissémina-
La Lettre du Cardiologue - n° 368 - octobre 2003
31
CAS CLINIQUE
Figure 5. ETO, incidence longitudinale : masse intra-auriculaire gauche
infiltrant la paroi postérieure de l’aorte ascendante où elle mesure
2,5 cm (AO : aorte, OG : oreillette gauche).
Figure 6. ETO réalisé deux semaines après le début de la chimiothéra-
pie : incidence longitudinale orientée vers le septum interauriculaire et
les deux oreillettes ; nette régression de la masse biauriculaire en com-
paraison de la figure 2 (OD : oreillette droite, OG : oreillette gauche).
Figure 7. ETO réalisé deux semaines après le début de la chimiothéra-
pie, incidence longitudinale : nette régression de la masse intra-auricu-
laire gauche en comparaison de la figure 5 avec régression de l’infiltra-
tion de la paroi postérieure de l’aorte, qui ne mesure plus que 1 cm (AO :
aorte, OG : oreillette gauche).
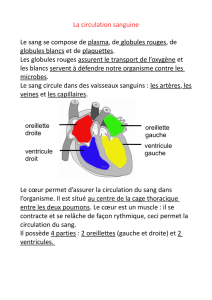
Figure 3. ETO, incidence transversale orientée vers les cavités droites :
masse intra-auriculaire droite mesurant 9 cm x 3 c m enclavée dans la
valve tricuspide (OD : oreillette droite, OG : oreillette gauche, VD : ven-
tricule droit).
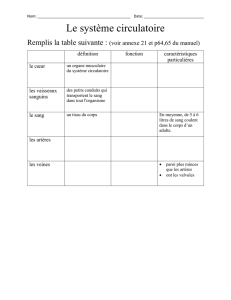
Figure 4. ETO, même incidence que la figure 3 : aspect laminé du flux de
remplissage transtricuspide en doppler couleur témoignant d’une gêne
majeure au remplissage du ventricule droit [flèche] (OD : oreillette droite,
OG : oreillette gauche, VD : ventricule droit, VG : ventricule gauche).

La Lettre du Cardiologue - n° 368 - octobre 2003
32
CAS CLINIQUE
tion se fait généralement par voie hématogène, ce qui explique
qu’une atteinte cardiaque puisse compliquer un lymphome extra-
thoracique (3). Les trois tuniques peuvent être touchées (endo-
carde, myocarde, péricarde). Les manifestations cliniques sont
variables et dépendent des tuniques intéressées. L’atteinte car-
diaque peut rester infraclinique, entraîner des signes non spéci-
fiques (dyspnée, douleurs thoraciques, palpitations, perte de
connaissance), une atteinte péricardique avec parfois tamponade,
une insuffisance cardiaque souvent à prédominance droite, des
troubles rythmiques et conductifs, ou un syndrome cave supé-
rieur. L’ECG peut retrouver des troubles du rythme ou de la
conduction, un microvoltage, et des anomalies de repolarisation
(1, 2).
L’échocardiogramme peut montrer un épanchement péricardique,
avec ou sans tamponade, une atteinte myocardique et des masses
intracavitaires. L’atteinte myocardique peut entraîner un aspect
d’hypertrophie ventriculaire gauche concentrique associée à une
échostructure anormale (1), une infiltration tumorale ou des
troubles de la cinétique. Les masses intracardiaques siègent pré-
férentiellement au niveau du cœur droit (2, 4), pouvant entraîner
une obstruction tricuspide (2, 4). Elles apparaissent polylobées
(2), souvent volumineuses, fixes ou mobiles. Elles peuvent éga-
lement concerner l’oreillette gauche, le septum interauriculaire,
l’auricule gauche et la région périaortique (5-7). L’ETO paraît
particulièrement performant pour le diagnostic, permettant de
l’évoquer chez des patients encore asymptomatiques (5), et pou-
vant guider un geste de biopsie (8). Les autres méthodes d’ima-
gerie utiles sont le scanner et l’IRM. Le diagnostic de certitude
repose sur la biopsie, éventuellement guidée par ETO, mais une
histologie négative n’exclut pas le diagnostic en cas d’atteinte
localisée (1).
Le pronostic est habituellement réservé (1, 5), mais des évo-
lutions favorables sous chimiothérapie ont été rapportées
(1, 4, 7).
CONCLUSION
Cette observation permet d’illustrer plusieurs aspects cliniques
et échocardiographiques des lymphomes cardiaques secondaires :
atteinte péricardique avec tamponade initiale, atteinte myocar-
dique avec hypertrophie concentrique du ventricule gauche,
troubles rythmiques et conductifs ayant conduit à l’implantation
d’un stimulateur cardiaque, et, surtout, volumineuse masse intra-
cardiaque biauriculaire obstruant l’orifice tricuspide et respon-
sable d’une insuffisance cardiaque droite. Elle souligne l’intérêt
diagnostique de l’ETO dans cette situation, et montre que l’évo-
lution de ces tumeurs intracardiaques peut être favorable sous
chimiothérapie. ■
Bibliographie
1. Cracowski JL, Trémel F, Nicolini F, Bost F, Mallion JM. Localisation myocar-
dique chimiosensible observée au cours d’un lymphome malin non hodgkinien.
Arch Mal Cœur 1997 ; 90 : 1527-31.
2. Ztot S, Cherradi R, Haddour L et al. Lymphome cardiaque primitif : à propos
d’un cas. Arch Mal Cœur 2002 ; 95 : 61-4.
3. Sanna P, Bertoni F, Zucca E et al. Cardiac involvement in HIV-related non-
Hodgkin’s lymphoma : a case report and short review of the literature. Ann
Hematol 1998 ; 77 : 75-8.
4. Pettelot G, Gibelin P, Blanc P et al. Disparition totale à 23 mois d’un volumi-
neux lymphome non hodgkinien cardiaque par chimiothérapie. Arch Mal Cœur
1996 ; 89 : 379-81.
5. Liang R, Yu CM, Au WY, Choy CKW, Kwong YL. Secondary lymphoma of the
heart manifesting as intracavitary masses. J Clin Oncol 2000 ; 18 : 1998.
6. Boey S, Fouda-Omgba F, Mirode A, Tribouilloy C, Quere JP, Lesbre JP.
Malignant cardiac lymphoma : diagnosis by echocardiography. Arch Mal Cœur
1997 ; 90 : 1655-61.
7. Grollier G, Troussard X, Agostini D et al. Cardiac involvement in two cases
of malignant non-Hodgkin’s lymphoma. Course of cardiac involvement under
chemotherapy. Arch Mal Cœur 1987 ; 80 : 651-6.
8. Jurkovich D, de Marchena E, Bilsker M, Fierro-Renoy C, Temple D, Garcia H.
Primary cardiac lymphoma diagnosed by percutaneous intracardiac biopsy with
combined fluoroscopic and transesophageal echocardiographic imaging. Cathet
Cardiovasc Interv 2000 ; 50 : 226-33.
1
/
3
100%