Les techniques nucléaires dans la détection et le suivi du cancer

PERSPECTIVES
Les techniques nucléaires
dans la détection et le suivi
du cancer
Les pays en développement s'intéressent de plus en plus
aux méthodes de diagnostic améliorées
par
R.D. Piyasena,
A. Cuarôn
et M. Nofal
Le cancer est une des grandes maladies de
notre époque. On a renoncé à lui trouver un
agent pathogène unique et, partant, un seul trai-
tement et, aujourd'hui, les milieux médicaux
sont plutôt d'avis que chaque cas est différent
et doit être traité séparément. De nombreux
agents cancérigènes comme le tabac, le bétel
(chiqué), certains agents viraux et les rayonne-
ments ultraviolets ont été identifiés. Ces der-
niers temps, on a pris note du rôle vital que
pourraient jouer les «gènes prédisposant aux
risques de cancer» (oncogenes) qui sont des
formes aberrantes de gènes normaux.
Les techniques de traitement du cancer
(chirurgie classique, radiothérapie, chimio-
thérapie ou, plus récemment, immunothérapie
et manipulation génétique) ont fait des progrès
importants et parfois spectaculaires. Cepen-
dant, il ne fait pas de doute que, dans la plupart
des cas, la détection au stade le plus précoce
possible reste l'élément décisif qui détermine
l'issue finale du traitement. Sur ce plan, la
situation n'est pas aussi satisfaisante qu'on
pourrait le souhaiter. Pour le cancer du poumon
par exemple, environ 20% seulement des cas
sont diagnostiqués avant que le mal ne se soit
propagé. C'est pourquoi des méthodes de diag-
nostic améliorées s'imposent.
Diagnostic: méthodes améliorées
Il existe deux grandes méthodes dont les
récents progrès ont eu une incidence marquante
sur la sensibilité (pourcentage de cas correcte-
ment diagnostiqués par test positif) et la spécifi-
cité (pourcentage de patients non atteints pour
lesquels les tests sont négatifs) du diagnostic du
cancer.
La première consiste à identifier et à quanti-
fier in vitro des substances appelées «indica-
teurs tumoraux» par des essais en laboratoire
effectués sur des spécimens de fluide biologi-
que qui sont le plus souvent des spécimens
sanguins.
M. Piyasena et M. Cuarôn sont membres de la Division des
sciences biologiques de l'AIEA, dont M. Nofal est
directeur.
La seconde comprend des techniques in vivo
qui requièrent la présence du patient. Ces
méthodes font appel à des procédures de visua-
lisation d'organes, modernes et souvent infor-
matisées, qui permettent de détecter les
tumeurs. En outre, elles peuvent parfois carac-
tériser les tumeurs malignes lorsque celles-ci
sont petites et se confinent au site primitif de la
maladie. Chaque groupe de tests, conjugué à
des données cliniques, est utilisé pour l'établis-
sement de diagnostics précoces et pour le suivi
ou l'évaluation du progrès de la maladie après
le traitement.
Le rôle des techniques nucléaires
Les techniques nucléaires ont apporté une
contribution très importante aux études de diag-
nostic. Elles constituent en particulier un
moyen pratique de détecter les indicateurs
tumoraux et de visualiser les tumeurs par des
tests in vitro et in vivo réalisés à l'aide de
radionucléides.
Détection des indicateurs tumoraux. Les
indicateurs tumoraux comprennent un certain
nombre de substances sécrétées par nombre de
tumeurs, certaines faisant exception. Ces subs-
tances sont libérées dans l'appareil circulatoire:
leur présence ou leur degré de concentration
peuvent signaler l'existence d'une tumeur.
Certaines d'entre elles sont des substances
chimiques normalement sécrétées par le corps
(«indicateurs eutopiques»). Une augmentation
de leur concentration peut signaler la présence
de tumeurs malignes. C'est ainsi que la calcito-
nine,
lorsqu'on la trouve en quantités élevées,
en particulier après stimulation à la Penta-
gastrine, est un bon indicateur biochimique
pour le diagnostic précoce du cancer médullaire
de la thyroïde. Il en va de même pour l'hor-
mone adréno-corticotrope (ou adrénocortico-
trophine (ACTH)).
D'autres indicateurs biochimiques peuvent
être «ectopiques». Ils sont produits sur des sites
inhabituels lorsqu'il y a cancer. L'adrénocorti-
cotrophine est normalement sécrétée par
l'hypophyse, mais on en trouve des concentra-
AIEA BULLETIN,
1/1991

PERSPECTIVES
tions élevées en cas de cancer des bronches ou
de certains autres organes.
Il existe aussi des indicateurs appelés «onco-
fœtaux». Normalement présents à différents
stades de la vie embryonnaire et fœtale, ils
peuvent subsister à de faibles concentrations
chez les adultes, mais réapparaissent en gran-
des quantités sur certaines tumeurs malignes
(par exemple, l'alpha-fœto-protéine (AFP) et
l'antigène carcino-embryonnaire (CEA)).
Le dernier groupe peut être rangé dans la
catégorie des «mutationnels». Il inclue notam-
ment la paraprotéine (myélomes) et une muta-
tion de la protéine P53 (cancers des bronches et
du colon).
On dispose habituellement d'environ deux
douzaines d'indicateurs de tumeurs détectables
par radio-immunodosage: AFP, choriogonado-
trophine /3 (HCG), microglobuline 0-2, CA
15-3,
CA 19-9, CA-50, CA-125, antigène
carcino-embryonnaire (CEA), Cortisol, gas-
trine,
HGH, insuline, MCA, néoptérine, NSE,
PAP,
prolactine, PSA, PTH, SCC, TCT, TG et
TPA.
Malheureusement, dans leur très grande
majorité, ces indicateurs ne sont pas spécifiques
d'un organe ou d'une maladie précise. Ils ne
sont pas sécrétés uniquement par un seul et
même organe. C'est ainsi qu'on retrouve des
quantités élevées de CEA dans les tumeurs du
tractus gastro-intestinal, du sein, du poumon,
des ovaires et de la thyroïde. Si, pour plus de
80%
des cancers ovariens, les concentrations
de CA-125 sont élevées, elles le sont aussi en
cas de maladies inflammatoires du pelvis,
d'endométriose, de cirrhose et de pancréatite.
Les indicateurs tumoraux ne sont pas non
plus spécifiques des affections malignes. Cela
est dû au fait qu'ils sont produits par des tissus
normaux ou ayant subi des modifications béni-
gnes.
Par exemple, l'antigène spécifique de la
prostate peut être sécrété aussi bien par une
prostate normale en cas d'hyperplasie bénigne
que par une prostate cancéreuse.
On a tenté de définir des «seuils» ou des
concentrations à partir desquels on peut penser
qu'il y a tumeur maligne. Pour certains indica-
teurs (AFP, HCG, CA-125), la démarche
s'est
révélée assez concluante, mais elle ne donne
pas entière satisfaction, car les concentrations
de ces indicateurs peuvent aussi augmenter en
cas de nécrose tissulaire bénigne, d'inflamma-
tion et d'hémorragie.
Ce n'est pas pour le dépistage ou le diagnos-
tic précoce que les indicateurs tumoraux sont le
plus utiles, mais plutôt pour l'évaluation des
pronostics, le suivi post-thérapeutique, la
détection des premières récidives et, lorsqu'ils
sont associés à des méthodes de visualisation
d'organes, pour surveiller la dimension des
tumeurs. Même la thyroglobuline, un des rares
exemples d'indicateur qui soit à 100% spécifi-
que d'un organe, est d'un intérêt pratiquement
nul pour le diagnostic du cancer de la thyroïde.
En revanche, cette hormone est très utile pour
la surveillance de la réaction au traitement. Si
celui-ci a été efficace, les concentrations
tendront à revenir à la normale mais, si la
tumeur résiste au traitement, elles resteront
élevées.
Les indicateurs tumoraux sont immuno-
gènes,
ou on peut faire en sorte qu'ils le devien-
nent en recourant à des moyens éprouvés. Par
conséquent, on peut s'en servir pour produire
des anticorps qui seront soit polyclonaux (déri-
vés de plusieurs lignées cellulaires appartenant
à un animal de laboratoire) soit monoclonaux
(provenant d'une seule lignée cellulaire obtenue
grâce à une méthode spéciale appelée la techni-
que des hybridomes). Cette dernière technique,
qui est aujourd'hui la plus couramment utilisée,
a beaucoup amélioré la sensibilité et la spécifi-
cité,
et élargi considérablement la gamme des
méthodes d'analyse employées pour la détec-
tion des indicateurs tumoraux.
Les techniques les plus couramment utilisées
pour la détection in vitro et la mesure des indi-
cateurs tumoraux contenus dans les fluides bio-
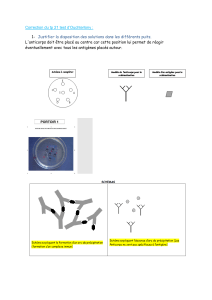
Principaux sites où sont
produits certains des
indicateurs tumoraux les
plus courants: 1) NSE:
cancer du poumon à
petites cellules; 2) TPA
et CEA: cancer du
poumon;
3) AFP: cancer
primitif du foie
(hépatomes); 4) CA-50 et
CA 19-9: cancer du
pancréas;
5) microglobuline 0-2:
leucémie; 6) AFP et
CA-125: cancer des
ovaires; 7) AFP et hCG:
cancer des testicules;
8) microglobuline 0-2:
lymphomes malins;
9) TPA, ER + - et CEA:
cancer du sein;
10) CA 19-9 et CEA:
cancer du colon;
11) CEA, TPA, CA 19-9 et
CA-50:
cancer
colo-rectal; 12) PSA et
PAP:
cancer de la
prostate.
logiques se fondent sur l'étude des réactions
entre l'indicateur lui-même, qui sert d'anti-
gène,
et l'anticorps correspondant. Un bon
exemple serait le CA-125, antigène du cancer.
Son déterminant antigénique est reconnu par
l'anticorps monoclonal OC-125 obtenu en utili-
sant une souche de cellules de cancer ovarien
(OVCA 433) comme immunogène. Les réac-
tions antigène-anticorps peuvent être étudiées
par des méthodes non isotopiques comme les
dosages immuno-enzymologiques (ELISA), où
l'on se sert d'un enzyme pour évaluer le résul-
tat final de la réaction ou le pourcentage d'anti-
gène lié à l'anticorps.
Cependant, les méthodes radio-isotopiques
—
radio-immunodosage (RIA) ou le plus souvent
dosage radio-immunoradiométrique (IRMA)
—
AIEA BULLETIN,
1/1991
5

PERSPECTIVES
offrent de nombreux avantages en termes de
sensibilité, de précision, de commodité et de
coût. Ce sont des méthodes micro-analytiques
qui dépendent essentiellement de la réaction
entre la substance que l'on souhaite détecter ou
mesurer (analyte), dans le cas qui nous inté-
resse ici un antigène, et un agent de liaison
approprié (réactif), en l'occurrence un anti-
corps monoclonal. En marquant, au moyen
d'un radionucléide approprié (généralement de
l'iode 125), l'antigène (méthode RIA) ou l'anti-
corps (méthode IRMA), on parvient à déter-
miner le taux d'occupation des sites de liaison
à la fin de la réaction. On peut dire que ce sont
là en fait des méthodes de choix applicables à
tous les indicateurs tumoraux, quelle que soit
leur nature.
Ce que l'on sait sur les caractéristiques de
sensibilité et de spécificité propres à certains
Spécificité de certains
indicateurs tumoraux courants
Indicateur
AFP
CA 15-3
Tumeurs
Hépatomes
Gonades
Cancer du sein
Cancer des ovaires
Spécificité
>80%
>80%
CA 19-9 Tractus gastro-intestinal
(cancer de l'estomac,
du foie, de la vésicule >65°/o
biliaire, du pancréas,
cancer colo-rectal)
CA-125
CEA
NSE
PAP
PSA
SCC
TCT
TG
Cancer des ovaires
Cancer du pancréas
La plupart des tumeurs
solides (chez les non-fumeurs!]
Cancer du poumon
à petites cellules
Apudomes
Séminomes
Cancer de la prostate
Cancer de la prostate
Cancer de l'oreille, du nez
et du larynx (ONL)
Cancer du poumon
Cancer de l'utérus
Cancer médullaire de la
thyroïde
Cancer de la thyroïde
(post-thérapeutique)
>70%
- 60%
>70°/o
80%
50%
>80%
>80%
>80%
TPA Cancer du sein
Cancer du poumon
Cancer colo-rectal
Cancer de la vessie
Cancer de l'utérus
6 AIEA BULLETIN,
1/1991
indicateurs tumoraux courants vient confirmer
le point de vue selon lequel ces indicateurs sont
généralement sans intérêt pour le dépistage
ou l'établissement de diagnostics précoces
(tableau 1). Ils sont en revanche plus utiles
lorsqu'il
s'agit
de suivre les traitements ou de
détecter les récurrences à temps. Certains
d'entre eux font toutefois exception à la règle.
C'est ainsi que les indicateurs eutopiques dont
on a déjà parlé sont couramment utilisés pour le
dépistage des groupes à haut risque — par
exemple, on effectue des mesures de chorio-
gonadotrophine humaine (hCG) pour détecter
les chorio-carcinomes chez les patients atteints
de môles hydatiformes.
Les mesures d'indicateurs tumoraux sont
parfois utiles pour évaluer le stade d'évolution
ou le degré de gravité d'une tumeur maligne.
Aux premiers stades du cancer du sein (stades 1
et 2), les concentrations d'indicateurs AFP et
CA 15-3 sont normales. En revanche, aux
stades 3 et 4 de la maladie, lorsque apparaissent
des métastases localisées ou distantes, elles sont
élevées. Là encore, toutefois, ces concentra-
tions peuvent aussi augmenter en cas de
tumeurs malignes non mammaires.
On peut parfois remédier à ces problèmes de
sensibilité et de spécificité insuffisantes en
mesurant simultanément plusieurs indicateurs
tumoraux et en recourant à des méthodes statis-
tiques fines d'analyse des données. Ces «grou-
pes d'indicateurs tumoraux» constituent peut-
être le meilleur moyen de distinguer les lésions
bénignes des lésions malignes et les différents
types de cellules cancéreuses. La méthode qui
a récemment été adaptée au cancer du poumon
a amélioré la précision des diagnostics. Par
ailleurs, on a constaté que les mesures conju-
guées de hCG /3 et d'AFP peuvent être utiles
pour la détermination clinique de l'évolution
des néoplasmes testiculaires.
Dans l'ensemble, toutefois, en dépit des
récents progrès et malgré les avantages que pré-
sentent les techniques radio-isotopiques sensi-
bles et précises, les mesures d'indicateurs
tumoraux restent complémentaires d'autres
procédures de diagnostic, du moins pour ce qui
concerne la détection précoce du cancer.
Visualisation d'organes: Dans ce domaine
aussi, les méthodes faisant appel à des radio-
nuclides sont utilisées en association avec
d'autres techniques non isotopiques comme la
radiographie, la tomodensitométrie (TDM) et
l'imagerie à résonance magnétique.
Les radionucléides capables de se localiser
très nettement sur la tumeur après administra-
tion par voie intraveineuse sont très peu nom-
breux. Ils se limitent semble-t-il à l'iode 131
(cancer différencié de la thyroïde après ablation
de cette glande) et à l'iode 131 MIBG (tumeurs
du tissu chromaffine (phaeochromocytomes,
neuroblastomes et paragangliomes)). Le tech-
netium 99m est un radionucléide de choix que
l'on peut désormais utiliser un peu partout,
y compris pour le marquage des monoclonaux.
Cependant, s'il peut faire apparaître des lésions
mesurables dans l'espace, il ne peut pas distin-

PERSPECTIVES
guer les lésions malignes des autres lésions
(kystes, voire processus inflammatoires) et ce,
qu'il soit administré seul ou en association avec
différents agents chimiques montrant une affi-
nité pour certains organes bien précis (par
exemple, le colloïde de soufre pour le foie).
Le gallium 67, qui compte parmi les radio-
nuclides que l'on utilise seuls, a une sensibilité
d'environ 90% et une spécificité de quelque
75%
pour la détection des tumeurs du poumon.
Toutefois, il ne discrimine pas bien les affec-
tions malignes.
A mesure que l'on parvenait à obtenir des
anticorps monoclonaux correspondant aux anti-
gènes associés aux tumeurs, on a mis au point
des procédés permettant aux radionucléides de
mieux se localiser. Par exemple, le P97 est un
antigène sécrété par les mélanomes malins. Il
est possible de lui trouver un anticorps mono-
clonal que l'on marquera de manière appro-
Les conditions générales requises pour l'uti-
lisation de cette technique sont donc claires. Il
faut un antigène spécifiquement sécrété par des
cellules cancéreuses, un anticorps monoclonal
correspondant de bonne qualité (à affinité et à
spécificité élevées), un radiomarqueur appro-
prié,
un procédé de marquage ne portant pas
atteinte à l'immunoréactivité, et enfin un
système de visualisation extérieure permettant
de localiser l'anticorps après administration au
patient. La technique en elle-même n'est pas
traumatisante. Elle consiste à administrer
l'anticorps marqué au patient (lequel n'a géné-
ralement pas besoin de préparatifs spéciaux) et
à visualiser cet anticorps après un certain délai
(qui peut aller de quelques heures à plusieurs
jours).
Le fait que la plupart des antigènes sécrétés
par les cellules cancéreuses ne sont pas spécifi-
ques des organes et des tissus est, en radio-
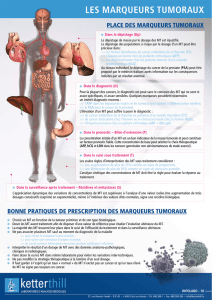
Le produit
radiopharmaceutique
injecté se localise dans
l'organe à examiner et
permet de le visualiser.
(Photo: ORNL)
priée. Administré par voie intraveineuse, cet
anticorps se lie à l'antigène sur la membrane
externe des cellules cancéreuses. Les lieux où
il se dépose peuvent ensuite être visualisés par
affichage extérieur. Ce procédé, appelé la
radio-immunoscintigraphie, se répand à mesure
que l'on met au point des anticorps de meilleure
qualité et des techniques de marquage isotopi-
que plus commodes.
immunoscintigraphie, tout aussi gênant que
dans le cas des méthodes in vitro précédemment
décrites. Les anticorps monoclonaux utilisés
sont, dans leur majorité, davantage associés
aux tumeurs que spécifiques de ces tumeurs et
le pourcentage de radioactivité injectée qui, en
fin de parcours, se localise sur la tumeur est
très faible
(0,01%
à 0,001%). Le reste se
retrouve dans le sang et dans des organes nor-
AIEA BULLETIN,
1/1991
7

PERSPECTIVES
maux comme
le
foie,
la
rate
et les
reins.
Il en
résulte
que,
dans
les
zones
à
faible bruit
de
fond,
les
grosses tumeurs sont habituellement
les seules qui puissent être détectées. Une inno-
vation récente
et
fort prometteuse dans
ce
domaine
est
l'emploi d'antigènes artificiels
comme l'Agl50H82, antigène
des
«panadéno-
carcinomes». En outre, certains antigènes asso-
ciés
aux
tumeurs (CEA,
AFP, hCG)
peuvent
être obtenus
à
l'état
pur, d'où la
possibilité
d'immuniser
les
animaux avec
ces
substances
plutôt qu'avec
des
extraits
de
tumeurs.
Les progrès du radiomarquage ont aussi per-
mis
des
améliorations importantes.
Le
techne-
tium
99m est
l'isotope
que l'on
trouve
le
plus
couramment dans
les
laboratoires
de
médecine
nucléaire
du
monde entier. Compte tenu
de sa
courte période,
il se
prête parfaitement
aux
techniques
de
radio-immunoscintigraphie,
car
la localisation
de
l'anticorps
sur la
tumeur
intervient essentiellement dans
les
premières
24 heures. Mais, lorsqu'il n'existe
pas de
méthodes satisfaisantes pour
le
marquage
des
anticorps
au
technetium
99m ou que la
visua-
lisation
se
fait après
un
délai plus long
que
prévu, d'autres isotopes comme l'iode
131 et
ï'indium
131
sont employés. Toutefois,
on a
récemment fait état
de
méthodes
de
marquage
d'anticorps
au
technetium
99m qui
sont
commodes
et
susceptibles d'application dans
les laboratoires de médecine nucléaire des hôpi-
taux.
Ces
méthodes sont douces
et ne
portent
pas atteinte
à
l'immunoréactivité des anticorps.
En
ce qui
concerne l'instrumentation,
il est
indispensable d'avoir
une
caméra gamma
à
canaux parallèles couplée
à un
ordinateur.
La
tomodensitométrie
à
émission de photon unique
a peut-être pour avantage d'améliorer
la
résolu-
tion, notamment
si l'on se
sert
de
caméras
à
double
ou
triple collimateur. Mais
la
question
semble n'avoir toujours
pas été
tranchée
et
certains spécialistes
se
demandent
si, en
radio-
immunoscintigraphie,
la
tomodensitométrie
à
émission
de
photon unique
ne
pose pas plus
de
problèmes qu'elle
n'en
résout.
Tout comme les techniques in vitro, la radio-
immunoscintigraphie
est
plus utile pour
la
détection des cancers récurrents
et
pour
le
suivi
post-thérapeutique
que
pour
le
dépistage. Elle
est aussi généralement plus sensible
que la
tomodensitométrie. La détection par cette tech-
nique des cancers récurrents
du
tractus gastro-
intestinal,
de
l'appareil uro-génital
et
du tractus
génital
de la
femme
a
une sensibilité voisine
de
100%
et une
spécificité
de
80%. Ces pourcen-
tages sont plus élevés
que
pour
les
techniques
in vitro. (Pour
un
exemple typique
de
cancer
récurrent
du
colon détecté
par
radio-
immunoscintigraphie
au
moyen
d'un
anticorps
monoclonal correspondant
à
l'antigène
du
CEA,
voir
la
photo
de
couverture
du
présent
numéro).
La technique la plus récente dans le domaine
de l'utilisation des radionucléides pour la détec-
tion
des
lésions malignes
est la
tomographic
à
émission
de
positons. Cette méthode complexe
fait appel
à
des radio-isotopes de courte période
comme
le
fluor
18,
l'oxygène
15 et le
car-
bone 11, produits dans
un
cyclotron. Elle per-
met
non
seulement
de
localiser
la
tumeur mais
aussi
de
recueillir des informations
sur
son état
fonctionnel
et son
métabolisme, renseigne-
ments
qui
peuvent être déterminants pour
la
caractérisation
des
affections malignes.
La
tomographic
à
émission
de
positons permet
même, dans
le
cas des tumeurs
du
cerveau,
de
déterminer
le
degré
de
malignité
ou le
stade
d'évolution de
la
tumeur, chose que
ni la
tomo-
densitométrie
ni
l'imagerie
par
résonance
magnétique
ne
sont capables
de
faire avec pré-
cision.
Il y a
fort
à
parier que c'est
la
technique
de l'avenir mais, pour qu'elle puisse
se
diffu-
ser,
il
faudrait la rendre plus commode et moins
coûteuse.
Centres d'intérêt
et
activités
de
l'AlEA
Pendant toutes
ces
années, F AIE A
a
aidé
à
mettre
sur
pied
un
réseau
de
laboratoires
de
radio-immunodosage
et de
médecine nucléaire
bien équipés
et
compétents dans
les
principaux
hôpitaux, centres universitaires
et
autres éta-
blissements des pays en développement.
Il
n'est
pas surprenant que
les
laboratoires
de
ces pays
s'intéressent
de
plus
en
plus
aux
techniques
de
radio-immunodosage
des
indicateurs tumoraux
et
à la
radio-immunoscintigraphie,
car il
leur
est plus facile d'obtenir
les
réactifs (anticorps
monoclonaux, technetium 99m, etc.)
et
instru-
ments (matériel
de
radio-immunodosage
et
caméras gamma) nécessaires,
et ils ont
davan-
tage
de
personnel qualifié.
Pour répondre
à cet
intérêt,
la
Section
de
médecine nucléaire
de la
Division des sciences
biologiques
de
l'AIEA
a
intensifié
ses
travaux
dans les domaines précités. En mai dernier
s'est
réuni
un
séminaire
sur
l'emploi
des
techniques
nucléaires pour
le
diagnostic précoce du cancer
dans
les
pays
en
développement.
En
1991,
les
contrats
de
recherche individuels
qui ont été
passés
au
cours des dernières années viendront
à point lors
du
lancement,
au
niveau mondial,
de programmes
de
recherche coordonnée
sur
les dosages d'indicateurs tumoraux (selon
le
modèle
de
l'AFP pour
le
cancer
du
foie)
et sur
la radio-immunoscintigraphie (selon
le
modèle
du
CEA
pour
le
cancer colo-rectal).
Des
réu-
nions
de
consultants auxquelles
ont
participé
des experts internationaux ont déjà
eu
lieu pour
donner des conseils sur les aspects techniques
et
logistiques
de la
mise
en
œuvre de ces projets.
Pour
les
années
à
venir,
on
prévoit
un
programme
de
travail intensif (passation
de
contrats
de
recherche, signature d'accords
de
recherche, octroi
de
bourses
de
formation,
organisation d'ateliers et de réunions de coordi-
nation
de la
recherche).
Ces
activités apporte-
ront
une
contribution
non
négligeable
à
l'implantation des méthodes dont
il est
ici ques-
tion dans
les
pays
en
développement
et au
renforcement du rôle des techniques nucléaires
dans l'amélioration
de la
santé humaine.
8 AIEA BULLETIN,
1/1991
1
/
5
100%