MICI-final

Mécanisme de l'inflammation au
cours des Maladies Inflammatoires
Chroniques de l’Intestin
(MICI)
CHU ROUEN
DES AVRIL 2016

I) Stimulation anormale des cellules résidentes dans
la muqueuse intestinale et inhibition de l'apoptose
a) Activation des voies de transduction
b) Production de médiateurs inflammatoires
c) Surexpression de molécules d'adhésions
d) Inhibition de l’apoptose
II) Activation anormale du système immunitaire
a) Rupture de la tolérance vis-à-vis de sa propre flore intestinale
b) Augmentation de la perméabilité de la barrière intestinale
c) Anomalies fonctionnelles des cellules epithéliales/cellules de
Paneth
d) Anomalies des lymphocytes T
III) Application thérapeutique
PLAN

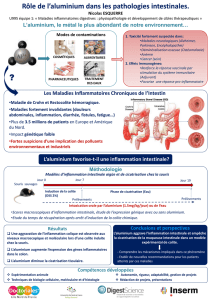
Facteurs déclenchants
-Tabac (seul FdR universellement reconnu)
-Alimentation
-Hygiène domestique
-Utilisation d'antibiotiques
-Mutation gène NOD2 (FdR le plus fort)
-Très grand nombre de gènes impliqués
dans la susceptibilité aux MICI (IL23R,
JAK2, STAT3, P40…)
Développement de la maladie
Microbiote
Genes
Environnement
3 principaux phyla
bactériens :
FIRMICUTES
BACTEROIDETES
ACTINOBACTERIES

I-Stimulation anormale des cellules
résidentes dans la muqueuse
intestinale et inhibition de l’apoptose

a) Activation des voies de la
transduction
-
IkB
NFkB +
NFkB
MAP Kinases
P38
ERK
JNK
P38
ERK
JNK
Translocation
ADN
Facteur
de stress = agent
pathogène
Cellule épithéliale
intestinale (pôle
apical)
Pôle basal
+
Cytokine inflammatoire (TNF α) et son
récepteur
Activation gènes de réaction inflammatoire
Production de cytokines inflammatoires
Chimiokines, molécules d'adhésions...
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
1
/
31
100%