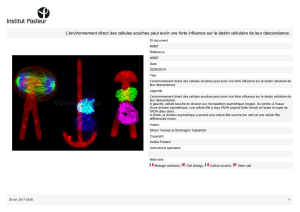
L`épiderme et son renouvellement par les cellules souches

Vie et mort des cellules dans les tissus
I. L'épiderme et son renouvellement par les cellules
souches
II. Épithélium sensoriel
III. Voies aériennes et intestin
IV. Vaisseaux sanguins et cellules endothéliales
V. Renouvellement par des cellules souches
multipotentes : la formation des cellules sanguines
VI. Genèse : modulation et régénération du muscle
squelettique
VII. Les fibroblastes et leurs transformations : la famille
des cellules du tissu conjonctif
VIII. Ingénierie des cellules souches

Vie et mort des cellules dans les tissus
•Être unicellulaire : individu originel
•Être pluricellulaire : cellules au
service du corps tout entier
•Plus de 200 types de cellules
différents dans l’organisme

3
Cells of the Adult Human
Body : a Catalogue
•How many distinct cell types are there in an adult human being? In other words, how many
normal adult ways are there of expressing the human genome? A large textbook of histology
will mention about 200 cell types that qualify for individual names. These traditional names are
not, like the names of colors, labels for parts of a continuum that has been subdivided
arbitrarily: they represent, for the most part, discrete and distinctly different categories. Within
a given category there is often some variation—the skeletal muscle fibers that move the eyeball
are small, while those that move the leg are big; auditory hair cells in different parts of the ear
may be tuned to different frequencies of sound; and so on. But there is no continuum of adult
cell types intermediate in character between, say, the muscle cell and the auditory hair cell.
•The traditional histological classification is based on the shape and structure of the cell as seen
in the microscope and on its chemical nature as assessed very crudely from its affinities for
various stains. Subtler methods reveal new subdivisions within the traditional classification.
Thus modern immunology has shown that the old category of “lymphocyte” includes more than
10 quite distinct cell types. Similarly, pharmacological and physiological tests reveal that there
are many varieties of smooth muscle cell—those in the wall of the uterus, for example, are
highly sensitive to estrogen, and in the later stages of pregnancy to oxytocin, while those in the
wall of the gut are not. Another major type of diversity is revealed by embryological
experiments of the sort discussed in Chapter 21. These show that, in many cases, apparently
similar cells from different regions of the body are nonequivalent, that is, they are inherently
different in their developmental capacities and in their effects on other cells. Thus, within
categories such as “fibroblast” there are probably many distinct cell types, different chemically
in ways that are not easy to perceive directly.
•For these reasons any classification of the cell types in the body must be somewhat arbitrary
with respect to the fineness of its subdivisions. Here, we list only the adult human cell types
that a histology text would recognize to be different, grouped into families roughly according to
function. We have not attempted to subdivide the class of neurons of the central nervous
system. Also, where a single cell type such as the keratinocyte is conventionally given a
succession of different names as it matures, we give only two entries—one for the
differentiating cell and one for the stem cell. With these serious provisos, the 210 varieties of
cells in the catalogue represent a more or less exhaustive list of the distinctive ways in which a
given mammalian genome can be expressed in the phenotype of a normal cell of the adult
body.

4
http://www.garlandscience.com/t
extbooks/0815332181/pdfs/appe
ndix.pdf
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
 62
62
 63
63
 64
64
 65
65
 66
66
 67
67
 68
68
 69
69
 70
70
 71
71
 72
72
 73
73
 74
74
 75
75
 76
76
 77
77
 78
78
 79
79
 80
80
 81
81
 82
82
 83
83
 84
84
 85
85
 86
86
 87
87
 88
88
 89
89
 90
90
 91
91
 92
92
 93
93
 94
94
 95
95
 96
96
 97
97
 98
98
 99
99
 100
100
 101
101
 102
102
 103
103
 104
104
 105
105
 106
106
 107
107
 108
108
 109
109
1
/
109
100%