la réponse dans les gènes

Pourquoi
meurt-on
encore
d’une
méningite
à
méningocoque
:
la
réponse
dans
les
gènes
?
Why
meningococcal
meningitis
is
still
lethal:
Response
in
genes?
Le
pronostic
des
méningites
bactériennes
est
déterminé
par
les
délais
de
prise
en
charge
diagnostique
et
thérapeutique.
Malgré
des
recommandations
récentes,
qui
ont
certainement
permis
une
optimisation
de
la
prise
en
charge,
certains
décès
ne
peuvent
toujours
pas
être
évités.
La
mortalité
attribuable
aux
infections
invasives
à
méningocoque
en
France
est
de
10
%
[1].
Nous
publions
ici
le
cas
d’un
patient
de
23
ans
décédé
d’une
méningite
aiguë
foudroyante
à
méningocoque
pour
laquelle
des
facteurs
de
risque
génétiques
liés
à
la
bactérie
et
à
l’hôte
ont
été
cherchés.
Observation
Un
homme
de
23
ans
a
consulté
au
service
des
urgences
pour
un
syndrome
méningé
fébrile
associé
à
des
pétéchies
infra-
millimétriques
non
extensives
et
non
nécrotiques
des
membres
inférieurs.
Il
n’y
avait
pas
d’instabilité
hémodynamique.
Rapi-
dement,
le
patient
a
été
atteint
d’une
confusion
et
d’une
hémiparésie
gauche.
Une
antibiothérapie
intraveineuse
par
4
g
de
ceftriaxone
a
immédiatement
été
débutée,
avant
la
réalisation
d’une
tomodensitométrie
(TDM)
cérébrale
non
in-
jectée.
Cette
TDM
était
normale
(figure
1).
La
réalisation
secondaire
de
la
ponction
lombaire
a
mis
en
évidence
un
liquide
céphalorachidien
(LCR)
purulent
et
des
diplocoques
Gram
négatif
à
l’examen
direct.
Du
fait
d’une
dégradation
rapide
de
la
vigilance,
le
patient
a
été
transféré
en
réanimation.
La
prise
en
charge
a
consisté
en
une
protection
des
voies
aériennes
par
intubation
orotrachéale,
une
poursuite
de
l’anti-
biothérapie
intraveineuse
ciblée
sur
le
méningocoque
par
ceftriaxone
à
100
mg/kg/j
en
deux
injections
et
l’injection
de
10
mg
de
dexaméthasone
toutes
les
six
heures.
Une
heure
plus
tard,
le
patient
avait
une
mydriase
bilatérale
aréactive
ainsi
qu’une
hypertension
artérielle
à
180/100
mmHg
et
une
tachycardie
sinusale
à
180/min.
Une
TDM
cérébrale
a
montré
une
hypertension
intracrânienne
(HTIC)
par
oedème
cérébral,
avec
un
engagement
sous-falcoriel,
sous-tentoriel
et
foraminal
(figure
1).
Après
un
avis
neurochirurgical,
l’indication
de
cra-
niectomie
de
décompression
n’a
pas
été
retenue.
Malgré
un
traitement
médical
de
l’HTIC
par
osmothérapie,
pentothal
intraveineux
et
une
prévention
des
agressions
cérébrales
se-
condaires
d’origine
systémique,
le
patient
a
eu,
moins
de
12
heures
après
son
admission
aux
urgences,
des
signes
cliniques
de
mort
encéphalique.
Le
diagnostic
a
été
confirmé
par
deux
électro-encéphalogrammes
successifs,
à
distance
de
l’arrêt
des
hypnotiques,
en
normothermie
et
après
négativation
de
la
barbitémie.
L’analyse
du
LCR
a
permis
d’identifier
a
posteriori
un
méningocoque
B
ST-32.
La
recherche
de
poly-
morphismes
génétiques
chez
le
patient
a
révélé
un
variant
homozygote
rare
du
facteur
tissulaire.
Discussion
Chez
l’adulte
jeune,
95
%
des
décès
par
méningite
aiguë
bactérienne
sont
attribués
aux
pneumocoques
et
aux
infections
invasives
à
méningocoque
(IIM)
[1].
Le
pronostic
est
lié
au
délai
d’introduction
de
l’antibiothérapie
probabiliste
et
de
la
cortico-
thérapie.
Son
instauration
doit
être
stéréotypée,
rapide
et
conforme
aux
recommandations
éditées
par
la
Société
de
pathologie
infectieuse
de
langue
française
(SPILF)
[2].
Malgré
une
prise
en
charge
optimisée,
la
mortalité
des
IIM
reste
à
10
%
depuis
2003,
témoignant
de
la
virulence
redoutable
de
la
bactérie.
Dans
le
cas
des
méningites
à
méningocoques
ass-
ociées
à
un
Purpura
fulminans,
la
mortalité
est
de
30
%.
Cependant,
2,8
%
des
décès
surviennent
chez
des
patients
n’ayant
ni
instabilité
hémodynamique,
ni
purpura
extensif
[3]
et
sont
attribuables
à
une
mort
encéphalique,
parfois
sans
que
l’on
n’ait
d’élément
explicatif.
Ces
décès
pourraient
être
liés
à
une
virulence
encore
plus
importante
de
la
bactérie
et/ou
à
la
présence
d’un
polymorphisme
génétique
chez
le
patient.
Le
méningocoque
est
un
diplocoque
à
coloration
Gram
négatif.
Il
s’agit
d’une
bactérie
potentiellement
mortelle
du
fait
de
son
tropisme
méningoencéphalitique
et
de
la
gravité
du
sepsis
qu’elle
peut
entraîner.
Cependant,
il
existe
une
multitude
de
méningocoques
dont
le
degré
de
pathogénie
diffère.
L’identi-
fication
du
méningocoque
peut
se
fait
par
l’examen
direct
du
LCR
et
par
des
techniques
de
biologie
moléculaire
telles
que
la
Polymerase
Chain
Reaction
(PCR),
qui
a
une
sensibilité
de
90
%
dans
l’identification
bactérienne
[4].
Le
sérogroupe
B
est
majoritaire
puisqu’il
représente
72
%
des
souches
en
France
et
56
%
en
Europe
[1].
Par
ailleurs,
la
carte
d’identité
génétique
de
chaque
méningocoque
isolé
peut
actuellement
être
identi-
fiée
par
la
méthode
de
Multi
Locus
Sequence
Typing
(MLST),
qui
363 Lettres à la rédaction
Figure
1
Coupes
tomodensitométriques
passant
par
les
ventricules
latéraux
à
H
+
5
et
H
+
7
montrant
l’apparition
d’un
oedème
cérébral
avec
une
hypertension
intracrânienne
tome
42
>
n83
>
mars
2013

permet
la
reconnaissance
du
séquence-type
(ST)
grâce
à
la
caractérisation
de
sept
gènes
constants
dits
«
de
ménage
»
[5].
Un
réseau
européen
de
laboratoires
s’est
alors
organisé
dans
les
buts
de
cartographier
la
distribution
des
souches
et
de
déterminer
le
pronostic
par
l’attribution
d’un
degré
de
virulence
à
chaque
souche
[6].
La
pathogénie
d’une
souche
peut
se
déterminer
par
son
caractère
hyperendémique
telles
que
les
souches
ST-32
et
ST
41/44,
qui
sont
majoritaires
en
France.
De
plus,
certaines
souches
hypervirulentes
telles
que
la
ST-269
sont
responsables
d’un
tableau
clinique
plus
grave
[7].
La
souche
ST-
32,
telle
que
celle
trouvée
chez
notre
patient,
est
prédominante
en
France
(20
%),
mais
n’est
pas
responsable
d’une
surmorta-
lité
[1].
Les
polymorphismes
génétiques
sont
définis
par
la
présence
de
variants
géniques
rendant
certains
individus
plus
sensibles
face
au
risque
infectieux.
Ils
entraînent
soit
une
susceptibilité
accrue
aux
infections,
soit
une
surmortalité
en
cas
de
sepsis
[8].
On
estime
que
1
%
de
la
population
est
porteuse
de
tels
variants
géniques
associés
au
risque
infectieux
[9].
Ils
peuvent
toucher
cinq
grandes
fonctions
:
le
système
ABO,
l’immunité
innée,
l’immunité
acquise,
la
cascade
inflammatoire
et
la
coagula-
tion
(tableau
I).
Dans
notre
observation,
une
recherche
ex-
haustive
des
variants
géniques
susceptibles
d’entraîner
un
sepsis
plus
grave
a
été
réalisée.
Un
variant
homozygote
rare
du
facteur
tissulaire,
responsable
d’un
état
d’hypercoagul-
abilité
en
cas
de
sepsis,
a
été
trouvé
chez
notre
patient
[10].
Ceci
évoque
l’hypothèse
d’une
artérite
cérébrale
thrombo-
sante
suraiguë,
responsable
d’un
oe d è m e
vasogénique
et
cytotoxique
lui-même
ayant
pu
entraîné
l’arrêt
circulatoire
cérébral.
Le
pronostic
d’une
méningite
bactérienne
est
surtout
condi-
tionné
par
la
qualité
de
la
prise
en
charge,
mais
l’observation
que
nous
rapportons
illustre
l’influence
incontestable
de
la
génétique
bactérienne
et
humaine
sur
la
gravité
de
l’infection.
Le
génotypage
bactérien
et
la
recherche
de
polymorphismes
génétiques
chez
les
patients
pourraient
à
l’avenir
être
intégrés
dans
notre
démarche
diagnostique
face
à
une
IIM
dont
la
gravité
est
inhabituelle.
En
effet,
la
connaissance
de
la
carte
génétique
du
patient
et
du
méningocoque
est
une
voie
de
recherche
prometteuse.
Elle
pourrait
intervenir
dans
la
réflexion
diagnostique
et
pronostique
et
permettre
de
fournir
des
éléments
de
réponse
aux
praticiens
et
aux
familles
en
cas
de
décès.
Dans
un
avenir
plus
lointain,
on
peut
espérer
le
développement
de
vaccins
ciblés
sur
les
souches
de
méningo-
coques
les
plus
virulentes,
ainsi
que
d’armes
thérapeutiques
novatrices
telles
que
les
thérapies
géniques
ou
l’immunothéra-
pie
chez
les
patients
porteurs
de
polymorphisme
génétique.
Déclaration
d’intérêts
:
les
auteurs
déclarent
ne
pas
avoir
de
conflits
d’intérêts
en
relation
avec
cet
article.
Références
[1]
Institut
de
veille
sanitaire.
Les
infections
invasives
à
méningocoques
en
France,
en
2009.
BEH
31-32/27
juillet
2010.
[2]
Prise
en
charge
des
méningites
bactériennes
aigues
communautaires
(à
l’exclusion
du
nouveau-né).
17
e
conférence
de
consensus
en
thérapeu-
tique
anti-infectieuse.
Med
Mal
Infect
2009;39:175–86.
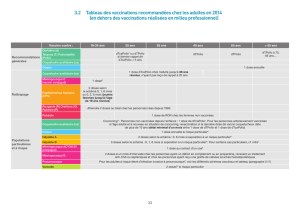
364
Tableau
I
Cibles
et
conséquences
du
polymorphisme
génétique
associé
au
risque
infectieux
[11–13]
Cible
des
polymorphismes
Implications
immunologiques
Implication
clinique
Système
ABO
Favorise
le
portage
pharyngé
du
méningocoque
Susceptibilité
accrue
aux
méningites
Immunité
innée
:
TLRs
MBL
Properdin
(Facteur
P)
Défaut
de
reconnaissance
de
l’antigène
Défaut
d’activation
du
complément
Susceptibilité
accrue
aux
chocs
septiques
Immunité
acquise
:
Récepteurs
FCgIIa
des
polynucléaires
neutrophiles
Défaut
d’activation
de
l’immunité
acquise
Défaut
de
reconnaissance
des
bactéries
encapsulées
(Neisseria
meningitidis)
Inflammation
:
TNF-alpha
Interleukine-1
Interleukine-6
Hyperproduction
de
cytokines
pro-inflammatoires
Défaillances
d’organes
Coagulation
:
Facteur
V
Facteur
tissulaire
t-PA
et
PAI
Activation
de
la
fibrinoformation
et
inhibition
de
la
fibrinolyse
Hypercoagulabilité,
CIVD,
Purpura
fulminans
TLRs
:
Toll-like
Receptors
;
MBL
:
Mannose
Binding
Lectin
;
t-PA
:
Tissue-type
Plasminogen
Activator
;
PAI
:
Plasminogen
Activator
Inhibitor
;
CIVD
:
coagulation
intravasculaire
disséminée
;
TNF-a
:
Tumor
Necrosis
Factor
alpha.
Lettres
a
`la
re
´daction
tome
42
>
n83
>
mars
2013

[3]
Perrocheau
A,
Taha
MK,
Lévy-Bruhl
D.
Epidemiology
of
invasive
meningococcal
disease
in
France
in
2003.
Euro
Surveill
2005;10:238-41.
[4]
Taha
MK.
Simultaneous
approach
for
nonculture
PCR-based
identification
and
serogroup
prediction
of
Neisseria
meningitidis.
J
Clin
Microbiol
2000;38:855-7.
[5]
Maiden
MC,
Bygraves
JA,
Feil
E,
Morelli
G,
Russell
JE,
Urwin
R
et
al.
Multi-
locus
sequence
typing:
a
portable
approach
to
the
identification
of
clones
within
populations
of
pathogenic
microorganisms.
Proc
Natl
Acad
Sci
U
S
A
1998;95:3140-5.
[6]
Racloz
VN,
Luiz
SJ.
The
elusive
meningococcal
meningitis
serogroup:
a
systematic
review
of
serogroup
B
epidemiology.
BMC
Infect
Dis
2010;10:175.
[7]
Law
DK,
Lorange
M,
Ringuette
L,
Dion
R,
Giguere
M,
Henderson
AM.
Invasive
meningococcal
disease
in
Quebec,
Canada,
due
to
an
emerging
clone
of
ST-269
serogroup
B
meningococci
with
serotype
antigen
17
and
serosubtype
antigen
P1.19
(B:17:P1.19).
J
Clin
Microbiol
2006;44:2743-9.
[8]
Joram
N,
Lopez
E,
Texereau
J,
Mira
J-P.
Polymorphismes
génétiques
et
infections.
Med
Mal
Infect
2006;36:314-21.
[9]
Charpentier
J,
Mira
JP.
Rôle
de
l’hôte
au
cours
des
infections
bactériennes
sévères.
Arch
Pediatr
2001;8(Suppl.
4):689-96.
[10]
De
Prost
D,
Moatti
D,
Petit
L,
Ollivier
V.
L’inhibiteur
de
la
voie
du
facteur
tissulaire
(TFPI),
molécule
clé
de
défense
contre
la
thrombose.
STV
1999;11:548-54.
[11]
Kugelberg
E,
Gollan
B,
Tang
CM.
Mechanisms
in
Neisseria
meningitidis
for
resistance
against
complement-mediated
killing.
Vaccine
2008;26:34-9.
[12]
Wright
V,
Hibberd
M,
Levin
M.
Genetic
polymorphisms
in
host
response
to
meningococcal
infection:
the
role
of
susceptibility
and
severity
genes.
Vaccine
2009;(Suppl.
27):B90–102.
[13]
Domingo
P,
Muniz-Diaz
E,
Baraldès
MA,
Arilla
M,
Barquet
N,
Pericas
R
et
al.
Associations
between
Fc
gamma
receptor
IIA
polymorphisms
and
the
risk
and
prognosis
of
meningococcal
disease.
Am
J
Med
2002;112:19-25.
Maximilien
Cruc,
Nicolas
François,
Ariane
Gentile,
Jean-Louis
Koeck,
David
Tran-Van,
Philippe
Labadie
Fédération
d’anesthésie-réanimation,
d’urgence
et
de
chirurgie
ambulatoire,
HIA
Robert-Picque,
33882
Villenave
D’Ornon,
France
Correspondance
:
Maximilien
Cruc,
Hôpital
d’instructions
des
armées
Robert-Picqué,
351,
route
de
Toulouse,
CS
80002,
33882
Villenave
d’Ornon
cedex,
France.
Reçu
le
16
octobre
2011
Accepté
le
15
mars
2012
Disponible
sur
internet
le
13
mai
2012
ß
2012
Elsevier
Masson
SAS.
Tous
droits
réservés
http://dx.doi.org/10.1016/j.lpm.2012.03.011
Hépatite
E
aiguë
révélée
par
des
polyarthralgies
inflammatoires
Inflammatory
polyarthralgia
reveling
acute
hepatitis
E
La
révélation
de
l’hépatite
virale
E
par
une
polyarthrite
aiguë
ou
des
polyarthralgies
inflammatoires
a
rarement
été
publiée,
mais
elle
mérite
d’être
connue.
L’hépatite
virale
E
peut
en
effet
évoluer
vers
la
chronicité
chez
les
patients
immunodé-
primés
et
l’efficacité
du
traitement
antiviral
a
été
récemment
rapportée.
Il
est
donc
important
d’évoquer
le
diagnostic
d’hépa-
tite
virale
E
devant
un
tableau
articulaire
inflammatoire
associé
à
une
cytolyse
hépatique
aiguë
de
cause
incertaine
et,
en
cas
de
confirmation
du
diagnostic,
de
surveiller
l’évolu-
tion
des
patients
immunodéprimés.
Observation
Une
patiente
de
40
ans
consultait
à
la
fin
de
l’été
pour
des
polyarthralgies
inflammatoires
acrales
symétriques
apparues
10
jours
plus
tôt.
Elle
n’avait
aucun
antécédent
personnel
notable,
ne
possédait
pas
d’animal
de
compagnie,
n’avait
pas
ingéré
de
viande
de
porc
ou
de
sanglier
mal
cuite,
ni
fait
de
séjour
en
pays
tropical.
Dix
jours
plus
tôt,
elle
avait
eu
un
syndrome
pseudo-grippal
transitoire.
Les
arthralgies
avaient
atteint
les
articulations
interphalangiennes
proximales,
les
poignets
et
les
avant-pieds.
Elles
suivaient
un
rythme
inflam-
matoire
avec
un
dérouillage
matinal
de
30
minutes.
À
l’ex-
amen,
la
patiente
était
apyrétique
et
non
ictérique.
L’examen
trouvait
une
limitation
douloureuse
de
ces
articulations
sans
épanchement
articulaire,
sans
synovite
ni
ténosynovite.
Il
n’existait
pas
d’exanthème
ou
de
lésion
des
muqueuses,
pas
d’adénopathies
superficielles
ni
d’hépatosplénomégalie.
Sur
le
plan
biologique,
l’hémogramme
était
normal
sans
syn-
drome
inflammatoire
(C-reactive
protein
[CRP]
=
4,2
mg/L).
Il
existait
en
revanche
une
cytolyse
hépatique
(aspartate
amino-
transférase
[ASAT]
=
8
N
;
alanine
aminotransférase
[ALAT]
=
12
N),
sans
cholestase
associée
(phosphatases
alcalines
60
UI/
L
;
bilirubine
=
15
mmol/L).
Le
TP
était
à
100
%.
On
notait
l’absence
d’IgM
anti-VHA,
d’IgM
anti-HBc,
d’Ac
anti-VHC,
d’IgM
anti-CMV,
HSV
1
et
2
et
parvovirus
B19.
La
sérologie
pour
le
virus
de
l’immunodéficience
humaine
(VIH)
1
et
2
et
la
polymerase
chain
reaction
(PCR)
pour
le
virus
de
l’hépatite
C
(VHC)
étaient
négatives.
Il
existait
en
revanche
des
IgM
anti-
VHE
et
la
PCR
du
virus
de
l’hépatite
E
dans
le
sérum
était
positive
;
la
PCR
du
VHE
dans
les
selles
n’a
pas
été
réalisée.
Le
bilan
auto-immun
était
par
ailleurs
négatif
(facteur
rhumatoïde,
anticorps
anti-CCP,
anticorps
anti-nucléaires).
Le
diagnostic
retenu
était
une
hépatite
virale
E
aiguë
auto-
chtone
avec
polyarthralgies
inflammatoires
révélatrices.
L’évo-
lution
était
favorable
sous
traitement
symptomatique
et
la
patiente
est
resté
totalement
asymptomatique
sur
le
plan
articulaire
avec
un
recul
de
2
ans.
La
biologie
hépatique
s’est
normalisé
après
6
semaines
d’évolution.
Discussion
Le
virus
de
l’hépatite
E
(VHE)
est
un
virus
à
ARN
dont
les
sources
de
contamination
et
les
modes
de
transmission
sont
actuelle-
ment
connus
[1,2].
Dans
les
régions
tropicales
et
sub-tropicales,
la
maladie
évolue
sur
un
mode
endémo-épidémique
:
de
transmission
féco-orale,
elle
se
transmet
par
la
consommation
d’eau
contaminée
ou
d’aliments
souillés.
Dans
les
pays
365 Lettres à la rédaction
tome
42
>
n83
>
mars
2013
1
/
3
100%