Le mystère du cuivre

2°10
CHIMIE
PREMIERE PARTIE : « L’UNIVERS »
2014 / 2015
TP SUR LE CHAPITRE 5 « LES ELEMENTS CHIMIQUES DE L’UNIVERS »
LE MYSTERE DU CUIVRE
Q3a)
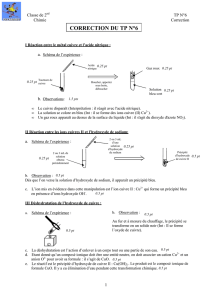
1ERE EXPERIENCE : ACTION DE LA SOUDE SUR LES IONS CUIVRE II
Description littérale de l’expérience : Dans un tube à essais, on introduit 2 mL de solution bleue contenant les ions cuivre II
Cu2+
(aq) puis on ajoute quelques gouttes d’hydroxyde de sodium ou soude (Na+
(aq) + HO
(aq)).
Schéma annoté :
Observation : Un précipité bleu roi d’hydroxyde de cuivre II Cu(OH)2(s) se forme.
Conclusion : L’élément cuivre initialement présent dans les ions cuivre II se retrouve à l’issue de la réaction dans le précipité
d’hydroxyde de cuivre II.
Remarque : L’équation traduisant cette réaction est : Cu2+
(aq) + 2 HO
(aq) Cu(OH)2(s).
2EME EXPERIENCE : CHAUFFAGE D’UN PRECIPITE D’HYDROXYDE DE CUIVRE II
Description littérale de l’expérience : On chauffe modérément quelques instants le tube à essais contenant le précipité
d’hydroxyde de cuivre II Cu(OH)2(s). Cette opération provoque la déshydratation du précipité.
Schéma annoté :
Observation : De l’oxyde de cuivre II noir CuO(s) se forme.
Conclusion : L’élément cuivre initialement présent dans le précipité d’hydroxyde de cuivre II se retrouve à l’issue de la réaction
dans l’oxyde de cuivre II.
Remarque : L’équation traduisant cette déshydratation est : Cu(OH)2(s) CuO(s) + H2O(ℓ).

3EME EXPERIENCE : ACTION DU CARBONE SUR L’OXYDE DE CUIVRE II
Description littérale de l’expérience : On place dans un tube à essais, l’équivalent d’une spatule d’un mélange de carbone C(s) et
d’oxyde de cuivre II CuO(s). On adapte, sur le tube à essais, un tube à dégagement. On chauffe fortement le mélange et dès que le
mélange est porté à incandescence, on plonge l’extrémité du tube à dégagement dans de l’eau de chaux contenue dans un verre à
pied.
Schéma annoté :
Observations : Du cuivre métallique rouge Cu(s) se forme dans le tube à essais tandis qu’un précipité blanc se forme dans l’eau de
chaux, ce dernier témoignant que du dioxyde de carbone s’est également formé.
Conclusion : L’élément cuivre initialement présent dans l’oxyde de cuivre II se retrouve à l’issue de la réaction dans le métal
cuivre.
Remarque : L’équation traduisant cette réaction est : 2 CuO(s) + C(s) CO2(g) + 2 Cu(s).
Q3b) Pour faire « disparaître » le métal cuivre, Tournesol a fait réagir le métal cuivre avec l’acide nitrique.
Q3c)
Cu
Métal cuivre
Action de
l’acide nitrique
Cu2+
Ion cuivre II
Action du carbone et du
chauffage
Action de la soude
CuO
Oxyde de cuivre II
Action du chauffage
Cu(OH)2
Hydroxyde de cuivre II
Q3d)
On constate que l’élément cuivre s’est conservé au cours des différentes réactions chimiques dans lesquelles il a été engagé.
L’élément cuivre peut se définir ainsi : c’est ce qui est commun aux espèces chimiques telles que le métal cuivre Cu(s), l’ion
cuivre II Cu2+
(aq), l’hydroxyde de cuivre II Cu(OH)2(s) et l’oxyde de cuivre II CuO(s), malgré la diversité de leurs apparences.
*****
1
/
2
100%