02/12/2013 BRIS Pierre-Nicolas L3 Immunopathologie et

Immunopathologie et immunointervention – Biothérapie cellulaire
02/12/2013
BRIS Pierre-Nicolas L3
Immunopathologie et immunointervention
Relecteur 11
Pr. Olive
16 pages
Biothérapie cellulaire
A. Rappels
I. Activation des lymphocytes T et réponse immune
Comment activer le Lymphocyte T ?
Le signal d'activation du lymphocyte T vient d'un récepteur qui reconnaît un antigène. Ce récepteur met
en route le système, il est présent à la surface des lymphocytes T. L'antigène reconnu par cette molécule, c'est la
combinaison d'un peptide associé à une molécule HLA, classe I ou II selon que ce soit CD8 ou CD4. Cette
combinaison est portée à la surface des cellules présentant l'antigène. C'est le signal princeps, nécessaire mais
non suffisant pour activer le lymphocyte.
Pour que l'activation du lymphocyte T soit suffisante, il faut un deuxième signal. Le signal 1 joue un
rôle important pour la spécificité, pour la mise en route mais « pour » éviter des problèmes d’auto-immunité,
cette activation est très fortement contrôlée. Le signal qui va lui permettre de fonctionner, c'est la présence de
molécules (dont le prototype est B7-1, B7-2 ou CD80/86) à la surface de la cellule qui amène l'antigène. La
présence de ces molécules est induite, dans le cas d'une infection, par l'activation par le pathogène de la cellule
présentant l'antigène.
1/16
Plan
A. Rappels
I. Activation des lymphocytes T et réponse immune
II. Lymphocytes B et anticorps
B. Système immunitaire et cancer
I. Traitements des cancers
II. Tumeur et micro-environnement tumoral
C. Immunothérapie cellulaire
I. Les différents types d'immunothérapies T
II. Déroulement de la pathologie tumorale
III. Le rôle de l'immunité innée dans la réponse immune anti-tumorale
IV. Les antigènes associés aux tumeurs (TAA)
V. Les différentes stratégies d'immunothérapie active utilisant les TAA
D. Anticorps monoclonaux
I. Histoire des traitements à base d'anticorps monoclonaux
II. Production des anticorps monoclonaux
III. Récapitulatif des différents modes d'action des anticorps thérapeutiques

Immunopathologie et immunointervention – Biothérapie cellulaire
La cellule présentant l'antigène et qui a les
molécules B7-1/B7-2 va activer le LT qui a le
récepteur T ad hoc et la molécule CD28 qui est
la molécule de co-stimulation. Si on a tout ça,
une réponse immune se met en place. Avec ces
bases-là, on peut imaginer des déficits et des
façons d'optimiser ces réponses dans un contexte
pathologique.
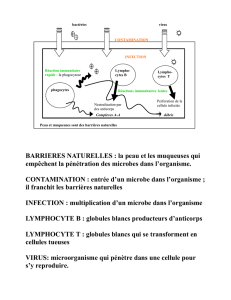
Déroulement d'une réponse immunitaire T
On a trois phases lors d'une réponse immune.
De gauche vers la droite : on a d'abord l'activation du LT par l'antigène lié à HLA et le signal de co-
stimulation.
Ensuite, le LT va proliférer. A ce stade-là, on a des facteurs de croissance qui jouent un rôle moteur dans
ce phénomène. On a historiquement l'Interleukine 2 mais d'autres ont été décrits. Ces cytokines vont permettre
d'avoir une prolifération des cellules pour amplifier la réponse. En même temps, on a une différentiation des
cellules qui vont alors acquérir leur programme fonctionnel pour être le plus efficace possible et acquérir une
fonction différenciée.
2/16

Immunopathologie et immunointervention – Biothérapie cellulaire
A droite, on a la cellule activée. Son fonctionnement est maintenant différent. La cellule activée a quitté
les organes lymphoïdes (rate, etc...) et se trouve dans les tissus périphériques pour lutter contre une infection
par exemple. On a sur l'image une cellule épithéliale infectée par un virus. Dans ce contexte, la cellule activée
est capable d'aller vers le lieu d'infection. Son activation ne dépend alors plus que du récepteur T. Il n'y a plus
besoin du signal de co-stimulation. La cellule de gauche est la cellule dite naïve, celle de droite est la cellule
différenciée qui a la fonction effectrice.
II. Lymphocytes B et anticorps
Le système immunitaire acquis ou adaptatif comprend la réponse T mais aussi les lymphocytes B. Le
lymphocyte B n'a pas d'effet direct pour lutter contre un pathogène mais il fonctionne par procuration : au stade
terminal de sa différentiation, il produit des anticorps. Les anticorps sont intéressants en biothérapie car c'est un
outil très puissant.
Sur cette figure, on voit deux des fonctions les mieux connues d'un anticorps : à gauche, l'activation du
complément. La conséquence de l'activation du complément, c'est que l'anticorps qui va reconnaître son
antigène peut induire la lyse de la cellule qui porte cet antigène grâce au recrutement du complément.
A droite, le recrutement des effecteurs de l'immunité. On peut voir le recrutement d'un phagocyte qui
est apte à interagir avec une structure reconnue par l'anticorps. Dans ce contexte-là, l'anticorps fonctionne à
travers son site appelé le fragment Fc, qui est la partie constante. Le fragment Fc va permettre de recruter les
cellules phagocytaires grâce aux Fc récepteurs présents à la surface de ces cellules.
3/16

Immunopathologie et immunointervention – Biothérapie cellulaire
B. Système immunitaire et cancer
I. Traitements des cancers
Beaucoup de traitements actuels dans le cadre de leucémies, de lymphomes font appel au système
immunitaire. Sur cette diapo, on voit l'ensemble des médicaments utilisés chez un patient atteint de leucémie ou
de lymphome.
A gauche, en vert, on a des traitements classiques : les chimiothérapies et la radiothérapie. Juste en
dessous, on a des traitements qui vont agir sur les oncogènes (molécules impliquées dans le développement du
lymphome, de la leucémie, ex : kinase inhibitors).
Dans la partie haute du camembert, en couleurs mauve et bleue, on a les transplantation de moelle
osseuse ou de cellules souches. La façon dont ça marche, c'est essentiellement à travers ce qu'on appelle la
réponse immunitaire allogénique impliquant surtout des effecteurs immuns qui sont issus le plus souvent de la
sœur ou du frère et qui vont avoir des fonctions anti-tumorales. C'est connu depuis les années 70, c'est un
standard thérapeutique. On peut utiliser des lymphocytes du donneur qu'on injecte en même temps que les
cellules de moelle osseuse ou les cellules souches pour avoir la réponse allogénique.
A droite, on a les anticorps monoclonaux, ce sont des traitements qui sont entrés dans le domaine
thérapeutique de l'immunothérapie des lymphomes depuis 1997. On peut donc utiliser les anticorps, il y a par
exemple CD20. CD est une nomenclature internationale, qui veut dire groupe de différenciation. On peut ainsi
avoir un nom d'anticorps reconnu au niveau international.
CD 20 est le premier et depuis ce domaine se développe avec des cibles portées par les lymphomes et
leucémies.
4/16

Immunopathologie et immunointervention – Biothérapie cellulaire
A côté de ça, on a des thérapies plus expérimentales qui correspondent à l'immunothérapie active. Active
veut dire que ce que l'on va injecter va stimuler une réponse par le système immunitaire du receveur. Cela
permet une vaccination du patient contre quelque chose (tumeur par exemple). Ce sont des thérapies qui font
partie des plus attractives car la réponse dure longtemps mais il existe néanmoins des soucis quant à l'efficacité
vaccinale.
Pour finir, il y a des agents chimiques utilisés tous les jours chez les patients. Le prototype, qui est l'un
des plus intéressants, s'appelle IMID. Ce sont des agents qui modifient les réponses immunes. IMID est un
acronyme anglais qui veut dire Immunomodifiers. Plusieurs composés sont utilisés et certains sont des
traitements utilisés chez les patients atteints de leucémie et de myélome multiple (cancer du plasmocyte).
On a donc dans les stratégies thérapeutiques actuelles des agents qui vont utiliser le système
immunitaire de manière différente par rapport aux thérapies standards.
II. Tumeur et micro-environnement tumoral
a) Le micro-environnement tumoral
Au niveau d'un cancer, on a un environnement complexe avec de nombreux acteurs qui vont au delà de
la tumeur et qui impliquent d'autres partenaires dont le système immunitaire qui est présent au niveau du site.
On a une réponse immune des cellules immunes présentes qui est plus ou moins importante avec une réponse
plutôt CD8 et CD4, de type suppresseur. On a aussi les vaisseaux, du collagène et un stroma avec des
fibroblastes. On ne sait pas répondre à certaines questions comme : pourquoi y a-t-il des différences entre les
différentes tumeurs dans ce microenvironnement tumoral ?
5/16
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
1
/
16
100%