les atomes pour comprendre la transformation chimique

LES ATOMES POUR COMPRENDRE
LA TRANSFORMATION CHIMIQUE
I- Structure de la matière.
1- Les limites du modèle moléculaire.
Lors de la combustion du carbone dans le dioxygène, les réactifs, (C et O2) sont consommés
tandis qu’un produit apparaît (CO2)
L’utilisation des modèles moléculaires ne peut expliquer la formation des produits à partir
des réactifs consommés. Un autre modèle est donc nécessaire pour comprendre les transformations
chimiques
Exemple : Combustion du carbone
+ =
Carbone + dioxygène = dioxyde de carbone
2- Les atomes.
C’est vers 1811 avec les travaux du chimiste AVOGADRO que la distinction entre atomes
et molécules fut faite : Les molécules sont elles mêmes constituées de particules infiniment plus
petites qu’elles : Les atomes (d = 0.1 milliardième de mètre).
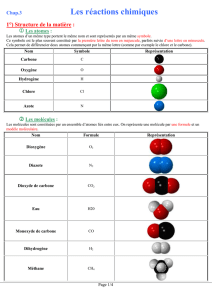
Les atomes sont modélisés par des sphères de couleurs et de tailles différentes et sont
représentés par des symboles.
3- Les molécules
Dans la matière, les atomes sont souvent assemblés pour former des molécules.
Une molécule est représentée par une formule chimique et un modèle moléculaire.
Fiche d’activité à compléter
IMPOSSIBLE !

4- Corps pur et corps composé
Lorsque les atomes formant de la matière sont identiques, cette matière est un corps pur
(C, O2, N2,H2…), dans le cas contraire c’est un corps composé.
II- Interprétation des transformations chimiques.
1- Combustion du carbone.
Un atome de carbone réagit avec une molécule de dioxygène pour former une molécule de
dioxyde de carbone. Le nombre et la « couleur » des atomes sont bien conservés, on dit que
l’équation est équilibrée.
2- Combustion du méthane
Pour l’instant, l’équation chimique n’est pas équilibrée, il faut placer des coefficients
multiplicatifs devant les molécules pour « équilibrer l’équation »

Je retiens :
Au cours d’une transformation chimique, les
atomes présents dans les réactifs ne disparaissent pas mais
s’associent différemment pour donner les produits.
Une transformation chimique conserve le nombre et
la nature des atomes dans les réactifs et dans les produits.
III- La masse varie t’elle au cours d’une transformation
chimique ?
Expérience :
Je retiens :
Au cours d’une transformation chimique, la masse des
réactifs disparus est égale à la masse des produits formés. C’est la loi de la
conservation des atomes au cours d’une transformation chimique.

Activité :
ATOMES ET MOLECULES
Matériel : Boîte de modèles atomiques.
LES ATOMES.
C’est vers 1811 avec les travaux du chimiste AVOGADRO que la distinction entre atomes et molécules fut
faite : Les molécules sont elles mêmes constituées de particules infiniment plus petites qu’elles : Les atomes (d = 0.1
milliardième de mètre).
Les atomes sont modélisés par des sphères de couleurs et de tailles différentes et sont représentés par des symboles
LES MOLECULES
Les molécules sont composées d’atomes liés entres eux.
Une molécule est représentée par une formule chimique et un modèle moléculaire.

1
/
5
100%