Problème 1

DL 11
ÉLECTROMAGNÉTISME – THERMODYNAMIQUE – CRISTALLOGRAPHIE
Problème 1
Microscope à émission d’ions
Le microscope à émission d’ions,
imaginé et construit par Erwin
MÜLLER en 1951, fut le premier
appareil ayant une résolution suf-
fisante pour visualiser des atomes
dans un cristal métallique. Le mi-
croscope se compose d’une pointe
très fine de métal placée dans
une cavité dont la paroi en verre
(l’écran du microscope) est recou-
verte d’un revêtement phosphores-
cent et conducteur. Le dispositif est
rempli d’hélium (ou d’un autre gaz)
à une très basse pression, l’écran est
mis à la masse et un important po-
tentiel électrique positif est appliqué
à la pointe.
À cause de l’effet de pointe, le champ
électrique est très important au ni-
veau de la pointe, et l’on fait en sorte
qu’il soit suffisant pour ioniser les
atomes d’hélium qui passent à proxi-
mité.
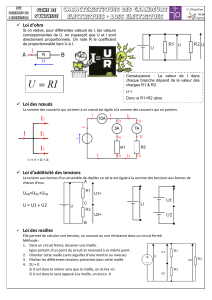
FIGURE 1: Image obtenue à partir d’une
pointe d’iridium. Chaque tache est l’image
d’un atome. Les zones avec des labels sont
des régions qui correspondent aux faces du
cristal, avec des atomes coplanaires. Avec de
l’habitude, on peut distinguer des défauts du
cristal.
L’électron part dans la pointe et l’ion He+est violemment projeté sur l’écran
et y forme une petite tache lumineuse. C’est au voisinage immédiat des
atomes qui composent la pointe que le champ électrique est le plus impor-
tant, et donc les ions d’hélium sont majoritairement formés au niveau de ces
atomes.
L’image produite sur l’écran reproduit donc l’agencement des atomes à la
surface de la pointe.
Seuls quelques aspects de ce dispositif seront abordés dans ce sujet. La pre-
mière partie établit quelques résultats utiles de la théorie cinétique des gaz.
Constantes physiques
Constante de Planck : h=6,63.10−34 J.s
Constante diélectrique du vide : ε0=8,85.10−12 F.m−1
Constante de Boltzmann : kB=1,38.10−23 J.K−1
Constante des gaz parfaits : R=8,31 J.mol−1.K−1
Charge du proton : e=1,6.10−19 C
Masse de l’électron : me=9,1.10−31 kg
Masse de l’hélium : mHe =6,6.10−27 kg
Polarisabilité de l’hélium : αHe =2,5.10−30 m3
Diamètre effectif de l’hélium : dHe =0,19 nm
On prendra les valeurs suivantes pour les applications numériques
Champ électrique à la pointe : E0=4,4.1010V.m−1
Pression dans la cavité : P=0,15 Pa
Rayon de la pointe : r0=30 nm
Rayon de l’écran : Re=15 cm
Température du gaz : T=300 K
On rappelle les valeurs des intégrales suivantes
Z+∞
−∞
e−x2
2d x =p2πZ+∞
−∞
xe−x2
2d x =1
Z+∞
−∞
x2e−x2
2d x =p2πZ+∞
−∞
x3e−x2
2d x =2
1. Partie préliminaire : Théorie cinétique des gaz
1.1. Atmosphère isotherme - facteur de Boltzmann
L’atmosphère terrestre est assimilée à un gaz parfait constitué de molécules
de masse molaire M=29 g.mol−1et plongé dans un champ de pesanteur g

Page 2 DL 11 Lycée Clemenceau Nantes – MPSI
uniforme et dirigé vers le bas avec °
°g°
°=10 m.s−2. On suppose que ce gaz
parfait est à l’équilibre thermodynamique à une température T=300 K.
1.1.1 Établir la loi donnant la pression P(z)en fonction de l’altitude.
1.1.2 Évaluer l’épaisseur caractéristique de l’atmosphère dans ce modèle.
Donner un ordre de grandeur de la pression au sommet de l’Everest.
1.1.3 Montrer que, dans ce modèle, la densité volumique n(z)des molécules
est donnée par
n(z)=n(0)expµ−Ep(z)
E0(T)¶(1)
où Ep(z)est l’énergie potentielle d’une molécule d’altitude zet où E0(T)
est une énergie caractéristique dépendant de la température mais indépen-
dante du gaz considéré. Donner l’expression de E0en fonction de Tet de la
constante de Boltzmann.
1.2. Distribution de Maxwell
On veut maintenant décrire la distribution d’équilibre des vitesses des molé-
cules dans un gaz à la température Tlorsque l’on néglige l’influence de tout
champ extérieur.
1.2.1 Justifier que 〈vx〉=vy®=〈vz〉=0, où 〈.〉représente la valeur moyenne
sur toutes les molécules du gaz et où (vx,vy,vz) sont les trois composantes de
la vitesse en coordonnées cartésiennes.
Par analogie avec l’équation (1), on admet que la densité des molécules dans
l’espace des vitesses est proportionnelle à exp£−Ec(v)/E0(T)¤, où Ec(v)est
l’énergie cinétique d’une molécule. C’est la distribution de MAXWELL.
1.2.2 Montrer que la loi de distribution de probabilité de chacune des com-
posantes (vx,vy,vz) de la vitesse est décrite par une loi " gaussienne " ou "
normale ", et écrire la probabilité pour que les composantes de la vitesse
soient respectivement comprises entre vxet vx+d vx, entre vyet vy+d v yet
entre vzet vz+d vz.
1.2.3 Montrer que la " vitesse quadratique moyenne " vq=rDv2Evérifie
v2
q=3kBT
m
où mest la masse d’une molécule.
On s’intéresse maintenant à la distribution de probabilité de la norme de la
vitesse v=°
°v°
°.
1.2.4 Déterminer la probabilité p(v)d v que cette norme soit comprise entre
vet v+d v. La fonction p(v)est appelée densité de probabilité de v.
1.2.5 En déduire que la valeur moyenne de la norme de la vitesse d’une mo-
lécule est donnée par
〈v〉=s8kBT
πm(2)
1.2.6 Est-il étonnant que vq/〈v〉soit un simple facteur numérique qui ne
dépende pas des caractéristiques du gaz ?
1.3. Chocs sur une surface
On considère une petite surface dS et l’on veut compter le nombre moyen
de chocs de molécules du gaz sur un côté donné de cette surface pendant un
temps τ. On note nle vecteur unitaire sortant normal à l’élément de surface.
Dans un premier temps, on ne compte que les chocs des molécules ayant une
vitesse comprise entre vet v+d v.
1.3.1 De quelle région de l’espace peuvent venir les molécules du gaz sus-
ceptibles de frapper la surface pendant le temps τ? On repère les points de
ce volume par leurs coordonnées sphériques (r,θ,φ) d’axe n(voir la figure).
Quelles sont les valeurs pertinentes de (r,θ,φ) ?
On considère un petit volume dV dans cette région de l’espace.
1.3.2 Exprimez le nombre total de molécules dans le volume dV en fonction
de la pression et de la température du gaz, puis le nombre de molécules avec
une vitesse entre vet v+d v. On exprimera le résultat à l’aide de la fonction
p(v)introduite à la question 1.2.4. Quelle approximation fait-on ? Est-elle
justifiée si l’on veut appliquer ces résultats au microscope ?

Page 3 DL 11 Lycée Clemenceau Nantes – MPSI
1.3.3 Quelle est la proportion des molécules dans le volume dV qui vont dans
la bonne direction pour heurter la surface dS ?
1.3.4 En déduire le nombre moyen de chocs sur la surface dS pendant le
temps τpar des molécules avant une vitesse entre vet v+d v.
1.3.5 On tient maintenant compte de toutes les vitesses possibles. Montrer
que le nombre total moyen de chocs sur la surface dS pendant le temps τest
de la forme τncdS avec
nc=P
p2πmkBT(3)
Préciser la dimension et l’ordre de grandeur de ncdans les conditions de
fonctionnement du microscope.
Problème 2
L’espace est rapporté au repère cartésien (O,x,y,z) et on se situe dans l’air
(assimilé au vide quant aux propriétés diélectriques).
1. Préliminaires :
1. 1. Enoncer le théorème de GAUSS pour l’électrostatique
1. 2. On considère un fil rectiligne illimité porté par (Oz), portant une distri-
bution uniforme de charge λ>0.
1.2. a. Faire l’étude des symétrie et invariance de cette distribution. Expri-
mer le champ E(M)en tout point M de l’espace où il est défini, en fonction des
vecteurs de base des coordonnées cylindriques notés (ur,uθ,uz) et des compo-
santes non nuls du champ.
1. 2. b. En déduire le champ E(M)en M à partir du théorème de GAUSS.
2. Étude d’une plaque infinie uniformément char-
gée.
On considère maintenant une plaque infinie dans le plan O,y,z, uniformé-
ment chargée avec la densité surfacique de charge σ>0.
2. 1. Faire l’étude des symétrie et invariance de cette distribution. Exprimer
le champ E(M)en tout point M de l’espace où il est défini, en fonction des vec-
teurs de base des coordonnées cartésiennes notés (i,j,k) et des composantes
non nuls du champ.
2. 2. En déduire le champ E(M)en M à partir du théorème de GAUSS.
2.3. A.N. Calculer °
°
°E(M)°
°
°pour σ=7,11.10−5C.m−2.
3. Étude de deux plaques infinies uniformément
chargées.
On considère maintenant deux plaques infinies A et B, la première dans le
plan O,y,z, uniformément chargée avec la densité surfacique de charge σ>0,
et la deuxième parallèle à la première translatée du vecteur ei chargée avec
la densité surfacique de charge −σ?.
3.1. Exprimer les champs EAet EBcréés en tout point de l’espace par les
plaques A et B.
3.2. En utilisant le théorème de superposition, exprimer le champ Eà l’exté-
rieur et à l’intérieur des deux plaques. Dessiner quelques lignes de champ.
3.3. Déterminer l’expression de la différence de potentiel VA−VB.
3.4. A.N. Calculer VA−VBpour σ=7,11.10−5C.m−2et e=5µm.
3.5. Sur chacun des plans, isolons par la pensée deux régions identiques
d’aire S. En déduire la capacité Cdu condensateur formé par les deux sur-
faces Sen regard.
Problème 3
On considère la Terre comme une sphère de masse M, à répartition uniforme
de masse, de rayon Ret de centre O.
1. En raisonnant par analogie, donner l’équivalent du théorème de GAUSS
pour la distribution de masse. Justifier l’analogie entre électrostatique et
gravitation.
2. Calculer le champ de gravitation get le potentiel gravitationnel Vcréés
en tout point de l’espace par la Terre.
3. Montrer que le champ à l’extérieur de la Terre n’est pas modifié si on sup-
pose seulement la répartition de masse à symétrie sphérique mais non plus
uniforme.
Problème 4
ATOMISTIQUE
1- Donner la configuration électronique du fer sous forme atomique et des
ions fer II et fer III. On donne Z=26 pour le fer. En réalité la couche de
valence de Fe2+est 4s03d6. Quelle peut en être la raison ?
2- Le fer forme des complexes avec l’ion cyanure CN−et avec l’eau. Donner
la formule de LEWIS de ces deux ligands. Indiquer la forme dans l’espace de
ces deux ligands.

Page 4 DL 11 Lycée Clemenceau Nantes – MPSI
STRUCTURE CRISTALLINE DU FER ET DE L’ACIER
Le fer peut cristalliser sous deux formes selon la température. À basse tem-
pérature, la maille conventionnelle du fer αpossède la structure cubique
centrée (CC) alors qu’à haute température, le fer γadopte la structure cu-
bique à faces centrées (CFC). La transition s’opère à 910 °C à la pression
standard ; puis, au-dessus de 1390 °C, le fer δreprend une structure CC.
Données numériques :
masse molaire du fer M(Fe)= 55,85 g.mol−1, masse molaire du carbone M(C)=
12 g.mol−1, nombre d’Avogadro NA=6,02.1023 mol−1.
1 - Fer α
1-a. Donner la définition d’une maille élémentaire. Par quel(s) paramètre(s)
est-elle déterminée ?
1-b. Dessiner la maille conventionnelle du fer α.
1-c. Combien cette maille renferme-t-elle d’atomes ?
1-d. Définir puis calculer la compacité CCC d’une structure CC en adoptant
le modèle de sphères dures indéformables.
1-e. Calculer le paramètre aαde la maille cubique, sachant qu’à 20 °C la
masse volumique du fer αest ρα=7868 kg.m−3.
1-f. Calculer le rayon Rαde l’atome de fer αà 20 °C.
2 - Influence de la température
Le volume massique du fer αpasse de la valeur v(α)20 =0,1271 cm3.g−1à la
température de 20 °C, à la valeur v(α)910 =0,1321 cm3.g−1à 910 °C, la va-
riation étant linéaire en fonction de la température. L’étude est menée à
pression constante.
2-a. Lequel des trois coefficients thermoélastiques α,βou χTces données
vous permettent-elles de calculer ? En donner la valeur moyenne.
2-b. Entre quelles limites le paramètre de maille varie-t-il entre ces deux
températures ?
2-c. Quel est le rayon de l’atome de fer αà 910 °C ?
Dans la suite, le rayon atomique du fer αsera Rα=125 pm.
3 - Fer γ
3-a. Dessiner la maille conventionnelle du fer γ.
3-b. Combien cette maille renferme-t-elle d’atomes ?
3-c. Calculer la compacité CCFC d’une structure CFC (modèle de sphères
dures indéformables).
3-d. Le rayon atomique du fer γest Rγ=129 pm. Calculer le paramètre aγde
la maille cubique.
3-e. Evaluer le volume massique v(γ)910 du fer γ.
Si le carbone est très soluble dans le fer liquide (au-dessus de 1536 °C), il
n’en va pas de même lorsqu’il se forme une solution solide fer-carbone (fonte
ou acier). En effet, le carbone, dont le rayon atomique vaut RC=77 pm, doit
s’insérer dans les sites octaédriques des mailles cristallines de fer αou de fer
γ.
4 - Sites octaédriques
4-a. Dans la représentation de la maille de fer αci-contre, un site interstitiel
a été singularisé. De quel de type de site s’agit-il ? Est-il régulier ? (réponse
à justifier)
4-b. Quel serait le rayon maximal RMαd’un atome qui s’insérerait dans ce
site sans entraîner de déformation de la structure cristalline? Calculer RMα.
4-c. Où sont situés les sites octaédriques dans le fer γ? S’agit-il d’octaèdres
réguliers ?
4-d. Quel serait le rayon maximal RMγd’un atome qui s’insérerait dans ce
site sans déformer la structure cristalline ? Calculer RMγ.
4-e. Que pouvez-vous en conclure sur la solubilité par insertion du carbone
dans le fer solide ?
5 - Insertion du carbone
Par hypothèse, lorsqu’un atome de carbone s’insère dans le cristal de fer, toutes
les mailles subissent la même expansion. L’insertion de carbone dans le fer α
permet de former un alliage appelé ferrite ; lorsque l’insertion s’opère dans le
fer γ, l’alliage obtenu est dénommé austénite.
5-a. Quelle valeur prend le paramètre de maille du fer αlorsqu’un atome
de carbone s’insère dans un site octaédrique ? À quelle variation relative de
volume cela conduit-il ?

Page 5 DL 11 Lycée Clemenceau Nantes – MPSI
5-b. De même, que devient le paramètre de maille du fer γlorsqu’un atome
de carbone s’insère dans un site octaédrique ? Quelle est la variation relative
de volume induite ?
5-c. Quelles conclusions pouvez-vous en tirer quant à la formation de la fer-
rite et de l’austénite ?
Un acier austénitique contient 1,33% de carbone en masse.
5-d. Quel est le nombre moyen d’atomes de carbone qui ont été insérés par
maille ?
5-e. Calculer la masse volumique de cet acier. Que pensez-vous de ce résul-
tat ?
Problème 5
Les données numériques nécessaires à la résolution du problème sont re-
groupées à la fin de l’énoncé.
Le soufre est un élément chimique de la famille des chalcogènes, de symbole
S et de numéro atomique 16.
On le trouve dans beaucoup de minéraux (sulfures et sulfates) et même sous
forme native, particulièrement dans les régions volcaniques.
I. Structure électronique du soufre et de composés oxygénés
du soufre.
1- Donner la structure électronique de l’atome de soufre dans l’état fonda-
mental.
On considère les espèces suivantes : SOCl2, SO2−
4, l’atome de soufre est
l’atome central.
2- Proposer une structure électronique de LEWIS pour chacune de ces deux
espèces.
3- Représenter leur géométrie d’après la méthode VSEPR.
II. Structure cristalline de la blende.
Le principal minerai de zinc est le sulfure de zinc ZnS de type blende. La
blende, appelée aussi sphalérite, est la variété allotropique du sulfure de
zinc qui cristallise dans le système cubique.
Dans le cristal de blende ZnS, les ions Zn2+et S2−jouent des rôles symé-
triques. On peut ainsi décrire la maille de ce cristal comme constituée d’un
réseau cubique à faces centrées d’ions S2−avec occupation de la moitié des
sites tétraédriques par les ions Zn2+.
4- Dessiner la maille conventionnelle et donner la coordinence des ions Zn2+
et S2−.
5- Donner la formule littérale de la masse volumique ρde la blende en fonc-
tion du paramètre ade la maille, de la constante d’Avogadro NAet des
masses molaires du zinc M(Zn) et du soufre M(S).
6- Calculer la plus petite distance entre les ions Zn2+et S2−dans la struc-
ture blende en fonction du paramètre ade la maille. La comparer aux rayons
ioniques donnés et interpréter ce résultat.
Données pour l’ensemble du problème
Numéros atomiques : Z(C) = 6, Z(O) = 8, Z(S) = 16 et Z(Cl) = 17
Masses molaires atomiques en g.mol−1: M(C) = 12, M(O) = 16
et M(S) = 32
Constante des gaz parfaits : R = 8,31 J.K−1.mol−1
Constante de Nernst à 298 K : ln10 RT
F=0,06 V
Structure de la blende :
paramètre de maille a=540 pm
rayons ioniques r(Zn2+) = 74 pm et r(S2−) = 184 pm
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
1
/
12
100%