Thesis - Archive ouverte UNIGE

Thesis
Reference
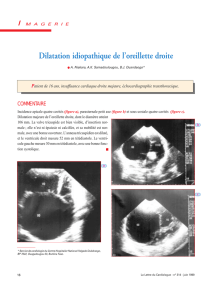
Les masses auriculaires droites : apport de l'échocardiographie
FRANGOS, Caroline
Abstract
L'échocardiographie bidimensionnelle transthoracique et, dans les cas difficiles,
transoesophagienne représente actuellement une des meilleures méthodes non-invasives
pour la détection et le diagnostic des masses auriculaires droites. Le présent travail décrit les
principales masses visibles dans l'oreillette droite : thrombi et masses iatrogènes, tumeurs
cardiaques primaires bénignes (myxome, lipome, fibroeslastome papillaire), malignes
(sarcomes) et tumeurs secondaires (métastases). L'hypertrophie lipomateuse du septum
interauriculaire et l'anévrisme du septum interauriculaire sont des pathologies fréquemment
diagnostiquées depuis l'avènement de l'échocardiographie. Les vestiges embryonnaires tels
que la valve d'Eustachi et le réseau de Chiari sont bien visibles en échocardiographie et
doivent être reconnus. Des structures ou anomalies rares sont également décrites au niveau
de l'oreillette droite telles que kystes, varices ou fistules, de même que l'endocardite du coeur
droit. Après une discussion des principales pathologies et une revue de la littérature, des
présentations de cas illustrent [...]
FRANGOS, Caroline. Les masses auriculaires droites : apport de l'échocardiographie.
Thèse de doctorat : Univ. Genève, 2003, no. Méd. 10325
URN : urn:nbn:ch:unige-3507
Available at:
http://archive-ouverte.unige.ch/unige:350
Disclaimer: layout of this document may differ from the published version.
1 / 1

UNIVERSITE DE GENEVE FACULTE DE MEDECINE
Section de médecine clinique
Département de médecine
interne
Division de cardiologie
______________________________________________________________
Thèse préparée sous la direction
du Docteur Antoine BLOCH
chargé de cours
____________
LES MASSES AURICULAIRES DROITES :
APPORT DE L’ECHOCARDIOGRAPHIE
Thèse
Présentée à la Faculté de Médecine
de L’Université de Genève
pour obtenir le grade de Docteur en médecine
par
Caroline Frangos
de
Genève
______
Thèse N° 10325
Genève 2003

2
LES MASSES AURICULAIRES DROITES :
APPORT DE L’ECHOCARDIOGRAPHIE
I. INTRODUCTION 4
II. ANATOMIE DE L’OREILLETTE DROITE 6
III. ECHOCARDIOGRAPHIE DE L’OREILLETTE DROITE 9
a) ECHOCARDIOGRAPHIE TRANSTHORACIQUE
9
1. ECHOCARDIOGRAPHIE UNIDIMENSIONNELLE (MODE TM) 9
2. ECHOCARDIOGRAPHIE BIDIMENSIONNELLE (2D) 9
b) ECHOCARDIOGRAPHIE TRANSOESOPHAGIENNE
10
c) ECHOCARDIOGRAPHIE TRIDIMENSIONNELLE (3D)
10
IV. THROMBI, MICROTHROMBI ET MICROBULLES 11
a) THROMBUS MOBILE DU CŒUR DROIT 12
b) THROMBUS ADHERENT DU CŒUR DROIT 14
c) MICROBULLES DANS L’OREILLETTE DROITE 15
V. MASSES IATROGENES 16
THROMBUS SUR CATHETER VEINEUX CENTRAL OU
SONDE DE PACEMAKER 16
VI. TUMEURS CARDIAQUES PRIMAIRES 18
a) TUMEURS PRIMAIRES BENIGNES 18
1. MYXOME 18
2. LIPOME 21
3. FIBROELASTOME PAPILLAIRE 22
b) TUMEURS MALIGNES PRIMAIRES 23
1. ANGIOSARCOME 23
2. RHABDOMYOSARCOME 24
3. FIBROSARCOME 24
4. AUTRES TUMEURS MALIGNES 24

3
VII. TUMEURS SECONDAIRES 26
a) LYMPHOME 27
b) MELANOME MALIN 27
c) THYMOME 28
VIII. TUBERCULOSE CARDIAQUE 29
IX. HYPERTROPHIE LIPOMATEUSE DU SEPTUM INTERAURICULAIRE 30
X. ANEVRISME DU SEPTUM INTERAURICULAIRE 32
XI. VESTIGES EMBRYONNAIRES 38
a) INTRODUCTION 38
b) VALVE D’EUSTACHI 39
c) RESEAU DE CHIARI 41
XII. KYSTES 42
a) KYSTE DE LA VALVE D’EUSTACHI 42
b) KYSTE CARDIAQUE ECHINOCOCCIQUE (KYSTE HYDATIQUE) 42
XIII. VARICES 43
XIV. ANEVRISME DE L’AURICULE DROIT 44
XV. ENDOCARDITE 45
XVI. FISTULES CORONAIRES – OREILLETTE DROITE 48
XVII. ARTEFACTS DANS L’OREILLETTE DROITE 52
XVIII. PRESENTATIONS DE CAS 53
XIX. DISCUSSION 63

4
REMERCIEMENTS
Je tiens à exprimer ma gratitude au Professeur Ulrich Sigwart qui m'a fait
l'honneur de présider cette thèse.
Je remercie chaleureusement mon Directeur de thèse, le Dr Antoine Bloch, chargé
de cours, qui m'a apporté une aide précieuse à la réalisation de ce travail par ses
conseils et son active collaboration.
Que soient également remerciés les Drs Marco Bettoni, Stefano Ciaroni, Edoardo
De Benedetti, Jacques Lars Hoffmann, Patrick Schopfer, Jean-Christophe
Stauffer, Marc Zimmermann, ainsi que toute l'équipe de l'Unité de cardiologie non-
invasive de l'Hôpital de la Tour.
J'aimerais enfin témoigner ma reconnaissance à ma famille qui m'a encouragée ainsi
qu'à Mme Nathalie Timmerman pour son excellent travail de dactylographie.
__________________
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
 62
62
 63
63
 64
64
 65
65
1
/
65
100%