Introduction -inégalités d`Heisenberg (mise à jour 09/2014)

Mécanique Quantique
Frédéric Le Quéré
Equipe de Chimie Théorique
Labo de Modélisation et Simulation Multi Echelle
Bât Lavoisier, bureau K35 (3ème étage)
lequere@univ-mlv.fr

semaine mardi jeudi
38 Cours
39 Cours TD
40 TD Cours
41 TD Cours
42 TD Cours
43 TD Cours
44
45 TD Partiel
46 11-nov Cours
47 TD Cours
48 TD Cours
49 TD Cours
50 TD Cours
51 TD TD
52
1
2 TD
Organisation : Partiel
Document autorisé :
Une feuille A4 manuscrite
Examen
Document autorisé :
Une copie double A4 manuscrite
Photocopies interdites

Bibliographie
• P.H. Communay « physique quantique » Groupe de recherche et édition.
• Berkeley « Cours de physique » vol 4 : Méca quantique Armand Colin
• C. Leforestier « Introduction à la Chimie Quantique » Dunod
• Y. Ayant E.Belorizky « Cours de mécanique quantique » Dunod
• C. Cohen Tanoudji, B. Diu, F. Laloé « Mécanique Quantique » Herman.
• http://alpha.univ-mlv.fr/meca

INTRODUCTION
I) Pourquoi a-t-on besoin de la mécanique Quantique ?
• A la fin du XIXème siècle, les lois de la nature semblaient totalement
connues à travers la théorie de la gravitation (Newton) et de
l’électromagnétisme (Maxwell). Deux types de mouvements
mutuellement exclusifs étaient connus :
– Mouvement ondulatoire :
• Caractérisé par la fréquence et la longueur d’onde d’un signal oscillant.
• La lumière est considérée comme une onde à cause des phénomènes
d’interférences (Young).
– Mouvement d’un solide :
• Caractérisé par sa masse, sa position et sa quantité de mouvement.
• Il restait « juste » quelques petits points obscurs ….

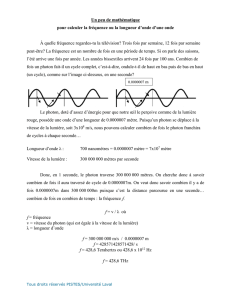
Premier problème : la catastrophe ultra violette.
Lorsque l’on chauffe un solide parfait (appelé corps noir), il émet des ondes
électromagnétiques dans un domaine de longueurs d’ondes caractéristique de sa
température.
λM
Expérimentalement la courbe présente un maximum lié à la température par la
relation de Wien :
λM*T = 2,9.10-3 m.K
En 1900, Rayleigh ne parvient pas à expliquer théoriquement ce phénomène. Son
calcul amène à une équation qui diverge dans l’ultra violet (catastrophe).
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
1
/
36
100%