II Couches et sous-couches électroniques

8
Chimie générale en 30 fiches
Structure de l’atome
I Composition d’un atome
FICHE 1
nuage d’électrons (chargés )
noyau
Z
protons(chargés )
N
neutrons (neutres)
A
nucléons
Symbole :A
ZXX = nom de l’élément chimique
• Z= numéro atomique et A= nombre de masse
Un atome étant électriquement neutre, le nombre d’électrons est égal au nombre de
protons.
• anion = atome ou groupe d’atomes portant une ou plusieurs charge(s) négative(s)
(le nombre de charges (–) doit figurer).
• cation = atome ou groupe d’atomes portant une ou plusieurs charge(s) positive(s)
(le nombre de charges (+) doit figurer).
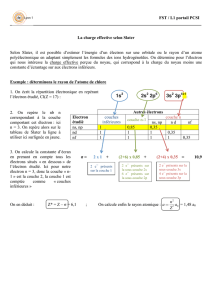
II Couches et sous-couches
électroniques
•Couches électroniques
Les électrons se déplacent sur des couches électroniques, caractérisées par leur
nombre quantique principal n.
n= entier positif non nul : n= 1, 2, 3, etc.
n
= 3
n
= 1
n
= 2
Plus nest élevé, plus
la couche est éloignée
du noyau

9
FICHE 1 – Structure de l’atome
© Dunod – La photocopie non autorisée est un délit.
1
•Sous-couches électroniques
Chaque couche se subdivise en une ou plusieurs sous-couches, dont la forme est carac-
térisée par le nombre quantique secondaire l.
l= entier tel que : 0ln−1
• l=0: sous-couche de type s
• l=1: sous-couche de type p
•l=2: sous-couche de type d
Exemple
Soit la couche n=2; on a l=0ou l=1: la couche n=2est donc
constituée de deux sous-couches notées (2s) et (2p).
•Orientation des sous-couches électroniques
Une sous-couche est formée de une ou plusieurs orbitales, caractérisées chacune par
le nombre quantique magnétique m.
m= entier tel que : −lm+l
On peut associer à chaque orbitale une case quantique :
•Spin d’un électron
Tout électron est caractérisé par son nombre quantique de spin s :s=±1
2.
III Répartition des électrons
•Règles de remplissage
Selon la forme de la sous-couche il y a un nombre limité d’électrons.
• sous-couche de type s : 2 électrons maximum
• sous-couche de type p : 6 électrons maximum
• sous-couche de type d : 10 électrons maximum
Tant que Zn’est pas trop élevé, les électrons doivent garnir complètement les sous-
couches dans l’ordre suivant :
(1s) (2s) (2p) (3s) (3p) (4s) (3d) (4p) …
Quelques exceptions existent (l’atome de chrome, par exemple).
type s
m= 0
une orientation
type p
m= –1 ; 0 ou 1
trois orientations
type d
m= –2 ; –1 ; 0 ; 1 ou 2
cinq orientations

•Configuration électronique : elle donne la répartition des électrons sur les sous-
couches
Exemple de l’atome d’oxygène
(1s)2(2s)2(2p)4
•Couche de valence : c’est la dernière couche occupée.
Exemple de l’atome d’oxygène
(1s)2(2s)2(2p)4
•Répartition des électrons dans les cases quantiques
Règle : les électrons doivent garnir le plus possible de cases quantiques avec un maxi-
mum de 2 par case. L’intérêt des cases quantiques est de déduire le nombre d’électrons
célibataires ou appariés
Exemple de l’atome d’oxygène
10
Chimie générale en 30 fiches
Atome de potassium
1. Donnez la configuration électronique de l’atome de potassium (Z=19) ; justifiez
le fait que le dernier électron a pour nombre quantiques (n=4; l=0; m=0;
s=1
2).
2. Cet atome possède 20 neutrons ; donnez son symbole.
Solution
1. (1s)2(2s)2(2p)6(3s)2(3p)6(4s)1
Le dernier électron est sur une sous-couche (4s), donc n=4; l=0. l=0implique
que m=0; enfin, pour un électron, s=±1
2
2. L’élément chimique potassium a pour symbole K.
Z=19 ; N=20 donc A=39 nucléons d’où : 39
19K.
• • • • • • • •

Configurations électroniques
1. Donnez la configuration électronique des espèces chimiques indiquées ci-dessous,
en précisant à chaque fois la couche de valence et le nombre d’électrons célibataires.
O (Z= 8) ; Al (Z= 13)
2. Donnez la configuration électronique de l’espèce chimique Cl–.
Solution
1. Les couches de valence sont soulignées ci-dessous.
O : Z=8(1s)2(2s)2(2p)4
(2 électrons célibataires)
Al : Z=13 (1s)2(2s)2(2p)6(3s)2(3p)1
(1 électron célibataire)
2. Cl : Z=17 (1s)2(2s)2(2p)6(3s)2(3p)5
Cl– :17 +1=18 électrons : (1s)2(2s)2(2p)6(3s)2(3p)6
Probabilité de présence
d’un électron
On peut montrer que la probabilité pde présence en un point d’un électron apparte-
nant à une sous-couche (1s) ne dépend que de sa distance rau centre du noyau et du
numéro atomique Z de l’atome considéré. On a :
p=K×r2×e(−2×Z×r
a0)avec K=constante et a0=52,9×10−12 m.
Déterminez la valeur de rpour laquelle la probabilité de trouver l’électron est la plus
grande dans le cas de l’atome d’hydrogène (Z= 1).
Solution
Z=1donc p=K×r2×e(−2×r
a0); pmaximale si dp
dr=0
Or dp
dr=K×2×r×e(−2×r
a0)+K×r2×−2
a0×e(−2×r
a0).
dp
dr=0équivaut à : K×2×r×e(−2×r
a0)=K×r2×2
a0×e(−2×r
a0)
Il reste : r=a0=52,9×10−12 m.
11
FICHE 1 – Structure de l’atome
© Dunod – La photocopie non autorisée est un délit.
1
• • • • • •
• • •
1
/
4
100%