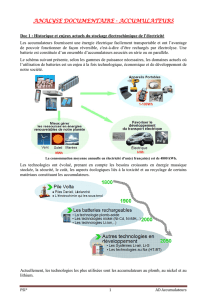
De Volta aux accumulateurs Li-ion

Date de publication :
10 novembre 2016
Mots-clés
Batteries | Stockage
électrochimique | Véhicules
électriques et hybrides
Keywords
batteries | electrochimical
storage | electric and hybrid
vehicles
Pour toute question :
Service Relation clientèle
Techniques de l’Ingénieur
Immeuble Pleyad 1
39, boulevard Ornano
93288 Saint-Denis Cedex
Par mail :
Par téléphone :
00 33 (0)1 53 35 20 20
Réf. : BE8620 V1
De Volta aux accumulateurs
Li-ion - Développement des
batteries au lithium
Cet article est issu de : Énergies | Ressources énergétiques et stockage
par Frédéric LE CRAS, Didier BLOCH
Résumé Depuis leur mise sur le marché en 1991, les accumulateurs lithium-ion ont
envahi notre quotidien : ils alimentent en énergie nos smart phones, ordinateurs portables,
tablettes, vélos électriques, etc. tandis que véhicules électriques et hybrides se répandent
dans les rues. Comment cette technologie s’est-elle, en quelques années, substituée aux
filières établies depuis des décennies? Comment l’industrie Asiatique a-t-elle réussi à
occuper dans ce domaine une position dominante? Quelles seront les prochaines étapes
du développement de ces systèmes de stockage électrique? En replaçant cette
problématique dans un contexte historique, cet article a pour objectif de permettre de
comprendre l’enchaînement des découvertes et des évolutions dans ce domaine, et
d’apporter un éclairage sur les développements en cours
Abstract Since their introduction on the market in 1991, lithium batteries became
ubiquitous: manufactured by tens of millions every month, they feed with energy not only
our smartphones, tablets, electric bikes, but also electric and hybrid vehicles. How did this
technology replace lead acid, nickel cadmium, and nickel hydride batteries existing so far
so rapidly? How could the Asian industry win such a dominant position on the market?
What are the next evolutions of these energy storage systems? This article proposes to
the reader to get a better idea of how the present situation occurred by positioning these
issues in a historical context, and to imagine what could be the possible challenges in the
next future.
Document téléchargé le : 24/11/2016
Pour le compte : 7200083534 - cea saclay // 132.166.84.222
© Techniques de l'Ingénieur | tous droits réservés

BE 8 620 11 - 2016
Copyright © – Techniques de l’Ingénieur – Tous droits réservés BE 8 620 – 1
De Volta aux accumulateurs Li-ion
Développement des batteries au lithium
par Frédéric LE CRAS
Expert senior au CEA – LETI, Grenoble, France
et Didier BLOCH
Responsable de laboratoire au CEA – LITEN, Grenoble, France
ans la longue histoire du développement des systèmes de stockage élec-
trochimique de l’énergie (piles, accumulateur), l’avènement des
accumulateurs au lithium métal, puis lithium-ion représente un tournant. Cette
technologie d’accumulateur utilisant une électrode négative à fort pouvoir
réducteur et par voie de conséquence un électrolyte non aqueux permet,
une fois associée avec une électrode positive adéquate, de générer une force
électromotrice d’environ 4 V. Cette tension élevée est un premier atout pour
permettre de stocker une énergie électrique importante rapportée à la masse et
au volume de l’accumulateur. L’optimisation du choix des matériaux et les
progrès des techniques de fabrication réalisés depuis la mise sur le marché
des premiers accumulateurs Li-ion en 1991 permettent d’atteindre aujourd’hui
des densités d’énergies voisines de 250 Wh · kg–1 et 600 Wh · L–1. Ces valeurs
sont de loin les plus élevées obtenues parmi les systèmes rechargeables fonc-
tionnant à température ambiante.
Les premiers accumulateurs Li-ion ont été conçus et commercialisés initiale-
ment par Sony (et Asahi Kasei) pour l’alimentation de caméscopes. Depuis
1. De la pile Volta aux premières technologies d’accumulateurs
commerciaux......................................................................................... BE 8 620 - 2
2. 1965-1985 : développement des piles au lithium....................... — 3
3. 1970-1991 : boom des systèmes rechargeables ......................... — 4
3.1 Accumulateurs au sodium « haute température »................................ — 4
3.2 Accumulateurs au lithium(-ion).............................................................. — 4
3.3 Accumulateurs nickel-hydrure de métal................................................ — 6
4. Développement des systèmes lithium-ion.................................... — 6
4.1 Spécificité des accumulateurs Li-ion...................................................... — 6
4.2 De nouveaux matériaux pour de meilleures performances................. — 7
4.3 Différents formats d’accumulateur Li-ion.............................................. — 8
5. Évolution des performances et des applications........................ — 9
5.1 Évolution des performances................................................................... — 9
5.2 Évolution des applications...................................................................... — 10
5.3 Principaux producteurs ........................................................................... — 14
5.4 Coût de fabrication des accumulateurs Li-ion....................................... — 16
6. Perspectives d’évolution des accumulateurs au lithium.......... — 19
6.1 Principales évolutions en vue pour la technologie Li-ion .................... — 19
6.2 Nouveaux systèmes utilisant une électrode de lithium métallique .... — 20
7. Conclusion ............................................................................................. — 20
8. Glossaire................................................................................................. — 20
Pour en savoir plus ........................................................................................ Doc. BE 8 620
D
Parution : novembre 2016 - Ce document a ete delivre pour le compte de 7200083534 - cea saclay // 132.166.84.222
Ce document a ete delivre pour le compte de 7200083534 - cea saclay // 132.166.84.222
Ce document a ete delivre pour le compte de 7200083534 - cea saclay // 132.166.84.222tiwekacontentpdf_be8620 v1

DE VOLTA AUX ACCUMULATEURS LI-ION ________________________________________________________________________________________________
Copyright © – Techniques de l’Ingénieur – Tous droits réservés
BE 8 620 – 2
lors, cette technologie a accompagné de manière synergique l’explosion du
marché des appareils électroniques portables et a rapidement supplanté dans
ces applications la technologie d’accumulateur aqueux la plus avancée, le
nickel-hydrure métallique (Ni-MH). Par ailleurs, le rôle clef joué par cette tech-
nologie dans la conception et la réalisation des équipements électroniques
portables, allié à la position de quasi-monopole prise par l’industrie asiatique
sur ces marchés depuis la fin des années 1980, a rapidement conduit à une
intégration de la fabrication des accumulateurs Li-ion au sein des firmes
concernées. Ce positionnement stratégique explique en grande partie la préé-
minence actuelle des fabricants d’accumulateurs japonais, coréens, plus
récemment chinois sur cette production.
Parallèlement, dans un contexte global imposant la réduction de l’utilisation
des énergies fossiles et le recours à des sources d’énergies renouvelables, la
question du stockage de l’énergie électrique devient de plus en plus prégnante.
Considérés il y a peu comme trop coûteux et insuffisamment sûrs, les accumu-
lateurs Li-ion tirent aujourd’hui bénéfice de la maturité technologique de la
filière et pénètrent chaque jour davantage le marché du véhicule électrique et
hybride et du stockage stationnaire à grande échelle. Ces nouveaux domaines
d’application, impliquant de plus forts volumes de production comparés à celui
de l’électronique portable, imposeront sans nul doute de nouveaux développe-
ments à la technologie Li-ion, et motivent dès à présent la recherche de
systèmes « post Li-ion » encore plus performants.
1. De la pile Volta aux
premières technologies
d’accumulateurs
commerciaux
À l’aube du XIXe siècle, après plusieurs décennies d’études empi-
riques des phénomènes galvaniques, Alessandro Volta pose les
premières bases scientifiques de l’électrochimie en étudiant la géné-
ration d’électricité aux bornes d’un empilement (d’où le terme
« pile ») constitué de deux électrodes métalliques (zinc et cuivre)
séparées par un tissu imprégné d’une solution saline. Quelques
décennies plus tard, Michael Faraday énonce une première
« théorie électrochimique » résistante à l’épreuve des faits expéri-
mentaux, comprenant, entre autres, la loi qui porte son nom, selon
laquelle la quantité de matière transformée au cours d’une réaction
est proportionnelle à la quantité d’électricité qui a traversé la cellule
électrochimique. Il propose de nouveaux termes : électrode, anode,
cathode, électrolyte pour définir les constituants d’une telle cellule.
Sur ces bases, de nombreuses initiatives vont contribuer au déve-
loppement de nouveaux systèmes électrochimiques.
Les premiers développements « industriels » de générateurs
électrochimiques débutent vers 1836 avec John Frederic Daniell
qui, pour répondre aux besoins naissants des télécommunications
sans fil, conçoit une pile (–) Zn/H2SO4//CuSO4/Cu (+) générant une
force électromotrice (fem) de 1,1 V. Il faut ensuite attendre 1859
pour que les accumulateurs au plomb soient découverts par
Gaston Planté. Ceux-ci, constitués de deux électrodes de plomb
séparées par une toile de lin et plongées dans de l’acide sulfu-
rique, constituent les premiers systèmes rechargeables et génèrent
une fem d’environ 2 V. Camille Fauré en propose une conception
améliorée en 1881, facilitant sa production en masse pour diffé-
rentes applications (éclairage ferroviaire, stationnaire) dès 1886.
Dès la fin du XIXe siècle, les limitations des accumulateurs au
plomb motivent de nouvelles recherches dans le domaine. Dans ce
contexte, Waldemar Jungner invente en 1899 les accumula-
teurs nickel-cadmium et Thomas Edison contribue en 1901 à
l’émergence de la filière nickel-fer. Ces batteries, très robustes,
offrent une cyclabilité remarquable, qui permet une durée de vie
de l’ordre de vingt ans et une densité d’énergie (40 Wh · kg–1)
supérieure à celle des accumulateurs au plomb. Cela explique
pourquoi elles seront utilisées très tôt pour alimenter des véhi-
cules électriques, et notamment la « Detroit » dès 1911. L’utilisa-
tion des accumulateurs Ni-Fe reste essentiellement cantonnée aux
véhicules ferroviaires et sa production s’arrête en 1975 (Exide). En
revanche, le domaine d’application des accumulateurs Ni-Cd n’a
de cesse de progresser au cours du vingtième siècle. Leur utilisa-
tion s’impose dès les années 1930 pour beaucoup d’applications
embarquées à forte valeur ajoutée telles que l’aéronautique et le
spatial d’abord. La société SAFT (Société des accumulateurs ferro-
viaires et de traction), notamment, en commercialise pour l’alimen-
tation de secours dans le ferroviaire, l’aéronautique et l’éclairage
au cours de la deuxième moitié du XXe siècle. Dans les années
1980, ce système s’impose également pour l’alimentation d’appa-
reils électroniques et d’outillages portables, et en particulier des
premières générations de téléphones mobiles. Détrônés sur ce sec-
teur par les accumulateurs Ni-MH, puis Li-ion à la fin des années
1990, ils restent encore largement utilisés dans les systèmes d’ali-
mentation de secours (meilleure fiabilité que le Pb-acide) et dans le
secteur aéronautique.
Quant aux accumulateurs au plomb, ils représentent encore
de nos jours près de 90 % du marché des accumulateurs vendus
dans le monde (environ 60 % en valeur, figure 1). Peu coûteux, ils
restent parfaitement adaptés aux applications stationnaires (sauve-
garde centraux téléphoniques et serveurs informatiques, ondu-
leurs, stockage d’énergie provenant de sources renouvelables sur
sites isolés...), ainsi qu’à certaines applications embarquées, telles
que les batteries de démarrage, les véhicules micro-hybrides et les
chariots élévateurs.
Parution : novembre 2016 - Ce document a ete delivre pour le compte de 7200083534 - cea saclay // 132.166.84.222
Ce document a ete delivre pour le compte de 7200083534 - cea saclay // 132.166.84.222
Ce document a ete delivre pour le compte de 7200083534 - cea saclay // 132.166.84.222tiwekacontentpdf_be8620 v1

________________________________________________________________________________________________ DE VOLTA AUX ACCUMULATEURS LI-ION
Copyright © – Techniques de l’Ingénieur – Tous droits réservés BE 8 620 – 3
2. 1965-1985 :
développement des piles
au lithium
Les premiers travaux de recherche sur les générateurs au
lithium et au sodium sont initiés à la fin des années 1950, puis
s’intensifient sensiblement, aux États-Unis notamment, durant la
décennie suivante sous l’impulsion de programmes gouvernemen-
taux touchant principalement à la défense et au domaine spatial
(NASA) [1]. Le début des années 1970, voit par la suite l’émer-
gence de systèmes davantage dédiés aux applications électro-
niques grand public, développés principalement par des firmes
japonaises (Sanyo, Matsushita).
Dans tous les cas, la motivation de ces développements est la
réalisation de systèmes d’alimentation et de stockage élec-
triques embarqués présentant une densité d’énergie sensible-
ment plus élevée que celle des systèmes aqueux existants. Une
des caractéristiques des métaux alcalins ( , Na, K...) est en
effet leur fort pouvoir réducteur. La valeur des potentiels standards
des couples A+/A est en effet particulièrement basse (– 3,05 V/ENH
pour Li+/Li) et permet donc d’envisager la réalisation de généra-
teurs électrochimiques présentant une force électromotrice, et
donc une densité d’énergie, nettement supérieure à celle obtenue
avec des électrodes négatives de Zn, de Pb ou de Fe. Par ailleurs,
parmi ces métaux, le lithium et le sodium ont une masse molaire
relativement faible, ce qui est un avantage supplémentaire pour
l’obtention de générateurs électrochimiques à forte densité d’éner-
gie. En contrepartie, ces matériaux sont extrêmement réactifs et
s’oxydent rapidement notamment au contact de l’air et de l’humi-
dité. Pour cette même raison, seuls des électrolytes aprotiques
sont susceptibles de leur être associés.
Dans les années 1950, la démonstration de la stabilité du lithium
métallique dans des solvants aprotiques ouvre la voie à la réalisa-
tion des premières piles au lithium fonctionnant à température
ambiante [2]. Des électrolytes stables vis-à-vis du lithium sont syn-
thétisés à base de solvants purifiés parfaitement anhydres (PC,
γ-butyrolactone, di-méthoxy-éthane...), solubilisant différents sels
de lithium (LiClO4 , LiAsF6 , LiPF6 , LiBF4) [3]. Cette stabilité découle
en réalité de la formation d’une couche de passivation à la surface
du lithium, formée par les produits de décomposition de l’électro-
lyte, constituée de différents composés inorganiques et organiques
et appelée communément SEI (Solid Electrolyte Interphase ) [4].
Une grande variété de matériaux d’électrode positive est alors éva-
luée dans des cellules de ce type. Au final, cela a débouché sur la
fabrication industrielle plus ou moins pérenne de différents types
de piles [5] [6] [7] [8] [9] [10] [11] [12] [13] [14] qui sont détaillés
dans le tableau 1.
Figure 1 – Évolution en valeur du marché des accumulateurs
(doc. Avicenne Energy)
Année
1990 2000
Plomb
NiCd
NiMH
Li-ion
Autres (NaS, redox flow…)
2005
70
60
50
40
30
Milliards de $ US
20
10
0
2010 2013 2014 2015
À l’heure actuelle, les piles Li/FeS2 , Li/MnO2 continuent
d’être commercialisées pour des usages grand public, les piles
Li/CFx pour des usages essentiellement industriels et les piles
Li/I2-PVP et Li/Ag2V4O11 pour l’alimentation des pacemakers.
D’autres technologies de piles sont également utilisées pour
des applications plus spécifiquement industrielles et
militaires : les piles à cathode soluble (Li/SOCl2 , Li/SO2) et les
piles à activation thermique (Li(Si)/FeS2).
Tableau 1 – Piles au lithium à cathode solide fonctionnant à température ambiante
Cathode Tension
nominale
(V)
Densité
d’énergie
(Wh · kg–1)
Densité
d’énergie
(Wh · L–1)
Température de
fonctionnement
(°C)
Date de brevet
ou de mise
sur le marché
Premiers déposants
ou fabricants
Cus 1,5 300 470 – 40 à + 60 1967 SAFT
Dupont de Nemours
FeS21,5 310 560 – 40 à + 60 1971 Eveready
Dupont de Nemours
CuO 1,5-1,2 280 650 – 20 à + 70 1975 SAFT
V2O53,3 240 630 – 40 à + 60 1972 Honeywell
Duracell
Ag2CrO43,1-2,6 310 820 à 900 37 1972 SAFT
MnO23,0 330 700 – 40 à + 70 1976 Sanyo
CFx2,8 260 620 – 40 à + 85 1969 Matsushita
I2-Polyvinylpyridine 2,8 200 à 270 850 à 1 000 37 1972 Catalyst Research Co.
Wilson Greatbach
Parution : novembre 2016 - Ce document a ete delivre pour le compte de 7200083534 - cea saclay // 132.166.84.222
Ce document a ete delivre pour le compte de 7200083534 - cea saclay // 132.166.84.222
Ce document a ete delivre pour le compte de 7200083534 - cea saclay // 132.166.84.222tiwekacontentpdf_be8620 v1

DE VOLTA AUX ACCUMULATEURS LI-ION ________________________________________________________________________________________________
Copyright © – Techniques de l’Ingénieur – Tous droits réservés
BE 8 620 – 4
3. 1970-1991 : boom
des systèmes
rechargeables
Le regain d’intérêt pour le véhicule électrique après le choc
pétrolier de 1973, le développement exponentiel de l’électronique
grand public à partir de la fin des années 1970 et le plafonnement
des performances des accumulateurs Ni-Cd conduisent à une accé-
lération des recherches dans le domaine des accumulateurs. Dans
cette quête de sources d’énergie embarquées pour des applica-
tions grand public, les critères de performance tels que la densité
d’énergie, la cyclabilité, le coût sont d’abord privilégiés, avant que
la sûreté de ces systèmes ne devienne la préoccupation majeure.
Différentes avancées conduisent au développement de filières
d’accumulateurs distinctes : la découverte d’électrolytes solides
céramiques ouvre la voie aux accumulateurs fonctionnant à haute
température, celle d’alliages hydrurables à température ambiante
permet la conception des accumulateurs aqueux « alcalins »
Ni-MH, la connaissance des matériaux d’intercalation permet la
conversion des piles au lithium en système rechargeables, et au
bout du compte celle des premiers accumulateurs Li-ion.
3.1 Accumulateurs au sodium « haute
température »
Les premiers accumulateurs à électrode négative en métal alcalin
à voir réellement le jour sont des systèmes fonctionnant à haute
température (> 300 °C). Le plus emblématique d’entre eux est le sys-
tème sodium soufre (Na-S) inventé et perfectionné par Ford
Motors Co. et General Electric dès le milieu des années 1960 [15]. Sa
conception tire parti de la découverte des propriétés de conduction
ionique de matériaux céramiques, et notamment de l’alumine bêta
(β’’-Al2O3) qui est un oxyde mixte d’aluminium et de sodium de
composition 11Al2O3-xNa2O (x~1-2) dopé au Mg, dont la structure
cristalline présente des chemins de conduction des ions sodium. Sa
conductivité est faible à température ambiante (~ 10–2 S · cm–1),
mais atteint une valeur nettement plus élevée à 300 °C (~ 0,2 à
0,4 S · cm–1), compatible avec une utilisation pratique [16]. Ces accu-
mulateurs fonctionnent généralement à une température stabilisée
autour de 350 °C, à laquelle le sodium et le soufre sont sous forme
liquide. L’électrode positive est constituée d’un feutre de carbone
imprégné de soufre liquide. La réaction réversible :
se déroule à environ 2 V/Na+/Na et fait intervenir différents polysul-
fures de sodium Na2Sx comme intermédiaires réactionnels. De
nombreux incidents émaillent le développement de cette technolo-
gie et mettent en évidence la fragilité de l’électrolyte céramique
vis-à-vis des sollicitations thermomécaniques pouvant conduire à
une mise en contact direct du soufre et du sodium fondus. L’appli-
cation visée à l’origine, le véhicule électrique, est abandonnée au
profit du stockage stationnaire de grande dimension. De telles ins-
tallations dédiées à l’écrêtage des pics de production électrique ou
couplées à des sources d’énergie renouvelables (éolien, photovol-
taïque) fonctionnent actuellement au Japon (par exemple, l’instal-
lation de NGK insulators 245 MWh, 34 MW à Rokkasho).
Une variante du système Na-S appelée accumulateur ZEBRA
(Zeolite Battery Research Africa ) est développée à partir de 1985
en Afrique du Sud par le CSIR (Council for Scientific and Industrial
Research). Dans ce système, le soufre est remplacé par du chlorure
de nickel additionné d’un sel de sodium NaAlCl4 permettant
d’assurer la conduction ionique dans le compartiment positif. À la
température de fonctionnement nominale (270 à 350 °C), la
réaction :
est réversible. Cette technologie permet d’atteindre des perfor-
mances convenables (150 W · kg–1, 81 Wh · kg–1 pour une batterie
de complète de 30 kWh). Elle est introduite dans des véhicules
électriques en 1998 (Mercedes Classe A), mais doit être abandon-
née pour des questions de sûreté. Ces accumulateurs sont produits
actuellement par Fiamm SoNick en Italie pour des applications
essentiellement liées au stockage stationnaire (onduleurs,
couplage énergies renouvelables). De nouveaux travaux entrepris
en 2010 par General Electric pour améliorer cette technologie ont
été interrompus en 2015.
Des systèmes rechargeables au lithium fonctionnant à haute
température sont développés à partir du début des années 1970 au
sein des laboratoires américains d’Argonne [17] et de Sandia, rapi-
dement suivis par Toyota [18] après 1973. Après des essais infruc-
tueux de transposition du système Na-S au lithium, une
technologie utilisant un électrolyte en sels fondus (eutectique
LiCl-KCl) et le couple de matériaux d’électrode Li(Al)/FeS2 , solides
à la température de fonctionnement (450 à 500 °C), a été dévelop-
pée. Il s’avère en effet que la réaction de conversion :
est parfaitement réversible à haute température. C’est également
le cas pour d’autres sulfures métalliques ; cependant, des considé-
rations de coût amènent à privilégier le disulfure de fer. Le déve-
loppement de ces accumulateurs se prolonge jusqu’au début des
années 1990 [19] pour aboutir à des performances intéressantes
(180 Wh · kg–1, 400 W · kg–1), sans pour autant que cela débouche
sur une utilisation commerciale dans le domaine du véhicule élec-
trique.
3.2 Accumulateurs au lithium(-ion)
3.2.1 Systèmes rechargeables à électrode
de lithium métallique
L’application des concepts d’électrodes à insertion [20] [21] aux
dispositifs de stockage électrochimique de l’énergie, discutée au
cours de la conférence « NATO Advanced Study Institute on Fast
Ion Transport in Solids, Solid State Batteries and Devices » à Belgi-
rate (Italie) en septembre 1972, jette les bases du développement
des accumulateurs au lithium, puis par la suite Li-ion, fonctionnant
à température ambiante. Les électrodes à insertion sont en effet
constituées de matériaux, conducteurs mixtes ioniques et électro-
niques qui, de par leur structure cristallographique et leur compo-
sition, sont susceptibles de permettre l’insertion/désinsertion
d’ions au sein de leur structure et de compenser ce transfert de
charge ionique par un transfert électronique. Les dichalcogénures
de métaux de transition (TaS2 , TiS2 , MoS2...), constitués de feuil-
lets d’octaèdres MS6 maintenus entre eux par des liaisons faibles
de type Van der Waals et offrant des sites cristallographiques
vacants susceptibles d’accueillir des atomes supplémentaires entre
ces feuillets, en sont des exemples emblématiques. En 1974, Stan-
ley Whittingham démontre dans un premier temps la possibilité
d’y insérer électrochimiquement des ions Ag+ [22], puis transpose
ce travail au lithium. Il met en évidence la bonne réversibilité de
cette réaction d’intercalation du Li+ (figure 2) et le comporte-
ment de solution solide des composés LixTiS2 (0 < x < 1). Logique-
ment, il dépose un brevet concernant l’utilisation du TiS2 comme
électrode positive dans des systèmes réversibles (accumulateurs)
au lithium en 1976 [23] [24].
Par la suite, la société Exxon Entreprises (division batteries)
conçoit et commercialise durant la période 1976-1978 le premier
système rechargeable fonctionnant à température ambiante, des-
tiné à l’alimentation des montres. Il est constitué d’une électrode
positive de TiS2 , d’un électrolyte liquide (LiBPh4 dans 1,3 dioxo-
lane), d’un séparateur microporeux en polyoléfine (Celgard) et
d’un alliage LiAl comme électrode négative. Le prix élevé du TiS2
stœchiométrique et la cyclabilité très modeste obtenue au bout du
Parution : novembre 2016 - Ce document a ete delivre pour le compte de 7200083534 - cea saclay // 132.166.84.222
Ce document a ete delivre pour le compte de 7200083534 - cea saclay // 132.166.84.222
Ce document a ete delivre pour le compte de 7200083534 - cea saclay // 132.166.84.222tiwekacontentpdf_be8620 v1
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
1
/
26
100%