Technique d`identification ou de séparation : la CHROMATOGRAPHI

Objectifs : - Définir ce qu’est un élément chimique
- Mettre en évidence la conservation de l’élément chimique
au cours d’une chaîne de transformations chimiques
- Réaliser un organigramme résumant les étapes du cycle du
cuivre
Présentation de l’élément cuivre sous diverses formes :
Le cuivre métallique
Cu
L’ion cuivre II
Cu2+
L’oxyde de cuivre II
CuO
L’hydroxyde de cuivre II
Cu(OH)2
Métal rouge
Les solutions qui le
contiennent sont bleues
Solide noir
Solide bleu
I. Quelques réactions mettant en jeu l’élément cuivre
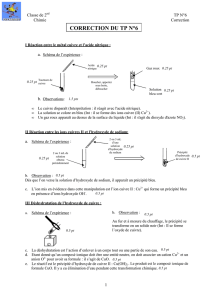
1°) Action de l’acide nitrique sur le métal cuivre (manipulation faite par le professeur !)
Travail à effectuer
Le cuivre réagit avec l’acide nitrique ..la solution devient bleue et il y a
degagement d’une vapeur rousse
cette manipulation est dangereuse a cause du degagement de NO2 roux
Le métal cuivre n’est plus présent , il s’est transformé en ions Cu2+. Ces ions
colorent la solution en bleu
Compléter la transformation suivante :
2°) Action de l’hydroxyde de sodium (Na++HO-) sur une solution contenant l’ion cuivre II.
On observe la formation d’un précipité bleu solide
Cu(OH)2. C’est de l’hydroxyde de cuivre
Compléter la transformation suivante :
3°) Déshydratation du précipité bleu obtenu au 2°)
Mode opératoire :
Chauffer modérément à la flamme du bec bunsen, le tube contenant le solide précédent.
Travail à effectuer
Le precipité bleue noircit
H2O. déshydratation signifie enlever l’eau
Le nom du composé formé est oxyde de cuivre
Compléter la transformation suivante :
4°) Action du carbone sur le solide noir obtenu au 3°) (bien lire la remarque ci-dessous !)
Travail à effectuer
Des grains couleur rouge se forment et l’eau de chaux se trouble
Les 2 réactifs sont l’oxyde de cuivre (CuO) et le carbone ( C)
Les 2 produits formés sont le CO2 et le cuivre Cu
Oxyde de cuivre + carbone = dioxyde de carbone+ cuivre
2CuO + C = CO2 + 2Cu
II. Conclusion
Après l’avoir recopié, compléter l’organigramme ci-dessous résumant toutes les
manipulations effectuée
CORRECTION DU TP 6 : CONSERVATION
DE L’ELEMENT CHIMIQUE
C
H
I
M
I
E
Cu Cu2+
Cu2+ Cu(OH)2.
Cu(OH)2 CuO
Cuivre métallique rouge (Cu)
Ions cuivre II(Cu2+)
Hydroxyde de
cuivre(Cu(OH)2)
Oxyde de cuivre (CuO)
Action de
Acide nitrique
Déshydratation
Action de (Na+ + OH-)
Action du
carbone+chauffag
e
1
/
1
100%