radioactivité

CHAPITRE P 4
RADIOACTIVITÉ
Historique
I) LE NOYAU ATOMIQUE
1) composition et symbole
2) dimensions et masse du noyau
3) isotopes
4) stabilité du noyau atomique ; diagramme de SEGRE
II) LA RADIOACTIVITE
1) définition
2) propriétés
3) différents types de radioactivité
- radioactivité
- radioactivité
- radioactivité +
- radioactivité
III) ENVIRONNEMENT ET APPLICATIONS
1) radioactivité naturelle et artificielle
2) effets biologiques de la radioactivité
3) applications de la radioactivité
Historique
découverte : BECQUEREL (1895) ; Marie et Pierre CURIE (1898)
radioactivité artificielle : Irène et Frédéric JOLIOT-CURIE ( 1934 )
première pile atomique : FERMI ( 1942 )
bombes : à fission( Hiroshima 1945 ) ; à fusion ( Bikini 1952 )
centrales nucléaires : années 50 ; 80 % de l’électricité actuelle est
« nucléaire »
Qu’est-ce que la radioactivité ? Quelles sont ses lois et ses applications ?

I) LE NOYAU ATOMIQUE
1) composition et symbole
composition : nucléons : protons et neutrons
symbole d’un noyau
exemples
nom
hydrogène
carbone
fer
uranium
symbole
H
1
1
C
12
6
Fe
56
26
U
238
92
nombre de masse A
1
12
56
238
nombre de protons Z
1
6
26
92
nombre de neutrons N = A Z
0
6
30
146
2) dimensions et masse du noyau
dimensions :
La matière a une structure lacunaire.
masse :
mp mn 1,67.10–27 kg mélectron 9,1.10-31 kg
m
m
électron
nucléon
2 000
exemple :
U
238
92
9,1.10 92 10-
1,67. 238
=
m électrons
mnoyau
31-
x
27
x
4700 mélectrons mnoyau
La masse d’un atome est concentrée dans son noyau
3) isotopes
a) définition :
2 noyaux, isotopes d’un même élément, ont le même numéro atomique Z mais
des nombres de masses A différents : ils ont même nombre de protons,
mais des nombres de neutrons différents.
X
A
Z
A = nombre de masse = nombre total de nucléons dans le noyau
Z = numéro atomique = nombre de protons dans le noyau
N = A – Z = nombre de neutrons dans le noyau
ratome
0,1 nm ( 1 nanomètre = 10-9 m )
rnoyau
1 fm ( 1 femtomètre = 10-15 m )
r 5
atome 10
rnoyau

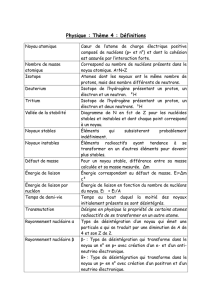
On distingue 4 zones de couleurs différentes :
Une zone centrale rouge appelée vallée de
stabilité est constituée des noyaux stables.
On note que pour Z < 30 les noyaux stables
sont situés près de la première bissectrice,
où N = Z.
Les trois autres zones (bleue, verte et
jaune) sont constituées de noyaux instables.
b) exemples
hydrogène
carbone
uranium
symboles
H
1
1
H
2
1
H
3
1
C
12
6
C
13
6
C
14
6
U
238
92
U
235
92
U
234
92
Z
1
1
1
6
6
6
92
92
92
A
1
2
3
12
13
14
238
235
234
N = A – Z
0
1
2
6
7
8
146
143
142
masse
molaire
( g / mol )
1
2
3
12
13
14
238
235
234
abondance
( en % )
99,98
0,02
traces
98,9
1,1
traces
99,3
0,7
traces
4) stabilité du noyau atomique ; diagramme de SEGRE
Comment un noyau peut-il être stable, puisque les protons se repoussent ? Entre 2
protons distants de 10 –14 m, Fgrav 2.10-36 N et Félec 2N Fgrav, le noyau devrait
«exploser». On admet qu’il existe une force d’attraction, l’interaction forte, entre
nucléons.
Sous l'action des différentes forces en présence, certains noyaux sont stables (ils
ont une grande durée de vie) et d'autres sont instables (ils se détruisent
rapidement).
Actuellement, environ 2000 noyaux ont pu être synthétisés (pour 118 éléments)
Parmi ces 2000 noyaux, 250 seulement sont stables.
On peut classer tous les noyaux connus dans un graphique appelé diagramme de
Segré (page 81 du livre), représentant le nombre de neutrons N en fonction du
nombre de protons Z .

II) LA RADIOACTIVITE
1) Définition
La radioactivité est la propriété de noyaux instables de se transformer spontanément
en d’autres noyaux, avec émission de particules ou , accompagnée souvent d’un
rayonnement .
C’est une réaction nucléaire, caractéristique du noyau père qui se désintègre : elle ne
fait pas intervenir les électrons, contrairement à une réaction chimique.
noyau père noyau fils + particule ou + rayonnement
2) Propriétés
Les réactions nucléaires sont :
aléatoires : il n’est pas possible de prévoir la date d’une désintégration
spontanées
inéluctables : rien ne peut les arrêter, elles sont indépendantes des
facteurs habituels (pression , température , catalyseurs…)
caractéristiques du noyau et pas des liaisons chimiques
la radioactivité de l’uranium est identique que ce soit le métal uranium , UO2 ,
UO2 SO4 , UF6 …
exothermiques : électricité nucléaire , bombe A et bombe H …
3) différents types de radioactivités
a) lois de conservation : lois de Soddy.
Au cours d’une réaction nucléaire , il y a conservation du nombre total de nucléons
et du nombre total de charges.
X
A
Z
Y
A1
1
Z
+
particule
A2
Z2
b) radioactivité
La radioactivité α concerne les noyaux lourds (A grand) : zone jaune du diagramme de
Segré ci-dessus.
Le noyau fils contient 2 protons et 2 neutrons de moins que le noyau père.
exemples :
U
238
92
He
4
2
+
Th
234
90
A = A1 + A2
Z = Z1 + Z2
La radioactivité α est l’émission par le noyau père d’une particule , c’est-à-dire
un noyau d’hélium :
X
A
Z
He
4
2
+
Y
4 -A 2 -Z

Ra
226
88
He
4
2
+
Rn
222
86
c) radioactivité -
La radioactivité β- concerne des noyaux qui présentent un excès de neutrons par
rapport aux noyaux stables de même nombre de masse A : zone bleue du diagramme
de Segré.
Le noyau fils contient 1 proton de plus et 1 neutron de moins que le noyau père.
exemples :
C
14
6
e
0
1-
+
N
14
7
Co
60
27
e
0
1-
+
Ni
60
28
d) radioactivité +
La radioactivité β+ concerne des noyaux qui présentent un excès de protons par
rapport aux noyaux stables de même nombre de masse A : zone verte du diagramme
de Segré.
Les forces électrostatiques entre protons sont plus fortes que les forces nucléaires
entre nucléons.
Le noyau fils contient 1 proton de moins et 1 neutron de plus que le noyau père.
exemples :
N
13
7
e
0
1
+
C
13
6
P
30
15
e
0
1
+
Si
30
14
e) désexcitation
Le noyau fils est en général obtenu dans un état excité (niveau d'énergie élevé). Cet
état est instable, le noyau se désexcite en évacuant cette énergie excédentaire, en
émettant un rayonnement électromagnétique , très pénétrant et énergétique
(longueur d’onde très courte, de 0,1 nm à 0,1 pm)
La radioactivité β- est l’émission par le noyau père d’une particule -, c’est-à-dire
d’un électron
e
0
1 -
:
X
A
Z
e
0
1 -
+
Y
A
1 Z +
La radioactivité β+ est l’émission par le noyau père d’une particule +, c’est-à-dire
d’un électron positif ou positon
e
0
1 +
:
X
A
Z
e
0
1 +
+
Y
A
1 -Z
La radioactivité est la désexcitation du noyau fils par émission d’un rayonnement :
noyau fils X* noyau fils désexcité X +
 6
6
1
/
6
100%