I. Travailler … a Capella (11 points)

17/04/2017 769783420 1/2
Le 30/11/2012
Devoir n° (1h) - Correction
Page : 1/2
I. Travailler … a Capella (11 points)
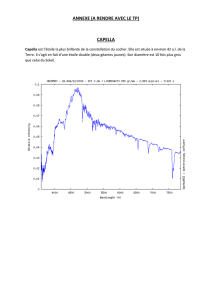
1. La carte d’identité de Capella
1.1. Compléter la phrase suivante : « A travers le télescope, l’astrophysicien voit l’étoile Capella telle qu’elle
brillait il y a 42 ans. Voir loin, c’est voir tôt »
1.2. Il s’agit d’un spectre de raies d’absorption car on observe des raies noires sur un fond coloré.
1.3.
longueur d’onde (nm)
400
434
486
527
656
L (cm)
0
2,0
5,0
7,5
15
1.4. Voir graphe
1.5. La courbe tracée est une droite représentant une fonction affine car elle ne passe par l’origine (0 ; 0) mais par
le point (400 ; 0).
1.6. En utilisant le graphe, pour L = 6,0 cm, (Mg) = 502 nm.
1.7. Pour une longueur d’onde = 580 nm, la distance attendue entre cette raie et la raie de longueur d’onde
400 nm prise pour origine est d’après le graphe D = 10,5 cm. Voir le spectre pour la place de cette raie.
2. Quelle est la couleur de Capella ?
2.1. T(°Celsius) = T(Kelvin) - 273 = 2530 - 273 = 2257 °C
2.2. Les longueurs d’onde extrêmes du domaine du visible sont 400 nm et 800 nm.
2.3. max T = 1,9 10 6 donc max =
Error!
=
Error!
= 751 nm
750 nm.
La couleur de cette étoile est rouge car la longueur d’onde est proche de 800 nm.
2.4. Mars appelée la «planète rouge» n’est pas une étoile et n’est donc pas rouge parce qu’il y règne une
température identique à la température qui règne à la surface de Capella mais simplement parce que la
surface de Mars est couverte de roche riche en oxyde de fer. La température moyenne à la surface de Mars
est de - 50°C.
II. Les éléments chimiques et la classification périodique (9 points + Bonus : 1 point )
H
He
Li
Be
B
C
N
O
F
Ne
Na
Mg
Al
symbole : Si
nom : silicium
P
symbole : S
nom : soufre
Cl
Ar
1) les éléments chimiques sont classés dans la classification périodique actuelle par numéro atomique croissant
suivant une ligne et par propriétés chimiques semblables suivant une colonne.
2) L’élément azote N a pour numéro atomique Z = 7, l’élément chlore Cl Z = 17 et l’élément phosphore P, Z = 15.
3) La structure électronique du lithium Li (Z = 3) est K2L1
La structure électronique de l’aluminium Al (Z = 13) est K2L8M3
4) L’élément chlore appartient à la famille des halogènes.
5) La famille des alcalino-terreux correspond à la 2ème colonne de la classification périodique : élément Be et Mg.
6) l’atome de chlore a pour structure électronique K2L8M7. Pour obtenir la structure électronique d’un gaz rare, il doit
gagner un électron pour former un ion chlorure Cl de structure électronique K2L8M8. L’ion formé est un anion car
il porte une charge négative.
7) Les « isotopes » sont des éléments qui ont même nombre de protons mais un nombre de nucléons différents
8) L’isotope 31P a 15 protons, 31 nucléons soit 16 neutrons et 15 électrons dans son nuage électronique
L’isotope 32P a 15 protons, 32 nucléons soit 17 neutrons et 15 électrons dans son nuage électronique
9) Bonus (1point) : Voir la classification périodique
580

17/04/2017 769783420 2/2
I
1.1
1
2
/22
1.2
1
2
1.3
1
2
3
1.4
1
2
1.5
1
2
1.6
1
2
1.7
1
2
2.1
1
2.2
1
2.3
1
2
3
2.4
1
2
II
1
1
2
/20
2
1
2
3
3
1
2
4
1
5
1
6
1
2
3
4
7
1
2
8
1
2
3
9
1
2
TOTAL : ............ /42
NOTE : ............ /20
CS : erreur de chiffres significatifs
U : oubli ou erreur d’unités
1
/
2
100%