La cellule, ses organites et leurs fonctions

La cellule, ses organites et leurs fonctions
La mitochondrie
Dans cette ressource nous nous focaliserons sur la mitochondrie, sa
morphologie, ses membranes (et leurs nombreux transporteurs) et son rôle
primordial dans la production de l'ATP nécessaire au déroulement des
fonctions cellulaires (fournisseur universel de l'énergie). La production de
l'ATP nécessite un fort approvisionnement en métabolites tels que glucose et
acides gras (et dans le cas de dénutrition extrême, acides aminés), un
approvisionnement géré à partir des réserves par des hormones (glucagon,
insuline et adrénaline). Les métabolites vont être convertis en NADH et
FADH2 (plus CO2) dans des processus, comme la glycolyse, la β-oxydation
et le cycle de l'acide citrique, pour finalement alimenter la chaîne respiratoire
aboutissant à la production de l'ATP grâce au phénomène de chimiosmose.
Les processus se déroulent dans des sites bien déterminés et le passage de
métabolites d'un site à l'autre est assuré par de nombreux transporteurs. En
plus de son rôle de production d'ATP, la mitochondrie est également
présentée pour son intervention dans la synthèse des stéroïdes, la mort
cellulaire programmée (apoptose) et l'homéostasie cellulaire du calcium.
Enfin dans trois « excursions », la mitochondrie est replacée dans un contexte
conceptuel élargi, ouvrant sur des implications aussi variées que diabète sucré
et paléontologie.
Prérequis :
Savoir que, dans leur grande majorité, les fonctions cellulaires
nécessitent l'hydrolyse de l'ATP : par exemple, contraction musculaire,
pompes ATPasiques ou encore transport des organites par les protéines
motrices.
Bien dominer les connaissances sur les diverses modalités de passage
de composants cellulaires au travers de la membrane lipidique.
Avoir une notion de la structure chimique des lipides et des glucides, de
leurs formes de stockage et de leur dégradation en métabolites
utilisables.
Connaître l'essentiel des voies métaboliques telles que glycolyse, cycle
de l'acide citrique et β-oxydation.
Objectifs :

Connaître les sites de localisation des différents processus métaboliques
qui aboutissent à la production de l'ATP (glycolyse, β-oxydation, cycle
de l'acide citrique, phosphorylation oxydative).
Connaître les différentes modalités de transport bidirectionnel des
métabolites au travers de l'enveloppe mitochondriale (acides gras,
pyruvate, ATP, ADP et Pi).
Comprendre comment l'oxydation des métabolites, résultant dans la
production de NADH et FADH2, alimente la chaîne de transport des
électrons de la membrane interne et crée un gradient de protons.
Comprendre comment le gradient de protons dirige la production de
l'ATP par l'ATP synthase.
Connaître les fonctions mitochondriales autres que la production de
l'ATP : synthèse des stéroïdes, homéostasie du calcium et mort
programmée.
Temps de travail prévu : 3 heures
Sommaire :
Qu'est-ce qu'une mitochondrie ?
:: Origine
:: Organisation de la mitochondrie
:: Les fonctions de la mitochondrie
La production d'ATP
:: L'ATP comme fournisseur universel d'énergie
Approvisionnement en métabolites
:: Prise de nourriture
:: Création et utilisation des réserves énergétiques ; les rôles opposés du
couple glucagon/adrénaline et de l'insuline
Les activités métaboliques à l'origine de la production d'ATP
:: Glycolyse, β-oxydation et cycle de l'acide citrique
:: Phosphorylation oxydative liée à la chaîne de transport des électrons
Transport au travers de l'enveloppe mitochondriale
:: Introduction
:: Transport à travers la membrane externe
:: Transport à travers la membrane interne
Autres fonctions de la mitochondrie
:: Rôle de la mitochondrie dans la synthèse des hormones stéroïdes
:: Rôle des mitochondries dans l'homéostasie du Ca2+
:: Rôle de la mitochondrie dans la mort cellulaire programmée (apoptose)
Maladies liées aux mitochondries
:: Maladies liées aux mitochondries

Excursions
L'ADN mitochondrial
:: Un tout petit génome
:: Similitudes entre cytochrome c bactérien et mammalien
:: L'ADNmt et les maladies neuromusculaires invalidantes
:: Médecine légale
:: Le développement de l'embryon
La mitochondrie complice des assassins
:: L'arsenic
:: Le cyanure
:: Les complexes organophosphorés
Diabète sucré, dérégulation de l'approvisionnement de la mitochondrie
en métabolites
:: Glucagon, insuline et glycémie (homéostasie du glucose)
Insuline et Diabetes mellitus
:: La découverte de l'insuline
:: Insuline et glycémie (homéostasie)
:: Diabète sucré type I et II
:: Diabète Insipide
Qu'est-ce qu'une mitochondrie ?
Sommaire
Qu'est-ce qu'une mitochondrie ?
Origine
La mitochondrie naquit lorsque deux bactéries, archéobactérie anaérobie
(hôte) d'une part et protobactérie aérobie (symbionte) d'autre part,
fusionnèrent (il y a quelques milliards d'années) pour donner un eucaryote
primitif duquel tous les eucaryotes actuels dériveraient. Une telle hypothèse
sur l'origine de la mitochondrie a été suggérée par la mise en évidence, en
1963, de l'ADN mitochondrial (ADNmt de 16 kb chez les mammifères)
différent de l'ADN du noyau.

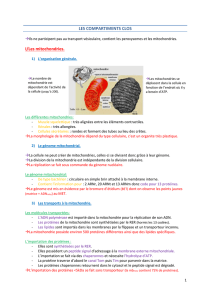
Figure 1. Les mitochondries
Le mot mitochondrie dérive du grec mitos, « filament », et chondros,
« graine » en raison de l'aspect de cet organite au microscope optique (et
électronique). Par exemple dans les cellules élaboratrices d'hormones
stéroïdiennes (corticosurrénales et gonades) les mitochondries sont
filamenteuses, alors que dans les hépatocytes (foie), elles sont granulaires.
Les mitochondries ont un diamètre d'environ . Les cellules en
contiennent de nombreuses : nombre estimé à 1000 dans un hépatocyte de rat.
Les mitochondries ne sont pas des organites statiques : elles se scindent ou,
au contraire, fusionnent couramment ce qui explique leur polymorphisme au
sein d'une même cellule (voir figure 1).
Sommaire
Qu'est-ce qu'une mitochondrie ?
Organisation de la mitochondrie
La mitochondrie est limitée par une enveloppe formée de deux membranes :
membrane externe et membrane interne (voir figure 2). Elles sont très

différentes dans leur composition et leurs fonctions. La membrane interne
délimite l'espace matriciel.
Figure 2. Le tube de jonction de crête
La membrane externe est perméable à toutes les molécules de 5 kDa ou
moins grâce à la présence de porines. Elle contient aussi des
translocases, transporteurs protéiques, impliquées dans l'import des
protéines (Translocase of the Outer Membrane, TOM).
La membrane interne se replie pour former de nombreuses crêtes
(cristae), ce qui a pour conséquence d'augmenter sa surface totale. Les
crêtes se présentent selon différentes formes : tubulaire, sacculaire,
laminaire et triangulaire, qui peuvent co-exister dans la même
mitochondrie et évoluer avec le temps. La base d'une crête est souvent
constituée par une structure tubulaire étroite appelée tube de jonction
de crête qui établit une communication entre l'espace intérieur de la
crête et l'espace inter membranaire périphérique de la mitochondrie
(voir figure2 ). La composition lipidique de la membrane interne est
particulière : elle contient une majorité de phosphatidylcholine et de
cardiolipine. Dans cette membrane on trouve la chaîne respiratoire de
transporteurs d'électrons, l'ATP synthase et de nombreux transporteurs
qui assurent le passage d'éléments tels que pyruvate, acide gras, ATP,
ADP et , composés nécessaires à la production d'ATP. La
membrane interne contient aussi des translocases (Translocase of the
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
1
/
48
100%