Situation de la batterie dans le circuit de charge et de recepteurs

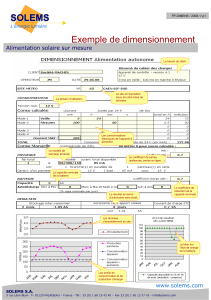
Annexe 1 : Situation de la batterie dans le circuit de charge et de récepteurs
Commentaire :
L’enseignant définira la masse (ligne équipotentielle).
L’enseignant pourra utiliser d’autre récepteur que la lampe.
Redresseur
Régulateur
G
M
BATTERIE
(Stocker)
ALTERNATEUR
(Transformer)
RECEPTEUR :
LAMPE
(Convertir)
(Google)

Annexe 2
PRODUCTION ET STOCKAGE D’UNE ENERGIE SUR
UN VEHICULE
Intervenants
temps
déroulement
Lieu et moyens
5min
Agro-équipement
physique
30 min
Physique
Eléves
20 min
Physique 20 min
Agro-équipement
5 min
Agro-équipement
10 min
20 min
Présentation de la séance
Introduction :
Présentation de schémas (Annexe 1)
Mise en forme de la chaîne
énergétique correspondante
(Annexe 2)
La batterie :
1/ La pile :
1-1/ Observations et fonctionnement
(Annexe 3)
1-2/ Branchement en série
Les différents binômes associeront
leurs piles en série. Possibilité de
mesurer I.
2/ Description de la batterie :
2-1/ Création d’une pile plomb
2-2/ Modèle éclaté (Annexe 4)
2-3/ Caractéristiques :
lecture d’étiquette
2-4/ Application :
Mesure U et I au niveau du
circuit d’éclairage
Calcul du temps de décharge
d’une batterie
Classe
Véhicule
Laboratoire chimie
Lames de cuivre et zinc
Acide sulfurique
c = 0,1 mol.L-1
Multimétre, fils conducteurs
Laboratoire chimie
Document à compléter
Acide sulfurique
c = 2 mol.L-1
2 plaques plomb
générateur 2 V ;100 mA
(environ 5 min)
Atelier
batterie
Véhicule + Multimètres
Calculatrice

20 min
15 min
10 min
5 min
2-5/Branchement en série et
dérivation (Annexe 5)
2-6/ Entretien , Mise en charge
L’enseignant demandera avec quel
liquide doit-on compléter le niveau de
la batterie et jusqu’à quelle hauteur ?
Sensibiliser les élèves sur l’intensité de
mise en charge (dégagement de H2
plus ou moins important)
2-7/ Sécurité
batteries
batterie
Physique
5 min
Agro-équipement
10 min
20 min
20 min
Physique
Agro-équipement
40 min
L’alternateur :
1/ Production d’une tension induite
2/ Modèle éclaté et fonctionnement
(Annexe 6)
3/ Transformation du courant
alternatif en courant continu et
régulateur
4/ Mesure de tension et d’intensité sur
un moteur au ralenti et sur un moteur
en accéléré
Application :
Calculs de :
- temps de charge de la batterie
au ralenti et en accéléré,
- puissances électriques fournies
par l’alternateur
- puissance mécanique
d’entraînement de l’alternateur
à partir du rendement
Laboratoire chimie
Bobines ,aimant,
galvanomètre
Schéma à compléter
Pinces ampéremètriques
Multimètres
Véhicule
Calculatrice
Formulaire

Annexe 3 : Expérience piles
Expérience 1: pile Cu-Zn: mise en évidence d'une tension
But: mettre en évidence la possibilité de fabriquer un générateur électrochimique
Électrolyte: H2SO4 0,1M Lames: Cu et Zn
Voltmètre
Observation: E = 0,8 V env
Commentaire : On peut mettre en évidence la circulation du courant avec une DEL ou un
Buzzer ou un Galvanomètre.
L’électrode de cuivre est une électrode inerte.
Expérience 2: Accumulateur Pb
But: mettre en évidence la réalisation d'un générateur électrochimique
Expérience 2,1: influence de l'état des plaques
But: montrer l'impossibilité d'obtenir un générateur avec 2 plaques
identiques
Électrolyte: H2SO4 2M Lames: Pb et Pb
Voltmètre
Observation: E = 0V

Expérience 2,2: électrolyse
Électrolyte: H2SO4 2M
Lames: Pb et Pb
Alimentation réglable Voltmètre
Ampèremètre
H2:
PbO2:
Observation: Passage courant
Si U > 2V, dégagement gazeux H2 sur plaque - (qui peut être éventuellement mis en
évidence)
Maintenir la charge qq min
Observer les plaques: plaque + : dépôt de PbO2 (brun)
Expérience 2,3
Mesure de la tension aux bornes de l'accumulateur
Observation: U = 2V
Commentaire : La surface des électrodes de plomb n’influe pas sur la valeur de la tension (on
peut immerger plus ou moins les plaques), mais influe sur la capacité.
On peut montrer le dégagement gazeux de l’hydrogène.
Les équations d’oxydo-réduction seront données par l’enseignant ainsi que les valeurs des
potentiels standards. Tout ceci sera développé plus tard dans le cours de chimie.
U
+
-
 6
6
 7
7
 8
8
1
/
8
100%