4 L`équation d`état d`un gaz parfait

Chaleur
10
Equation d’état des gaz parfaits
4 L’équation d’état d’un gaz parfait
Lorsqu’on élève la température d’un gaz, on ne constate pas
nécessairement une augmentation de son volume. Il peut y avoir
augmentation de sa pression. Dans le système décrit ci-contre, la
pression est maintenue constante. Il faudra évidemment négliger la
dilatation du récipient mais elle est vraiment insigniante au regard
de la dilatation du gaz. On constate que, comme dans le cas du solide,
le volume du gaz est sensiblement proportionnel au volume initial de
gaz et à l’élévation de température :
V V T
2 1 1= × +
( )
g D
γ est le coefcient de dilatation volumique du gaz étudié, à pression
constante. On observe que, à une température donnée, le coefcient
γ est le même pour tous les gaz. A la température de 0°C, il vaut
approximativement :
g = × - -
3 66 10 3 1
,K
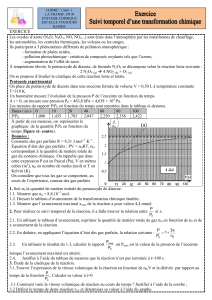
Le volume d’un échantillon de gaz en fonction de la
température.
Les différentes courbes correspondent à des gaz à
pression différentes.
Application
Trouver la relation entre g et la température du zéro
absolu.
4.1 La loi des gaz parfaits
Comme vous l’avez étudié au cours de chimie, on peut établir une relation expérimentale entre les
trois grandeurs P V et T :
PV
Tcte@
P est la pression en Pa
V le volume du gaz en m3
T la température de ce gaz en Kelvin
Aucun gaz n’est parfait, cependant, on peut considérer un gaz comme parfait si la pression à laquelle
il se trouve n’est pas trop grande et si sa température n’est pas trop basse. Il obéit alors à la relation
appelée loi des gaz parfaits :
PV
TnR=
n est le nombre de mol de gaz
R est la constante des gaz parfaits,
RJ
mol K
=×
8 31,
Cette équation est appelée équation d’état parce qu’elle établit une relation entre les variables
d’état du système. L’équation est valable seulement pour les états d’équilibre dans lesquels P, V et
T ont des valeurs bien dénies.

Chaleur
11
Equation d’état des gaz parfaits
Si l’une au l’autre des grandeurs p V ou T est constante on utilise les lois :
Nom de la loi Gay-Lussac
(≈1800)
Charles
(≈1800)
Boyle-Mariotte
(1662)
valeur constante p V T
loi
V
T
V
T
1
1
2
2
=
p
T
p
T
1
1
2
2
=
p V p V
1 1 2 2
=
nom du processus isobare isochore isotherme
Exemple
Calculer la masse de 60 cm3 d’oxygène à la pression de 80 cm de Hg et à la température de 20°C.
Exprimer les grandeurs dans les unités SI
p gh kg
m
m
sm Pa
Hg
= = × × × = ×r 13 6 10 9 81 0 8 1 067 10
3
3 2
5
, , , ,
V m= × -
60 10 6 3
T K= + =273 15 20 293 15, ,
Le nombre de mol
nPV
RT
Pa m
J
mol K K
mo= = × × ×
××
= ×
-
-
1 067 10 60 10
8 31 293 15
2 63 10
5 5 3
3
,
, ,
,ll
La masse moléculaire de l’oxygène est de 32, sa masse molaire est de
32 10 3
×-kg
mol
La masse du gaz est donc de
m nM mol kg mol kg= = × × × = ×
- - -
2 63 10 32 10 8 42 10
3 3 5
, ,

Chaleur
12
Equation d’état des gaz parfaits
4.2 Exercices
4.1 Montrez qu’à 0°C et 1 atm, la densité des molécules dans un gaz parfait est égale à
2 7 1019 3
, /×molécules cm
.
4.2 Écrivez la loi des gaz parfaits en fonction de la densité (mesurée en kg/m3) du gaz. À 0°C et
1 atm, déterminez la densité des gaz suivants : (a) azote ; (b) oxygène ; (c) hydrogène.
4.3 Un cylindre contient 1 kg d’oxygène à une pression de 3 atm. (a) Quelle serait la pression si
l’on remplaçait l’oxygène par 1 kg d’azote à la même température? (b) Quelle masse d’azote
produirait une pression de 2 atm à la même température ?
4.4 Deux moles d’hélium sont à 20°C et à une pression de 2000 hPa. (a) Trouvez le volume du gaz.
(b) Si l’on chauffe le gaz à 40°C et que l’on réduit sa pression de 30%, quel est son nouveau
volume ?
4.5 Un cube d’arête 10 cm est rempli d’oxygène à 0°C et 1 atm. La boîte est scellée et on élève sa
température à 30°C. Quelle est la force exercée par le gaz sur chaque paroi de la boîte ?
4.6 Un ballon à air chaud a un volume de 1200 m3. La température de l’air ambiant est égale à 15°C
et la pression à 1 atm. Quelle valeur doit atteindre la température de l’air dans le ballon pour
que celui-ci parvienne tout juste à soulever 200 kg? La masse molaire des molécules d’air est
de 29 g/mol.
1
/
3
100%