Epiderme de Tulipe Cellules chlorophylliennes d`Elodée

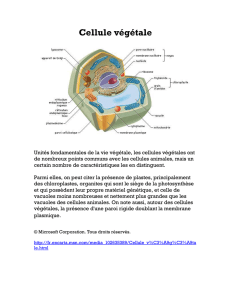
Epiderme de Tulipe
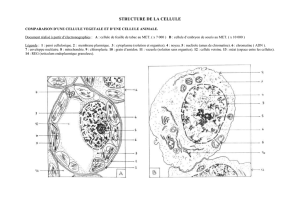
Cellules chlorophylliennes d’Elodée
N

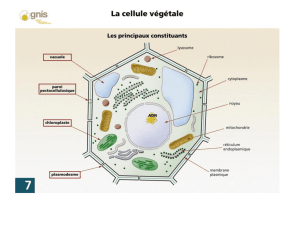
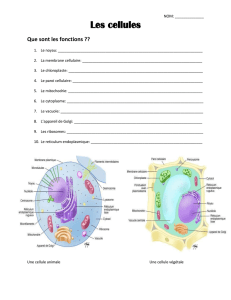
Un organite original : les vacuoles des plantes supérieures
1. Caractéristiques structurales et composition
1.1. Données de la microscopie : caractéristiques structurales
1.2. Données biochimiques : composition du suc vacuolaire
1.3. Données biochimiques : composition protéique du tonoplaste
2. La vacuole et l’équilibre hydrique des cellules végétales
2.1. L’équilibre hydrique des cellules végétales
2.2. Le contrôle de l’ouverture des stomates
3. Fonctions lytiques et de stockage
3.1. Deux populations de vacuoles dans une même cellule
3.2. Les fonctions de stockage
3.2.1. Accumulation des composés du métabolisme primaire
3.2.1. Accumulation des proténes de réserve dans les graines
3.2.1. Accumulation des composés du métabolisme secondaire
3.3. Les fonctions lytiques
3.4. L’adressage des protéines dans les vacuoles
4. Conclusion

Vacuole centrale
• Vacuole unique
•Volume important (jusqu’à
80-90% vol. cellulaire)
•Peu dense aux électrons
vacuus
= vide
•Organite limitée par une
membrane simple =
le tonoplaste
•Travées cytoplasmiques

Cellule méristématique d’apex racinaire

Différenciation de cellules du tapis de l’anthère
(Lin
et al
. 2001)
AB
C
AB
C
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
1
/
33
100%