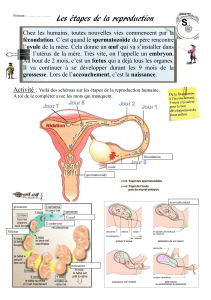
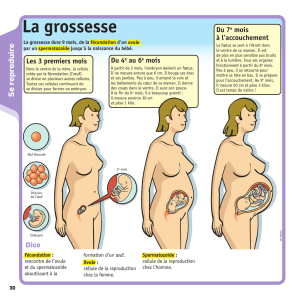
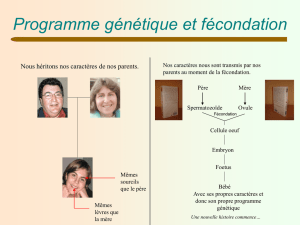
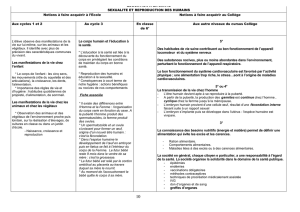
Embryologie de l'oursin: Biologie du développement

EMBRYOLOGIE!
PARTIE 2: BIOLOGIE DU DÉVELOPPEMENT DE L’OURSIN (C. GHIGLIONE)!
!
I - PRÉSENTATION DE L’OURSIN!
•L’Oursin est utilisé depuis très longtemps en recherche, notamment dans le but de
comprendre la reproduction."
•Pour comprendre ce qui se passe chez l’être humain, il faut se référer à des organismes
plus simples. L’Oursin a ainsi permis d’éclaircir comment nous nous reproduisons et
nous développons."
!
•Les Oursins sont des animaux à forme globulaire, recouverts par des piquants de
formes et de tailles variables. Généralement, l'Oursin est un animal de quelques
centimètres."
•La plupart des études nous intéressant ont été réalisées sur l'espèce méditerranéenne
Paracentrotus lividus (c’est une espèce comestible)."
1

•Les Oursins appartiennent au phylum des Échinodermes, comprenant 7000 espèces,
toutes marines. Le phylum des Échinodermes regroupe 5 classes:"
➤ Deutérostomes
•Les Échinodermes sont des deutérostomes, c’est à dire qu’au cours de leur
développement, l'anus se forme en premier à partir du blastopore, contrairement au
protostomes. "
2

•Donc d'un point de vue évolutif, les Échinodermes sont plus proches de nous que le
reste des Invertébrés."
•Caractéristiques des Deutérostomes:
-Développement de la région anale avant la région buccale"
-Segmentation holoblastique (= segmentation totale)"
-Segmentation radiaire: les plans de clivage sont soit parallèles, soit perpendiculaires
à l’axe primordial qui est l'axe animal-végétatif (A-V). "
-Capacité de régulation des blastomères."
!
➤ Oursin adulte
•Les Oursins adultes se retrouvent de manière générale sur des rochers."
•On oriente l’Oursin par rapport à la position de sa bouche:"
-La face orale est toujours face au support car l'Oursin est un animal brouteur."
-À l'opposé, la face aborale (= région ano-génitale) permet l’expulsion des gamètes et
des déchets."
•Entre les piquants, les Oursins possèdent des pieds ambulacraires, de longues
structures se terminant par des ventouses."
•Le squelette calcaire de l'Oursin est nommé test. On peut y observer une alternance de
bandes de différentes couleurs. C'est grâce à ce test calcaire que l'Oursin a une forme
globulaire."
•Les pieds ambulacraires ou podias permettent à l'Oursin de se déplacer lentement et
de monter sur la vitre des aquariums."
3

•On ne peut pas distinguer les mâles et les femelles à l'état adulte. Le seul moyen de
déterminer le sexe de l'Oursin est de voir les gamètes qu'il produit ou les gonades."
•Les pieds ambulacraires et les piquants s'organisent en rangées. Il y a alternance entre:"
-5 régions ambulacraires portant les pieds ambulacraire qui passent au niveau de
petits trous"
-5 régions interambulacraires, au niveau desquelles les piquants sont mis en place."
•Ces 2x5 régions de l’Oursin adulte témoignent de la symétrie pentaradiaire propre aux
Échinodermes. Il est beaucoup plus facile de repérer cette symétrie pentaradiaire au
niveau des Étoiles de mer."
•Au niveau de la bouche, on observe un très gros trou dans lequel travaille la lanterne
d’Aristote."
•Au niveau de la face aborale, quand on enlève tous les piquants, on voit la région ano-
génitale avec des petits trous servant à expulser les gamètes mâles ou femelles."
•Une dissection de la région orale permet de montrer la disposition de la lanterne
d'Aristote, appareil masticateur de l'Oursin adulte. "
•On y reconnaît les 5 dents calcaires alternées avec une pièce squelettique articulée
faisant office de pince: le compas. "
4

•Divers muscles assurent les mouvements des dents. "
•On remarquera la rigoureuse conservation de la symétrie pentaradiée."
!
➤ Avantages que présente l’Oursin pour l’étude du développement
animal
•L’Oursin est un organisme modèle pour comprendre le processus de développement
animal, plus particulièrement celui des Vertébrés. Les organismes modèles privilégiés
pour l’étude du développement des Invertébrés sont la drosophile et le nématode C.
elegans."
•L'embryon d'Oursin a permis de faire de grandes avancées dans la compréhension de
la fécondation et du développement précoce d'organismes plus évolués, notamment
les Mammifères et l’Homme."
•De nombreux avantages font de l’Oursin un organisme modèle pour l’étude du
développement animal:"
-Grand nombre de gamètes: "
‣Une femelle Oursin mise sur un bécher contenant de l'eau de mer et dont la ponte
est stimulée par injection de chlorure de potassium dans sa cavité peut produire à
elle seule jusqu'à 107 gamètes. "
‣Les Oursins mâles peuvent en produire jusqu'à 1012."
-Fécondation et développement externes: La fécondation se fait dans l’eau de mer.
On peut alors récupérer les gamètes et observer la fécondation et le développement
in vitro."
-Développement rapide et synchrone: "
‣L’œuf d’Oursin est oligolécithe, donc possède très peu de réserves vitellines. Le
développement ne peut donc pas durer dans le temps."
‣Un développement synchrone signifie que des œufs fécondés au même moment
passent les différents stades de développement au même moment."
-Génome de S. purpuratus séquencé: "
5
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
1
/
42
100%