20-021-A-10
Anatomie
et
physiologie
du
vestibule
C.
Chabbert
La
présente
revue
ambitionne
de
faire
un
point
sur
la
physiologie
du
vestibule.
L’idée
n’est
pas
de
repro-
duire
ici
les
différentes
présentations
déjà
disponibles
dans
de
nombreux
ouvrages
de
physiologie
ou
de
médecine
ou
sur
divers
sites
Internet,
mais
plutôt
d’apporter
un
regard
différent,
plus
mécanistique
et
moléculaire,
en
explorant
le
fonctionnement
du
vestibule
«
de
l’intérieur
».
Par
cette
approche,
nous
tenterons
de
décrire
les
principes
et
limites
physiques
qui
gouvernent
les
processus
de
mise
en
place
de
l’information
sensorielle
vestibulaire.
Nous
présenterons
également
plusieurs
approches
technologiques
originales
qu’il
a
été
nécessaire
de
développer
pour
appréhender
les
caractéristiques
morphofonctionnelles
des
organes
vestibulaires.
Cette
démarche
a
pour
objectif
de
susciter
l’intérêt,
mais
aussi
de
promouvoir
de
nouvelles
questions
et
projets
d’étude
sur
le
fonctionnement
de
cet
organe
original
qui
ne
cesse
d’étonner.
©
2015
Elsevier
Masson
SAS.
Tous
droits
réservés.
Mots-clés
:
Vestibule
;
Transduction
mécanoélectrique
;
Otoconies
;
Endolymphe
;
Synapses
en
ruban
Plan
■Vestibule
:
organe
complexe
aux
multiples
fonctions
1
■Cellules
ciliées
vestibulaires
et
transduction
mécanoélectrique
2
Processus
de
transduction
mécanoélectrique
2
Encodage
et
transmission
de
l’information
vestibulaire
3
■Endolymphe
comme
moteur
électrochimique
de
la
transduction
mécanoélectrique
et
notion
de
flux
endolymphatique
4
Composition
originale
de
l’endolymphe
vestibulaire
4
Flux
endolymphatique
:
mythe
ou
réalité
?
5
■Otoconies,
membrane
otoconiale
et
notion
de
masse
inertielle
5
Notion
de
masses
inertielles
5
Métabolisme
des
otoconies
5
■Synapses
afférentes
et
efférentes
6
Zone
de
transfert
et
de
codage
6
Zone
de
contrôle
6
Zone
de
plasticité
7
Zone
de
fragilité
7
■Conclusion
7
Vestibule
:
organe
complexe
aux
multiples
fonctions
Le
vestibule
est
une
merveille
d’évolution
et
de
miniaturisa-
tion
qui
rassemble
dans
le
volume
d’une
noisette,
un
détecteur
tridimensionnel
d’une
extrême
sensibilité
et
un
amplificateur
de
haute
fidélité
capables
d’informer
le
cerveau
en
temps
réel,
sur
les
moindres
accélérations
auxquelles
notre
tête
est
soumise.
Pour
atteindre
un
tel
degré
de
précision
et
d’efficacité,
l’oreille
s’est
dotée
au
cours
de
l’évolution,
de
systèmes
extrêmement
perfec-
tionnés,
mettant
en
jeu
des
mécanismes
moléculaires
hautement
spécialisés
(canaux
ioniques
membranaires
à
activation
méca-
nique,
par
le
voltage
ou
par
des
ligands,
rubans
synaptiques),
des
adaptations
biologiques
sans
équivalent
(masses
inertielles
des
macules,
synapses
en
calice)
et
utilisant
des
échanges
ioniques
entre
plusieurs
compartiments
distincts
(endolymphe,
milieu
intracellulaire,
périlymphe).
Différentes
zones
effectrices
(zones
mécanoréceptrices,
zones
sécrétoires,
zone
de
neurotransmission)
contribuent
de
concert
au
fonctionnement
de
cette
machinerie
unique
dans
le
système
nerveux [1].
Des
systèmes
de
rétrocontrôle
nerveux
(fibres
efférentes
cholinergiques
en
provenance
du
tronc
cérébral),
mais
également
endocrines
(expression
au
niveau
du
vestibule
de
récepteurs
à
l’adrénaline,
l’histamine,
la
sérotonine,
aux
estrogènes),
ont
également
été
développés
afin
d’assurer
un
réglage
fin
du
fonctionnement
du
vestibule
en
fonction
de
la
nature
de
notre
interaction
avec
l’environnement.
Au-delà
d’une
machine
ultraperfectionnée,
capable
de
repro-
duire
à
l’infini
et
de
manière
contrôlée
la
séquence
des
événements
unitaires
qui
supportent
le
principe
de
transduc-
tion
mécanoélectrique,
le
vestibule
dispose
de
propriétés
moins
connues,
mais
tout
aussi
surprenantes,
telles
qu’une
forte
pro-
pension
à
la
plasticité.
Cette
propriété
lui
permet
d’adapter
à
la
demande,
ses
capacités
de
neurotransmission,
mais
également
sous
certaines
conditions,
de
réparer
spontanément
son
réseau
neuronal
endommagé.
De
manière
étonnante,
ces
propriétés
plas-
tiques,
souvent
limitées
à
la
période
développementale
dans
beaucoup
de
tissus,
sont
préservées
dans
le
vestibule
des
mam-
mifères
adultes [2].
Le
vestibule
joue
enfin
un
rôle
de
senseur
de
notre
interaction
avec
l’environnement
et
assure
en
permanence,
via
la
voie
vestibulohypothamique,
un
contrôle
neuroendocrine
sur
divers
paramètres
biologiques,
tels
que
le
rythme
cardiaque,
la
température
corporelle,
ou
encore
le
métabolisme
osseux [3,
4].
Il
n’est
donc
pas
étonnant
qu’un
dispositif
aussi
précieux,
impliqué
à
la
fois
dans
le
maintien
de
la
posture
et
de
la
locomotion,
dans
l’orientation
du
corps
dans
l’espace
comme
dans
la
perception
corporelle,
soit
protégé
dans
un
«
coffre-fort
»
osseux
extrêmement
résistant,
l’os
temporal.
Pour
de
plus
amples
informations
sur
les
EMC
-
Oto-rhino-laryngologie 1
Volume
0
>
n◦0
>
xxx
2015
http://dx.doi.org/10.1016/S0246-0351(15)58501-2

20-021-A-10 Anatomie
et
physiologie
du
vestibule
différents
aspects
anatomiques
et
l’intégration
fonctionnelle
des
informations
vestibulaires,
le
lecteur
est
invité
à
se
référer
aux
excellentes
revues
récemment
publiées
sur
ce
thème [5–7].
Cellules
ciliées
vestibulaires
et
transduction
mécanoélectrique
La
cellule
ciliée
est
l’élément
de
base
de
la
transduction
méca-
noélectrique.
C’est
elle
qui
va
assurer
la
détection
des
moindres
déplacements
de
la
tête,
leur
encodage
en
informations
bioélec-
triques
et
la
transmission
de
l’information
sensorielle
vers
les
centres
supérieurs
via
le
nerf
vestibulaire.
Les
cellules
ciliées
sont
présentes
chez
tous
les
vertébrés,
depuis
les
poissons
jusqu’aux
mammifères.
Leur
forme
et
leur
fonction
de
mécanotransduc-
tion
ne
varient
globalement
que
très
peu
sur
toute
l’échelle
des
vertébrés.
Chez
l’homme,
134
000
cellules
ciliées
sont
disposées
de
manière
bilatérale,
en
cinq
épithélia
sensoriels
qui
assurent
chacun
des
fonctions
de
détections
complémentaires.
Les
crêtes
ampullaires
détectent
les
accélérations
angulaires,
tandis
que
les
macules
détectent
les
accélérations
linéaires.
La
disposition
et
l’orientation
de
chaque
cellule
ciliée
sur
les
différents
épithélia
sensoriels
ne
sont
pas
aléatoires.
Elles
répondent
au
contraire
à
un
programme
morphogénétique
précis
de
développement
qui
com-
mence
à
être
déchiffré
depuis
quelques
années [8].
Chaque
cellule
ciliée
est
séparée
de
ses
congénères
par
des
cellules
de
soutien
dont
la
fonction
dépasse
largement
le
simple
rôle
de
stabilisation
et
d’organisation
de
l’épithélium.
Ces
dernières
présentent
en
effet
à
leur
surface
de
petites
microvillosités
parfaitement
ordonnées
(Fig.
1)
qui
pourraient
contribuer
à
la
régulation
de
la
composi-
tion
ionique
de
l’endolymphe.
Dans
leur
partie
basolatérale,
les
cellules
de
soutien
expriment
des
protéines
membranaires
impli-
quées
dans
le
recyclage
du
glutamate
de
la
zone
synaptique [9].
Elles
pourraient
également
avoir
un
rôle
essentiel
dans
la
stabilisa-
tion
et
le
maintien
des
connexions
synaptiques
avec
les
neurones
du
ganglion
de
Scarpa,
via
la
libération
de
neurotrophines [10].
Dans
leur
partie
apicale,
les
cellules
ciliées
sont
équipées
d’une
véritable
antenne
de
réception
des
stimuli
mécaniques
:
la
touffe
ciliaire
(Fig.
1).
Composée
de
20
à
300
stéréocils
selon
les
espèces,
elle
est
capable,
grâce
à
sa
structure
sur
pivots,
de
ressentir
les
moindres
mouvements
et
accélérations
de
la
tête
et
d’enclencher
une
cascade
d’événements
qui
vont
conduire
à
un
changement
de
l’état
électrique
de
la
cellule
ciliée.
Les
stéréocils
sont
regroupés
de
manière
hexagonale.
Ils
varient
progressivement
en
longueur
sur
la
surface
de
la
cellule.
Ils
sont
composés
d’un
squelette
d’actine.
Un
seul
vrai
cil,
le
kinocil,
possédant
une
armature
de
microtu-
bule,
est
érigé
à
l’extrémité
la
plus
haute
de
la
touffe
ciliaire.
Il
joue
un
rôle
d’ancrage
de
la
touffe
ciliaire
à
la
membrane
otoconiale.
De
fins
filaments
d’actine
disposés
le
long
de
chaque
stéréocil
per-
mettent
de
les
maintenir
en
position
verticale
et
de
préserver
une
distance
d’environ
10
nm
avec
les
stéréocils
voisins.
Ce
dispositif
permet
de
rigidifier
la
touffe
ciliaire
et
de
la
rendre
plus
récep-
tive
aux
déplacements.
De
manière
remarquable,
les
stéréocils
ne
sont
pas
uniformes
(Fig.
1).
Leur
largeur
varie
selon
les
espèces,
de
100
à
900
nm
à
leur
apex
à
quelques
dizaines
de
nanomètres
à
leur
base.
Ce
rétrécissement
joue
un
rôle
de
pivot
autour
duquel
chaque
stéréocil
peut
bouger
librement [1].
Les
stéréocils,
grâce
à
leur
squelette
d’actine,
sont
ancrés
dans
la
plaque
cuticulaire.
Ce
socle
protéique
disposé
dans
la
partie
la
plus
haute
du
corps
cellulaire
et
composé
de
filaments
d’actine,
de
myosine
et
de
tro-
pomyosine
forme
les
fondations
de
cet
édifice.
Son
organisation
de
type
musculaire
pourrait
permettre,
selon
le
besoin,
d’adapter
la
rigidité
ou
la
position
de
la
touffe
ciliaire [11].
Processus
de
transduction
mécanoélectrique
Le
processus
de
transduction
mécanoélectrique
est
initié
par
la
mise
en
mouvement
de
la
touffe
ciliaire [13].
Le
glissement
des
sté-
réocils
adjacents
les
uns
par
rapport
aux
autres
exerce
une
traction
sur
de
fins
filaments
protéiques,
les
liens
apicaux,
situés
à
l’apex
de
chaque
stéréocil
et
reliés
directement
à
des
canaux
ioniques
membranaires
mécanosensibles
:
les
canaux
de
transduction [14].
L’ouverture
de
ces
canaux
ioniques
à
perméabilité
non
sélec-
tive
permet
l’entrée
massive
dans
le
cytoplasme
de
la
cellule
ciliée
d’ions
potassium
(K+)
et
calcium
(Ca2+)
en
provenance
de
l’endolymphe
qui
baigne
la
partie
apicale
des
cellules
ciliées
(Fig.
2).
Il
est
à
noter
qu’une
partie
des
canaux
de
transduc-
tion
(estimée
à
15
%)
reste
ouverte
au
repos [1].
Ainsi,
même
en
l’absence
de
mouvement,
les
cellules
vestibulaires
entretiennent
une
activité
de
repos
qui
maintient
une
décharge
électrique
de
base
dans
le
nerf
vestibulaire.
L’existence
de
cette
activité
de
repos
est
importante
si
l’on
considère
que
le
basculement
de
la
touffe
ciliaire
vers
les
cils
les
plus
grands
(appelé
sens
positif)
provoque
l’ouverture
de
la
totalité
des
canaux
de
transduction,
A
1
2
3
4
5
6
B
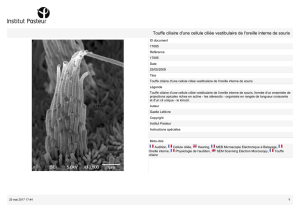
Figure
1.
La
touffe
ciliaire:
une
merveille
d’évolution
au
service
de
la
transduction
mécano-électrique.
A.
Photo
microscopie
électronique
à
balayage
de
la
surface
d’un
utricule
de
crapaud
buffle.
La
cohésion
des
stéréocils
et
leur
disposition
en
fonction
de
leur
taille
sont
particulièrement
visibles
sur
cette
photo.
Noter
également
le
rétrécissement
en
biseau
à
la
base
des
stéréocils
et
le
bulbe
du
kinocil
(en
haut
à
droite
de
la
touffe
ciliaire).
De
petites
microvillosités
parfaitement
alignées
sont
visibles
en
surface
des
cellules
de
soutien.
Échelle
2
m.
B.
Représentation
schématique
du
processus
d’adaptation
au
mouvement
de
la
touffe
ciliaire.
Le
déplacement
de
la
touffe
ciliaire
(1)
vers
les
stéréocils
(6)
les
plus
grands,
provoque
l’extension
des
liens
apicaux
(5)
et
l’ouverture
des
canaux
de
transduction
(2).
L’entrée
de
calcium
au
travers
de
ces
canaux
déclenche
localement
le
glissement
des
molécules
de
myosine
(3)
sur
les
filaments
d’actine
(4)
qui
forment
le
squelette
des
stéréocils.
Il
s’ensuit
un
déplacement
des
canaux
membranaires
au
sein
de
la
membrane
plasmique,
un
relâchement
des
liens
apicaux
et
une
refermeture
automatique
des
canaux
de
transduction.
Adapté
de [12].
2EMC
-
Oto-rhino-laryngologie

Anatomie
et
physiologie
du
vestibule 20-021-A-10
millivolts
-100
-60
-20
millivolts
-100
-60
-20
millivolts
-100
-60
-20
Voltage cellulaire
Décharge neurone
primaire
Mouvement de la cupule
ou des otoconies
Endolymphe
Périlymphe
Excitation Repos
Inhibition
K+K+
K+
K+K+
K+
K+
Ca2+
Figure
2.
Schéma
illustrant
le
principe
de
transduction
mécano-électrique.
L’ouverture
des
canaux
de
transduction
à
perméabilité
non
sélec-
tive
permet
l’entrée
massive
dans
le
cytoplasme
de
la
cellule
ciliée
d’ions
K+et
Ca2+ en
provenance
de
l’endolymphe
qui
baigne
la
partie
apicale
des
cellules
ciliées.
Le
déplacement
de
la
touffe
ciliaire
vers
les
cils
les
plus
grands
(gauche)
provoque
l’ouverture
de
la
totalité
des
canaux
de
transduc-
tion,
une
entrée
massive
de
K+dans
la
cellule,
une
augmentation
de
voltage
de
la
cellule
ciliée
et
une
activation
de
la
décharge
des
neurones
primaires.
Une
partie
des
canaux
de
transduction
ouverte
au
repos
(centre)
assure
une
activité
de
décharge
de
repos
dans
les
neurones
primaires.
Un
basculement
de
la
touffe
ciliaire
vers
les
cils
les
plus
petits
(droite)
provoque
la
fermeture
de
ces
canaux.
Selon
la
direction
de
l’accélération
rec¸ue
par
la
tête,
l’activité
de
repos
des
cellules
ciliées
est
ainsi
modulée
dans
le
sens
d’une
excitation
ou
une
inhibition.
tandis
qu’un
basculement
dans
le
sens
opposé
(sens
négatif)
pro-
voque
la
fermeture
de
ces
canaux
(Fig.
2).
Selon
la
direction
de
l’accélération
rec¸ue
par
la
tête,
l’activité
de
repos
des
cel-
lules
ciliées
sera
ainsi
modulée
dans
le
sens
d’une
excitation
ou
d’une
inhibition.
L’arrangement
varié
des
cellules
ciliées
sur
l’épithélium
sensoriel
permet
ainsi
à
tout
moment
et,
quelle
que
soit
l’orientation
du
mouvement
de
la
tête,
de
détecter,
encoder
et
transmettre
une
information
sensorielle
aux
centres
supérieurs.
Afin
de
pouvoir
répondre
à
des
stimulations
mécaniques
répé-
tées
et
rapprochées
dans
le
temps,
la
touffe
ciliaire
dispose
d’un
mécanisme
original
dit
«
d’adaptation
».
Ce
phénomène
assure
la
refermeture
automatique
des
canaux
de
transduction
à
l’image
d’une
porte
équipée
d’un
groom [12].
Ce
mécanisme
d’adaptation
est
basé
sur
l’interaction
de
molécules
de
myosine
présentes
à
l’intérieur
de
chaque
stéréocil [15] et
sur
lesquelles
sont
amarrées
les
protéines
membranaires
constituant
les
canaux
de
transduction.
L’ensemble
est
rattaché
aux
filaments
d’actine
qui
forment
le
sque-
lette
des
stéréocils
(Fig.
1).
L’entrée
de
Ca2+ depuis
l’endolymphe
permet
localement
le
glissement
des
molécules
de
myosine
le
long
des
filaments
d’actine.
Cette
opération
entraîne
le
glissement
des
canaux
de
transduction
le
long
des
stéréocils
et
leur
reposition-
nement
en
position
fermée
après
relâchement
de
la
traction
sur
les
liens
apicaux.
Ce
phénomène
d’adaptation
est
crucial
pour
réinitialiser
la
micromécanique
de
la
touffe
ciliaire
en
vue
des
stimulations
suivantes.
Encodage
et
transmission
de
l’information
vestibulaire
L’encodage
de
l’information
sensorielle
vestibulaire
consiste
à
conserver
lors
du
processus
de
transduction
mécanoélectrique,
les
différents
paramètres
des
déplacements
de
la
tête
(vitesse,
ampli-
tude,
durée).
Cette
opération
est
cruciale
afin
de
discriminer
entre
les
différents
types
d’accélérations
rec¸us.
La
mise
en
forme
de
l’information
sensorielle
débute
évidemment
à
l’apex
de
la
cellule
sensorielle,
au
niveau
de
la
touffe
ciliaire,
où
amplitude
et
durée
du
déplacement
déterminent
le
degré
d’ouverture
des
canaux
de
transduction,
la
quantité
d’influx
de
K+et,
par
conséquent,
le
degré
de
dépolarisation
de
la
cellule
ciliée.
L’encodage
se
pour-
suit
ensuite
dans
la
partie
basolatérale
de
la
cellule
sensorielle
où
sont
exprimés
différents
types
de
canaux
ioniques
membranaires
activés
par
le
voltage.
Le
flux
d’ions
K+entrés
via
la
touffe
ciliaire
envahit
progressivement
tout
le
corps
cellulaire
de
la
cellule
sen-
sorielle,
provoquant
un
changement
de
son
état
électrique.
Selon
le
degré
de
dépolarisation,
il
s’en
suit
une
ouverture
de
canaux
calciques
membranaires
activés
par
le
voltage
(type
L
sensibles
aux
dihydropyridines).
L’influx
d’ions
Ca2+,
déterminé
par
le
gra-
dient
électrochimique
local,
participe
ensuite
à
la
mobilisation
des
vésicules
synaptiques
et
au
relargage
du
glutamate
dans
la
fente
synaptique.
Cette
étape
est
déterminante
pour
le
transfert
de
l’information
sensorielle
vers
les
fibres
nerveuses
afférentes
des
neurones
vestibulaires
primaires
(neurones
du
ganglion
de
Scarpa).
Le
glutamate
libéré
par
chaque
vésicule
présynaptique
se
fixe
alors
sur
les
récepteurs
spécifiques
du
glutamate
exprimés
sur
la
membrane
des
terminaisons
nerveuses
afférentes.
La
fixation
du
glutamate
sur
ses
récepteurs
spécifiques
provoque
un
changement
de
conformation
de
ces
protéines
canaux
et
permet
l’entrée
mas-
sive
de
sodium
ou
de
calcium
selon
le
type
de
récepteur
considéré
(récepteurs
alpha-3-amino-OH-5-méthyl-4-isoxazole
propionique
[AMPA]
et
N-méthyl-D-aspartate
[NMDA]
respectivement)
dans
la
terminaison
nerveuse
afférente [16–19].
C’est
principalement
l’influx
de
Na+au
travers
des
récepteurs
AMPA
qui
est
à
l’origine
des
changements
transitoires
et
locaux
du
potentiel
de
membrane
appelés
potentiels
postsynaptiques
excitateurs
(PPSE).
Après
cheminement
et
sommation
au
niveau
du
premier
demi-nœud
de
Ranvier,
ces
PPSE
vont
contribuer
au
déclenchement
d’un
potentiel
d’action
qui
cheminera
ensuite
le
long
du
nerf
vestibulaire
vers
le
tronc
cérébral.
Il
est
à
noter
que
les
cellules
ciliées
disposent
d’un
système
original
de
libé-
ration
de
glutamate,
que
l’on
ne
retrouve
que
dans
les
cellules
sensorielles
(y
compris
les
photorécepteurs).
Ces
systèmes
appelés
«
rubans
présynaptiques
»
agissent
comme
des
tapis
roulants
per-
mettant
d’approvisionner
en
continu
les
synapses
vestibulaires
et
de
maintenir
un
rythme
de
libération
rapide
et
soutenu
du
neurotransmetteur [20,
21].
Afin
de
ne
pas
obstruer
les
récepteurs
du
glutamate
et
bloquer
le
processus
de
neurotransmission,
le
glutamate
se
décroche
ensuite
rapidement
des
récepteurs
et
est
évacué
de
la
«
zone
active
»
grâce
à
l’action
de
transporteurs
du
glutamate.
Ces
protéines
membra-
naires
exprimées
sur
la
membrane
des
cellules
de
soutien
fixent
le
glutamate
et
le
transbordent
vers
leur
cytoplasme.
Là,
il
est
EMC
-
Oto-rhino-laryngologie 3

20-021-A-10 Anatomie
et
physiologie
du
vestibule
transformé
en
glutamine,
puis
exporté
à
nouveau
vers
la
cellule
ciliée.
Cette
opération
constitue
ce
que
l’on
appelle
le
«
cycle
du
glutamate
».
Dans
le
cas
particulier
des
synapses
en
calice,
où
la
terminaison
nerveuse
s’étale
sur
la
totalité
de
la
membrane
baso-
latérale
de
la
cellule
ciliée,
l’action
des
transporteurs
du
glutamate
des
cellules
de
soutien
ne
peut
s’effectuer.
Dans
ce
cas
précis,
d’autres
types
de
transporteurs
du
glutamate
(EAAT4
et
EAAT5)
exprimés
à
la
fois
en
pré-
et
postsynapse
assurent
la
recapture
du
glutamate
directement
par
la
cellule
ciliée,
ou
encore
son
évacua-
tion
vers
la
terminaison
nerveuse [9].
En
parallèle
du
processus
de
neurotransmission,
la
dépolarisa-
tion
initiée
par
l’influx
de
K+en
provenance
de
l’endolymphe
active
des
canaux
K+membranaires
sensibles
au
voltage [22].
En
raison
du
gradient
électrochimique
local,
leur
ouverture
provoque
une
sortie
massive
de
K+depuis
le
cytoplasme
de
la
cellule
ciliée
vers
la
périlymphe
qui
l’entoure.
Cette
fuite
de
charges
électriques
positives
provoque
une
hyperpolarisation
progressive
de
la
cellule
ciliée
et
un
retour
à
son
potentiel
de
repos
(de
l’ordre
de
−80
mV
à
−90
mV
selon
le
type
cellulaire).
La
cellule
est
alors
prête
pour
réagir
à
la
prochaine
accélération.
Endolymphe
comme
moteur
électrochimique
de
la
transduction
mécanoélectrique
et
notion
de
flux
endolymphatique
L’endolymphe
baigne
la
touffe
ciliaire
des
cellules
sensorielles.
De
par
sa
composition
ionique
particulière
(riche
en
K+140
mM),
elle
constitue
le
moteur
électrochimique
de
la
transduction
méca-
noélectrique.
Comme
dans
l’ensemble
du
corps,
les
mouvements
ioniques
à
ce
niveau
sont
gouvernés
par
la
combinaison
d’un
gradient
électrique
et
d’un
gradient
chimique.
Le
gradient
élec-
trique
repose
sur
le
principe
que
deux
charges
électriques
de
signes
opposés
s’attirent,
tandis
que
deux
charges
de
mêmes
signes
se
repoussent.
Le
cytoplasme
de
la
cellule
ciliée
étant
chargé
négati-
vement
(potentiel
intracellulaire
de
l’ordre
de
–80
mV),
les
cations
situés
à
l’extérieur
de
la
cellule
(dans
l’endolymphe
comme
dans
la
périlymphe)
auront
ainsi
tendance
à
entrer
dans
la
cellule,
si
un
canal
ionique
membranaire,
assez
large
pour
les
laisser
passer,
s’ouvre.
Le
gradient
chimique
est
basé
sur
le
principe
de
diffusion
d’un
composé.
Ce
principe
implique
qu’un
ion
tend
à
diffuser
d’une
zone
où
il
est
très
concentré,
vers
une
zone
où
il
l’est
moins.
Les
ions
K+très
concentrés
dans
le
cytoplasme
de
la
cellule
auront
tendance
à
sortir
vers
la
périlymphe
où
ils
sont
bien
moins
repré-
sentés
(5
mM),
si
tant
est
qu’ils
en
aient
là
encore,
la
possibilité.
Au
niveau
des
différentes
zones
du
vestibule,
l’association
et
quelques
fois
l’opposition
de
ces
deux
gradients
régit
les
échanges
ioniques
entre
l’endolymphe
et
le
cytoplasme,
et
entre
le
cytoplasme
et
la
périlymphe
(Fig.
2).
Composition
originale
de
l’endolymphe
vestibulaire
La
composition
originale
de
l’endolymphe
vestibulaire
est
le
résultat
d’échanges
ioniques
qui
s’exercent
en
différentes
zones
du
vestibule [23].
Des
études
utilisant
des
électrodes
à
sélectivités
ioniques
ont
permis
de
démontrer
qu’une
sécrétion
massive
de
K+s’effectue
au
travers
de
canaux
potassiques
(KCNQ1/KCNE1)
exprimés
par
les
cellules
sombres
qui
bordent
les
crêtes
ampul-
laires
et
l’utricule
(Fig.
3).
La
dérégulation
pharmacologique
de
cette
sécrétion
ou
encore
l’altération
du
fonctionnement
de
ces
canaux
(cas
des
syndromes
de
Jervell
et
Lange-Nielsen
et
du
QT
court)
à
la
suite
de
mutations
génétiques
est
susceptible
de
per-
turber
considérablement
les
échanges
de
K+dans
l’endolymphe,
avec
la
conséquence
dans
certains
cas
de
provoquer
des
désordres
vestibulaires
importants [24–27].
L’expulsion
de
ce
même
K+du
compartiment
endolympha-
tique
vers
la
périlymphe
via
les
cellules
ciliées
contribue
au
cycle
du
K+dans
le
vestibule
(Fig.
3)[26].
Les
cellules
épithéliales
qui
forment
la
paroi
du
labyrinthe
membraneux
sont
également
une
zone
d’échange
ionique
importante.
Des
entrées
de
Cl–,
ainsi
que
des
sorties
de
Ca2+ et
de
Na+s’effectuent
à
ce
niveau.
De
même,
des
entrées
de
K+et
de
Na+s’effectuent
au
travers
des
cellules
transitionnelles
qui
bordent
les
épithélia
sensoriels [23].
Contrairement
aux
autres
épithélia
sensoriels
vestibulaires,
le
sac-
cule
ne
possède
pas
de
cellules
sombres.
Le
K+,
indispensable
à
la
transduction
mécanoélectrique
à
ce
niveau,
est
en
majeure
partie
acheminé
depuis
l’endolymphe
cochléaire
via
l’aqueduc
cochléo-
vestibulaire.
En
conditions
normales,
le
saccule
bénéficie
ainsi
du
K+sécrété
dans
l’endolymphe
au
travers
de
la
strie
vasculaire [26].
A
K+
K+
K+
CS
CC
CT
Cellules sombres
KCNQ1/
KCNE1
Cupule Endolymphe
Périlymphe
Cellules
épithéliales
B
Figure
3.
Métabolisme
et
dynamique
de
l’endolymphe.
A.
Photographie
en
microscopie
optique
d’un
vestibule
isolé
de
tortue
pseudemys
scripta
adulte.
Les
crêtes
ampullaires
et
une
partie
des
canaux
semi-
circulaires
emplis
d’endolymphe
sont
bien
visibles
sur
la
photographie.
À
cause
de
l’élasticité
du
vestibule
membraneux,
les
mouvements
liquidiens
de
l’endolymphe
lors
d’un
mouvement
de
la
tête
sont
très
limités.
B.
Schéma
illustrant
le
«
cycle
du
K+»
au
niveau
d’une
crête
ampullaire.
Le
K+sécrété
par
les
cellules
sombres
via
les
canaux
KCNQ1/KCNE1
est
expulsé
depuis
l’endolymphe
vers
la
périlymphe
au
travers
des
cellules
ciliées
(CC).
CS
:
cellules
de
soutien
;
CT
:
cellules
transitionnelles.
4EMC
-
Oto-rhino-laryngologie

Anatomie
et
physiologie
du
vestibule 20-021-A-10
Flux
endolymphatique
:
mythe
ou
réalité
?
On
a
longtemps
pensé
que
la
sécrétion
ionique
au
niveau
de
la
strie
vasculaire
s’accompagnait
de
la
génération
d’un
cou-
rant
liquidien
ou
«
flux
longitudinal
»,
prenant
naissance
dans
la
cochlée
et
se
propageant
vers
le
sac
endolymphatique,
après
circulation
dans
les
différents
compartiments
du
vestibule.
De
récents
travaux
réalisés
par
l’équipe
d’Alec
Salt
de
l’Université
de
Washington
à
Saint
Louis
(États-Unis)
viennent
d’infirmer
ce
postulat.
En
injectant
au
moyen
de
micropipettes
de
verre
des
marqueurs
chimiques
à
différents
niveaux
du
comparti-
ment
endolymphatique
et
en
utilisant
des
électrodes
à
sélectivité
ionique,
cette
équipe
a
pu
suivre
les
déplacements
de
ces
molécules
au
cours
du
temps
selon
leur
zone
d’injection [28,
29]
(voir
aussi
http://oto2.wustl.edu/cochlea/res1.htm).
Leurs
résul-
tats
démontrent
clairement
que
les
déplacements
de
liquide
dans
l’endolymphe
sont
infimes,
voire
inexistants.
En
absence
de
flux
endolymphatique,
la
répartition
ionique
de
l’endolymphe
est
donc
régie
d’une
part
par
la
simple
loi
de
diffusion
des
molécules
en
milieux
liquidiens,
et
d’autre
part
par
les
échanges
ioniques
qui
s’exercent
à
différents
endroits
du
vestibule.
Ces
travaux
sont
par-
ticulièrement
précieux
pour
appréhender
la
cinétique
de
diffusion
des
composés
administrés
par
voie
générale
ou
de
manière
locale,
et
pour
relier
leurs
effets
thérapeutiques
à
leur
action
effective
sur
les
organes
concernés.
Étant
donné
que
les
mouvements
liquidiens
de
l’endolymphe
sont
limités,
ou
pour
le
moins
extrêmement
lents,
on
peut
se
demander
comment
s’effectue
le
déplacement
des
touffes
ciliaires
au
cours
d’un
mouvement
de
la
tête.
Ce
point
est
illustré
dans
le
paragraphe
suivant.
Otoconies,
membrane
otoconiale
et
notion
de
masse
inertielle
Notion
de
masses
inertielles
Contrairement
à
l’anémone
de
mer
dont
les
tentacules
sont
mis
en
mouvement
par
les
flux
et
reflux
de
la
mer,
les
touffes
ciliaires
des
cellules
sensorielles
vestibulaires
ne
sont
pratique-
ment
pas
sensibles
aux
mouvements
liquidiens
de
l’endolymphe.
Ceci
pour
la
simple
raison
que
ces
mouvements
sont
extrême-
ment
limités,
même
lors
de
mouvements
violents
de
la
tête.
Pour
transmettre
efficacement
les
mouvements
de
la
tête
aux
touffes
ciliaires,
le
vestibule
s’est
doté
de
masses
inertielles
qui
amplifient
le
mouvement
subi.
Leur
déplacement
provoque
le
basculement
de
la
touffe
ciliaire
et
le
cisaillement
des
cils
néces-
saire
à
l’ouverture
des
canaux
de
transduction
et
à
l’initiation
de
la
transduction
mécanoélectrique.
Les
masses
inertielles
jouent
donc
un
rôle
amplificateur
de
mouvement.
Au
niveau
des
crêtes
ampullaires,
les
masses
inertielles
sont
appelées
cupules.
Elles
sont
constituées
d’une
masse
gélatineuse
dans
laquelle
sont
insérés
les
kinocils
des
touffes
ciliaires.
Au
niveau
des
macules,
les
masses
inertielles
sont
constituées
d’amas
de
cristaux
de
carbonates
de
calcium
appelés
«
otoconies
»
disposés
sur
une
structure
protéique
en
forme
de
filet,
«
la
membrane
otoconiale
».
La
membrane
oto-
coniale
repose
à
la
surface
des
épithélia
sensoriels
et
les
kinocils
des
touffes
ciliaires
y
sont
amarrés
(Fig.
4).
L’action
de
ces
masses
iner-
tielles
dans
l’élaboration
de
l’information
sensorielle
vestibulaire
est
essentielle.
On
a
pu
constater
sur
des
modèles
de
souris
géné-
tiquement
modifiées
que
l’absence
d’otoconies
suffit
à
elle
seule
à
abolir
totalement
le
processus
de
transduction
mécanoélectrique,
même
si
les
différents
acteurs
de
la
transduction
mécanoélectrique
(endolymphe,
cellules
ciliées,
contacts
synaptiques,
neurones
pri-
maires)
restent
parfaitement
fonctionnels [30].
Métabolisme
des
otoconies
À
l’image
des
perles
de
culture
qui
naissent
à
partir
d’un
grain
de
sable
au
cœur
d’une
huître,
les
otoconies
présentes
au
creux
de
notre
vestibule
sont
produites
dans
l’endolymphe
maculaire
par
des
concrétions
de
carbonate
de
calcium
autour
de
l’otoconine [31].
Cette
protéine
est
sécrétée
par
les
cellules
transitionnelles
qui
bordent
l’épithélium
sensoriel [32].
Cette
opération
est
favorisée
par
la
concentration
en
calcium
et
le
pH
particulier
à
cette
zone
qui
résultent
de
l’action
combinée
des
canaux
TRPV5/TRPV6
et
de
la
pendrine
respectivement [33].
Une
fois
formées,
les
otoconies
se
déposent
sur
la
membrane
otoconiale
où
elles
sont
prises
dans
le
gel
otoconial.
Ce
gel
se
comporte
ainsi
comme
une
colle
qui
assure
leur
maintien
en
position
sur
les
épithélia
sensoriels
des
macules [33,
34].
On
peut
ici
se
demander,
au
regard
de
la
théorie
des
cupulolithiases,
si
les
otoconies
sont
réellement
en
mesure
de
se
détacher
de
la
surface
des
macules
en
conditions
normales,
ou
si
des
conditions
pathologiques
particulières,
affectant
par
exemple
la
qualité
du
gel
otoconial
ou
modifiant
la
structure
des
otoco-
nies
peuvent
favoriser
un
tel
phénomène.
À
ce
sujet,
plusieurs
études
réalisées
sur
modèles
animaux
ont
montré
que
des
alté-
rations
métaboliques,
telles
que
la
suppression
de
la
sécrétion
d’œstrogènes [35] ou
l’altération
génétique
de
la
production
de
pendrine [33] étaient
susceptibles
de
déréguler
le
métabolisme
des
otoconies.
Dans
ces
différentes
conditions,
des
otoconies
géantes
étaient
observées
au
centre
des
macules.
De
telles
altérations
du
A
CC
CS
CT
CM
Ca2+
Ca2+
Ca2+
Ca2+
Pendrine
Otoconies
Endolymphe
Membrane
otoconiale
Gel otoconial
Otoconine
HCO3-
TRPV5/ TRPV6
B
Figure
4.
Les
otoconies
et
leur
métabolisme.
A.
Photo
microscopie
électronique
à
balayage
d’otoconies
de
cochon
d’inde.
Échelle
10
m
(cliché
A.
Sans
avec
permission).
B.
Représentation
schématique
du
microenvironnement
nécessaire
à
la
formation
des
otoconies.
CC
:
cellules
ciliées
;
CS
:
cellules
de
soutien
;
CT
:
cellules
transitionnelles
;
CM
:
cellules
épithéliales
du
mur.
EMC
-
Oto-rhino-laryngologie 5
 6
6
 7
7
 8
8
 9
9
1
/
9
100%