Glycogénoses musculaires

JOURNÉES DES FAMILLES 2013
Maltase acide
(Lysosome)
Glucose
UDPG PLD
Glycogène
Glucose-1-P
Glucose-6-P
Fructose-6-P
Fructose 1,6-P
Glyceraldéhyde-3-P
3-P-Glycéroyl Phosphate
3-Phosphoglycérate
2-Phosphoglycérate
Phosphoenol Pyruvate
Pyruvate
Lactate
ATP
ADP
2ADP
2ATP
2 ADP
2 ATP
II Maladie de Pompe
(déficit en maltase acide)
V Maladie de McArdle
(déficit en phosphorylase musculaire)
IV
n
dersen
b
ranchante) III Maladie de Cori-Forbes
(déficit en enzyme débranchante)
VII Maladie de Tarui
(déficit en phosphofructokinase musculaire)
IX (déficit en phosphoglycérate kinase)
X Maladie de Di Mauro
(déficit en phosphoglycérate mutase)
XI (déficit en lactate déshydrogénase)
XIV
(déficit en phosphoglucomutase)
Fa i t s m a rq ua n t s
glycogenose-musculaire.afm-telethon.fr
> Les glycogénoses sont dues à un défaut de transformation des sucres
entraînant une accumulation toxique de glycogène dans les cellules.
Elles résultent d’un défi cit ou d’une absence de certaines enzymes intervenant
dans la transformation des sucres que nous mangeons, en énergie utilisable
par les cellules de notre corps. Ce sont des maladies du métabolisme du
glycogène.
> En octobre 2012, l'Association Francophone
des Glycogénoses (AFG) a organisé une journée
d'information sur la maladie de Pompe.
> La 2e Journée des Thérapeutiques Genzyme®
pour les Myopathies a eu lieu le 26 novembre 2012
à Grenoble.
> La 4e Journée française de la maladie de
Pompe s’est déroulée à l’Institut de Myologie (Paris)
le 31 janvier 2013.
> Maladie de Pompe ou glycogénose de type II
L’analyse de l’activité enzymatique sur tâche de
sang séché s’avère être une méthode de diagnostic
rapide et fi able.
> Maladie de Cori-Forbes ou glycogénose
de type III
• Une étude de suivi prospectif chez 30 personnes
atteintes de glycogénose de type III est en cours de
recrutement à l’Institut de Myologie (Paris).
• Une étude réalisée chez six personnes atteintes
de glycogénose de type III met en évidence une
intolérance à l’exercice liée à une hypoglycémie.
> Maladie de McArdle ou glycogénose
de type V
Un nouveau modèle de souris plus pertinent a été
développé.
Glycogénoses musculaires
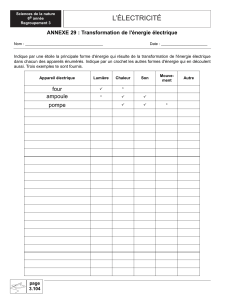
Métabolisme du glycogène.
Selon les besoins de l’organisme
et sous l’action de nombreuses
enzymes:
• Le glycogène (forme de stockage
du sucre) est formé à partir de
sucres fournis par l’alimentation
(glucose essentiellement) :
glycogénèse.
• Le glycogène est transformé en
glucose (forme utilisable du sucre)
pour fournir l’énergie aux cellules
au fur et à mesure de leurs besoins
énergétiques : glycogénolyse.

JOURNÉES DES FAMILLES 2013
Fa i t s m a rq ua n t s
glycogenose-musculaire.afm-telethon.fr
La maladie de Pompe est due au défi cit de l'enzyme α-glucosidase acide
(ou maltase acide).
maladie de pompe
> Enzymothérapie substitutive et autres pistes thérapeutiques
> Enzymothérapie substitutive et autres pistes thérapeutiques
> Une étude rétrospective a évalué le devenir
des 11 enfants traités par enzymothérapie à long terme
(sur 10 ans).
> Deux études ont confi rmé l’intérêt du Myozyme®
sur la force musculaire et la ventilation chez
l’adulte, même s'il s'agit d'une effi cacité limitée.
> Des résultats préliminaires encourageants
de l’essai de phase I/II du BMN-701 chez 30
personnes atteintes de forme tardive de la maladie
de Pompe ont été communiqués par Biomarin
Pharmaceutical.
> Mise au point d'une enzyme recombinante
nouvelle génération plus effi cace sur les modèles
cellulaires et animaux.
> Les résultats préliminaires de l’essai
de phase I/II de l’AT 2200 chez 23 personnes
atteintes de maladie de Pompe, annoncés par Amicus
Therapeutics, montre une bonne tolérance.
> Bonne tolérance de la thérapie génique
réalisée chez 5 enfants atteints de maladie de Pompe
sous ventilation assistée.
> Une nouvelle molécule candidate dans le
traitement de la maladie de Pompe : le facteur
de transcription EB testé dans des souris modèles.
Enzymothérapie substitutive
> Traitement visant à remplacer l’enzyme α-glucosidase acide, défi citaire dans la maladie de Pompe,
par une enzyme recombinante humaine, l'alglucosidase α (Myozyme®, laboratoire Genzyme).
> Myozyme® est un médicament à prescription restreinte classé dans la catégorie "médicaments
réservés à l'usage hospitalier".
> La Commission de Transparence de la Haute Autorité de Santé (HAS) reconnaît au Myozyme®
une amélioration du service médical rendu "importante" dans la forme infantile, en 2006, et une
amélioration du service médical rendu "modérée" dans la forme tardive, en 2010.
> En janvier 2013, au vu des résultats de l'utilisation du Myozyme® chez l'adulte, la HAS confi rme le
progrès thérapeutique mineur dans la forme tardive de la maladie de Pompe du fait de son effi cacité
limitée chez l'adulte.
Améliorer l’effi cacité de l’enzymothérapie substitutive
> BMN-701 : forme recombinante de l'alpha-glucosidase acide humaine associée à une molécule,
l'IGF2, qui améliore la pénétration de l'alpha-glucosidase recombinante dans les lysosomes des
cellules musculaires.
> Enzyme recombinante de nouvelle génération : nouvelle méthode de fabrication de l'alpha-
glucosidase recombinante, qui pénètre mieux jusqu’aux lysosomes.
> AT 2200 : protéine chaperonne qui stabilise et augmente l'activité de l'alpha-glucosidase
recombinante.
Thérapie génique
> La thérapie génique consiste à remplacer le gène GAA anormal pour rétablir l’expression d’une
protéine GAA fonctionnelle.
1
/
2
100%