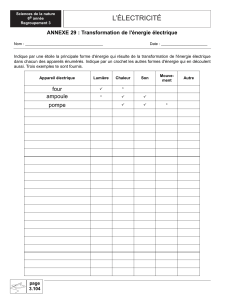
Glycogénoses musculaires

JOURNÉES DES FAMILLES 2015
Maltase acide
(Lysosome)
Glucose
UDPG PLD
Glycogène
Glucose-1-P
Glucose-6-P
Fructose-6-P
Fructose 1,6-P
Glyceraldéhyde-3-P
3-P-Glycéroyl Phosphate
3-Phosphoglycérate
2-Phosphoglycérate
Phosphoenol Pyruvate
Pyruvate
Lactate
ATP
ADP
2ADP
2ATP
2 ADP
2 ATP
II Maladie de Pompe
(déficit en maltase acide)
V Maladie de McArdle
(déficit en phosphorylase musculaire)
IV
n
dersen
b
ranchante)
III Maladie de Cori-Forbes
(déficit en enzyme débranchante)
VII Maladie de Tarui
(déficit en phosphofructokinase musculaire)
IX
(déficit en phosphoglycérate kinase)
X Maladie de Di Mauro
(déficit en phosphoglycérate mutase)
XI
(déficit en lactate déshydrogénase)
XIV
(déficit en phosphoglucomutase)
Fa i t s m a rq ua n t s
> Les glycogénoses sont dues à un défaut de transformation des sucres
entraînant une accumulation toxique de glycogène dans les cellules.
Elles résultent d’un défi cit ou d’une absence de certaines enzymes intervenant
dans la transformation des sucres que nous mangeons, en énergie utilisable
par les cellules de notre corps. Ce sont des maladies du métabolisme du
glycogène.
> Plusieurs évènements médico-scientifi ques ont eu lieu :
• les 12es Journées de la Société Française de Myologie sur
les avancées dans les maladies métaboliques (20-21
novembre 2014) ;
• une journée scientifi que dédiée aux glycogénoses de type III
(Cori) et de type V (McArdle) (28 février 2015) ;
• deux ateliers, organisés par l'European Neuromuscular
Center sur la maladie de Pompe (26-28 septembre 2014) et sur
la maladie de McArdle (17-19 avril 2015).
> Maladie de Pompe
• Une base de données internationale et une base de données
française.
• Une étroite surveillance des personnes asymptomatiques serait
suffi sante tant que leur état ne se dégrade pas.
• Une enquête réalisée sur 10 ans a évalué l’impact de la maladie
sur la vie quotidienne de 408 personnes.
• Les méthodes de diagnostic ont évolué en 10 ans.
> Maladie de Cori-Forbes ou glycogénose de type III
• Une base de données française.
• Une étude de suivi de personnes atteintes de la maladie en
France.
• Effi cacité de régimes alimentaires sur les symptômes cardiaques
et/ou musculaires.
• Une atteinte cognitive a été mise en évidence chez certains
patients.
> Maladie de McArdle ou glycogénose de type V
• Une base de données internationale (dont la France)
• Le grip-test comme méthode diagnostique fi able et peu
coûteuse.
• Le valproate de sodium pour augmenter l’expression de la
phosphorylase dans des modèles cellulaires et animaux.
> Myopathies à polyglucosans
• Un essai du triheptanoïne est en cours chez 18 personnes
atteintes de myopathie à polyglucosans.
Glycogénoses musculaires
Métabolisme du glycogène.
Selon les besoins de l’organisme
et sous l’action de nombreuses
enzymes:
• Le glycogène (forme de stockage
du sucre) est formé à partir de
sucres fournis par l’alimentation
(glucose essentiellement) :
glycogénèse.
• Le glycogène est transformé en
glucose (forme utilisable du sucre)
pour fournir l’énergie aux cellules
au fur et à mesure de leurs besoins
énergétiques : glycogénolyse.

JOURNÉES DES FAMILLES 2015
Fa i t s m a rq ua n t s
La maladie de Pompe est due au défi cit de l'enzyme α-glucosidase acide
(ou maltase acide).
maladie de pompe
> Enzymothérapie substitutive et autres pistes thérapeutiques
> Enzymothérapie substitutive et autres pistes thérapeutiques
> Un essai international (dont la France) de phase III du
BMN-701 chez 50 personnes atteintes de maladie de Pompe
déjà traitées par Myozyme® est en cours de recrutement.
> Un essai de phase II du BMN-701 pour évaluer la force
musculaire respiratoire chez 15 personnes atteintes de maladie
de Pompe est en cours de recrutement au Royaume-Uni.
> Un essai international (dont la France) de phase II/III
de la neo-GAA chez 21 personnes atteintes de maladie de
Pompe est en cours de recrutement.
> La société Amicus Therapeutics qui a développé l’AT-2220,
travaille sur une nouvelle enzyme recombinante, l’AT-B200.
> Un essai de phase IV du salbutamol chez 20 personnes
atteintes de maladie de Pompe déjà traitées par Myozyme®
est en cours de recrutement à Taïwan.
> Un essai de phase I/II de salbutamol pour améliorer la
fonction motrice chez 20 personnes atteintes de maladie de
Pompe déjà traitées par Myozyme® est en cours de recrutement
aux États-Unis.
> Un essai de phase I/II du clenbutérol pour améliorer la
fonction motrice chez 20 personnes atteintes de maladie de
Pompe déjà traitées par Myozyme® est en cours de recrutement
aux États-Unis.
> Un essai de thérapie génique chez 10 personnes atteintes
de maladie de Pompe est en cours aux États-Unis.
Enzymothérapie substitutive
> Traitement visant à remplacer l’enzyme α-glucosidase acide, qui manque dans la maladie de Pompe,
par une enzyme recombinante humaine, l'alglucosidase α (Myozyme®, laboratoire Genzyme).
> La Commission de Transparence de la Haute Autorité de Santé (HAS) reconnait au Myozyme® :
- En 2006 : amélioration du service médical rendu "importante" dans la forme infantile,
- En 2010 : amélioration du service médical rendu "modérée" dans la forme tardive,
- En 2013 : progrès thérapeutique mineur dans la forme tardive de la maladie de Pompe du fait de
son efficacité limitée chez l'adulte.
Améliorer l’effi cacité de l’enzymothérapie substitutive
> BMN-701 : enzyme recombinante associée à une molécule, l'IGF2 -> Améliorer la pénétration
dans les cellules musculaires.
> Neo-GAA ou AT-B200 : enzyme recombinante enrichie -> Mieux cibler les muscles.
> AT 2200 : protéine chaperonne -> Stabiliser et améliorer l'activité de l’enzyme recombinante.
Associer un traitement à l’enzymothérapie substitutive
> Salbutamol ou Clenbutérol : font grossir les muscles -> Améliorer la fonction motrice.
Thérapie génique
> Remplacer le gène
GAA
anormal -> Rétablir l’expression d’une protéine GAA fonctionnelle.
1
/
2
100%