ne première à l’ASCO cette année : l’élaboration de

U
ne première à l’ASCO cette année : l’élaboration de
sessions consacrées exclusivement aux nouvelles
approches, tous organes confondus. L’émergence
rapide de nouvelles molécules, de nouvelles stratégies ciblées, de
nouvelles approches biologiques, dont le développement est accé-
léré du fait de leur efficacité et de leur faible toxicité, a incité les
organisateurs à mettre en place des sessions intitulées “Théra-
peutiques en développement”. La Lettre du Cancérologue avait
prévu cette évolution avant l’ASCO en choisissant de consacrer
une section aux nouvelles approches il y a déjà quelques années…
Trois catégories de nouvelles approches ont été présentées durant
le congrès : nouveaux traitements cytotoxiques, immunothérapie
et nouvelles cibles moléculaires.
NOUVEAUX TRAITEMENTS CYTOTOXIQUES
Les nouvelles molécules ciblant l’Epidermal Growth Factor Recep-
tor (EGFR) et le Vascular Endothelial Growth Factor ( V E G F )
sont maintenant utilisées en association.
Pour chaque type de cible moléculaire, on dispose d’anticorps ou
d’inhibiteurs de tyrosine kinase (TK) associés aux récepteurs. Le
tableau I fait une synthèse des molécules anti-VEGF et anti-EGFR
ayant actuellement un développement avancé dans les tumeurs
solides. Habituellement, les anticorps ont une DCI se terminant
en “ab” et les inhibiteurs de TK une DCI se terminant en “ib”.
Ces divers types de molécules ont des propriétés différentes. Les
anticorps monoclonaux ont les particularités suivantes :
leur forte spécificité envers la cible,
leur cible est extracellulaire,
l’interaction avec la cible provoque un arrêt du cycle et l’apoptose,
leur administration est intraveineuse,
la fixation de l’anticorps sur la cible entraîne l’internalisation
du récepteur,
leurs effets indésirables les plus courants sont : rash, eczéma,
réactions d’hypersensibilité.
En revanche, les petites molécules inhibitrices de TK ont comme
propriétés :
une affinité pour la cible, mais aussi pour d’autres TK d’autres
récepteurs,
leur cible est intracellulaire,
leur administration est orale,
leur toxicité limitante est la diarrhée,
leur action est réversible,
les effets indésirables sont l’acné et la diarrhée.
Le bévacizumab est un anticorps monoclonal recombinant huma-
nisé anti-VEGF, et l’erlotinib HCl est un inhibiteur réversible et
sélectif de la TK d’HER1/EGFR.
L’association de ces deux drogues, qui ont montré leur efficacité
en monothérapie dans différents types tumoraux, a pour principe :
leur effet additif en préclinique ;
le faible taux de toxicité de chaque drogue, permettant leur asso-
ciation, d’autant que les toxicités ne sont pas croisées ;
l’hétérogénéité tumorale nécessitant une action sur des cibles
différentes.
Les données biologiques suggèrent par ailleurs des interactions
étroites entre les cellules tumorales et les cellules endothéliales
médiées par l’EGFR, le VEGF et le VEGFR (présence d’EGFR
sur les cellules endothéliales ; les anti-EGFR inhibent l’angio-
genèse sur les modèles précliniques et induisent l’apoptose des
cellules endothéliales ; présence de VEGFR sur les cellules tumo-
rales ; sécrétion autocrine et exocrine d’EGF et de VEGF par les
cellules tumorales).
Cette association a été testée dans le cancer du rein (voir chapitre
Tumeurs urologiques, p. 119) le cancer bronchique et le cancer
du sein.
Dans l’abstract 2000, présenté par A.B. Sandler et al., il s’agit
d’une étude de phase I/II évaluant l’anticorps anti-VEGF (béva-
cizumab, Avastin
™
) en association à l’erlotinib (Tarceva
®
) chez
les patients atteints de cancer bronchique non à petites cellules
(CBNPC), localement avancé ou en rechute. Les patients avaient
tous reçu au moins une première ligne de chimiothérapie.
La phase I a permis d’établir la dose d’erlotinib à 150 mg/j p.o. et
celle de bévacizumab à 15 mg/kg i.v. tous les 21 jours, en l’absence,
cependant, de dose limitante toxique.
Nouvelles approches
M. Saghatchian-d’Assignies*
145
La Lettre du Cancérologue - Volume XIII - n
o
3 - mai-juin 2004
* Institut Gustave-Roussy, Villejuif.
N
O U V E L L E S A P P R O C H E S
Tableau I. Molécules anti-EGFR et anti-VEGF : les “ab” et les “ib”.
Molécule Cible
Anticorps monoclonaux (ab) i.v.
– Trastuzumab HER2/neu (ErbB-2)
– Bévacizumab VEGF
– Cetuximab EGFR (ErbB-1)
Inhibiteurs de TK (ib) (petites molécules p.o.)
– Imatinib Bcr-Abl, KIT, PDGFR
– Gefitinib EGFR (ErbB-1)
– Erlotinib EGFR (ErbB-1)

Quarante-quatre patients ont été inclus et traités : âge médian =
59 ans (36-72), 21 femmes, 19 hommes, 30 adénocarcinomes,
1 bronchioloalvéolaire et 9 CBNPC sans différenciation. Les prin-
cipaux effets indésirables étaient attendus, à type de rash, diarrhée,
hématurie, protéinurie et nausées.
Au total, il y a eu 8 réponses complètes (20 %) et 26 stabilisa-
tions (65 %).
La survie médiane des patients traités était de 12,6mois, avec 73 %
de patients vivants à 6 mois et 51 % de patients vivants à 12 mois.
Une phase II randomisée comparant l’association au docétaxel
±bévacizumab est prévue. Il n’y a pas eu d’étude de corrélation
des réponses aux éventuelles mutations de l’EGFR, comme dans
les études présentées dans le chapitre Cancer bronchique, p. 1 3 0 .
Une phase II randomisée testant l’association docétaxel-erloti-
n i b ± bévacizumab est prévue.
M. Dickler et al. (abstract 2001 actualisé) ont présenté une étude
de phase II associant l’erlotinib au bévacizumab chez les patientes
atteintes de cancer du sein métastatique.
Le bévacizumab administré seul donne en moyenne, dans les
études de phaseII, 9 % de réponse objective. L’erlotinib en mono-
thérapie, chez les patientes lourdement prétraitées, donne 4 % de
réponse objective.
L’étude présentée ici est une phase II associant les deux drogues
chez les patientes en deuxième et troisième lignes de traitement :
erlotinib à 150 mg/j p.o. +bévacizumab 15 mg/kg i.v. tous les
2 1 jours. Il y avait 24 patientes éligibles, dont 18 évaluables. L’âge
médian des patientes était de 52 ans, et 68 % présentaient des
métastases viscérales. Il y a eu une RP (6 %), 6 stabilisations à
9semaines (33 %), une stabilisation > 6mois (6 %) et 10 pro-
gressions (56 %). La médiane de temps jusqu’à progression était
de 4 mois. Chez les patientes répondeuses, la durée de réponse
est de plus de 8,8 mois. La toxicité était modérée : rash, diarrhée,
fatigue, stomatite.
Les auteurs ont, par ailleurs, procédé à une analyse biologique
des tumeurs pour rechercher une corrélation avec les réponses
cliniques. Parmi les patientes évaluables, 6 étaient EGFR1+,
2 étaient EGFR2+ et 7 ne surexprimaient pas l’EGFR. La patiente
en réponse partielle était ER-, PR-, HER2-, EGFR1+ et ne pré-
sentait pas de mutation de l’EGFR (exon 18-24). Dans cette étude,
la surexpression de l’EGFR ne paraît pas suffisante pour sélec-
tionner les patientes susceptibles de répondre.
Ces nouvelles thérapies cytotoxiques doivent s’accompagner d’une
nouvelle méthodologie d’évaluation, permettant de mesurer bio-
logiquement leur effet, afin de mieux comprendre leur activité
clinique et de l’optimiser.
H.S. Rugo et al. (abstract 2503 actualisé) ont présenté la première
étude de phase I de l’AG-013736, antiangiogénique oral, chez
les patients présentant une tumeur solide métastatique, avec éva-
luation clinique et radiologique par IRM de la réponse vasculaire
tumorale. L’AG-013736 est un puissant inhibiteur des TK des
récepteurs 1, 2 et 3 du VEGF, du PDGF et de c-KIT.
L’AG-013736 était administré à dose croissante par voie orale
une ou deux fois par jour par cure de 28 jours. Au total, 36 p a t i e n t s
ayant reçu au moins une ligne de traitement ont été inclus et trai-
tés au sein de 6 cohortes de doses croissantes (2 à 20 mg/j). Il
s’agissait de patients présentant les cancers suivants : sein (11),
thyroïde (5), rein (5), poumon (4) et autres (5). La pharmaco-
cinétique était modifiée par l’alimentation. La dose maximale
tolérée (DMT) a été établie à 5 mg x 2/j à jeun. Les principales
toxicités étaient : une hypertension artérielle (HTA), pour laquelle
un traitement a été nécessaire chez 61 % des patients ; des crises
convulsives associées à l’HTA ; une thrombose de la veine mésen-
térique compliquée de pancréatite (1 patient) ; des stomatites.
Il y a eu deux réponses partielles chez les patients présentant un
cancer du rein et une réponse partielle dans le cancer de la thy-
roïde. Les auteurs ont rapporté également 7 stabilisations de plus
de 4 mois. Une évaluation de la réponse vasculaire était réalisée
par IRM à J2, J28 et J56. La variation de l’intensité de prise de
contraste vasculaire était évaluée. Six des 18 patients ayant des
IRM sériées évaluables étaient considérés comme étant en réponse
vasculaire tumorale, définie par une diminution de plus 50 % du
rehaussement vasculaire. La drogue sera évaluée dans des essais
de phase II sur les tumeurs suivantes: cancer du rein, sein (+ docé-
taxel), mélanome, thyroïde et poumon non à petites cellules.
Parmi les autres études de phase I présentées, on notera l’asso-
ciation de topotécan oral à l’elacridar (administré également par
voie orale), qui agit sur les molécules présentes à la surface de la
paroi gastrique modulant la biodisponibilité du topotécan (abs-
tract 2003). L’association est peu toxique à dose efficace (100 m g
d’elacridar p.o.) et permet d’optimiser la biodisponibilité du topo-
técan, qui peut alors être administré par voie orale à la dose de
2 mg/j pendant 5 jours.
Le SB-715992 inhibe sélectivement la KSP (kinesin spindle pro-
tein) et permet d’agir sur le fuseau mitotique. La KSP est une cible
potentiellement très intéressante, car elle est surexprimée dans les
cellules tumorales, n’est active que durant la mitose et n’est pas
exprimée au sein des neurones en différenciation terminale, per-
mettant ainsi d’éviter la toxicité neurologique que l’on rencontre
avec les molécules agissant sur le fuseau (poisons du fuseau,
taxanes). Dans l’étude de phase I présentée (abstract 2004), la
toxicité limitante était la neutropénie. À la dose recommandée
pour les études de phase II (7 mg/m
2
), il n’y avait aucune toxi-
cité de grade 3 ou 4. Les principales toxicités étaient hématolo-
giques. Quelques stabilisations ont été observées (3 patients sur
27 : rein, côlon, ORL).
L’étude de R.S. Mc Dermott et al. (abstract 2033) est intéres-
sante, car les auteurs évaluent directement l’activité de l’agent
BMS-214662, inhibiteur de farnesyl transférase (FT), par le taux
d’inhibition de l’activité FT sur les cellules mononucléées san-
guines, en prenant pour substrat le peptide H-ras. La drogue était
administrée une fois par jour, pendant 5 jours consécutifs, tous
les 21 jours. Ils montrent qu’il n’y a aucune diminution de l’acti-
vité FT ainsi mesurée à une posologie inférieure à 81 m g / m
2
/j. Aux
doses supérieures, cette inhibition ne dure par ailleurs que 6 h e u r e s
après l’administration du produit. La DMT a été établie à
81 mg/m
2
/j (toxicités limitantes : diarrhée, neutropénie). Cepen-
dant, les auteurs concluent, d’après les données d’évaluation bio-
146
La Lettre du Cancérologue - Volume XIII - n
o
3 - mai-juin 2004
N
O U V E L L E S A P P R O C H E S

logique, qu’une administration quotidienne ne permet d’obtenir
qu’une inhibition transitoire de FT et que d’autres schémas
d’administration seraient peut-être plus efficaces cliniquement.
Dans l’étude de A.M. Alousi et al. (abstract 2020), c’est le risque
de neutropénie limitante secondaire au XK469 qui est prédit pour
chaque patient, par un modèle de test in vitro de sensibilité des
CFU-GM (cellules souches hématopoïétiques dérivées en culture)
à l’exposition à la drogue.
Enfin, dans cette catégorie de molécules, il faut citer les nombreuses
nouvelles taxanes actuellement en développement.
Les épothilones sont des macrolides cytotoxiques qui stabilisent
les microtubules et induisent un arrêt en mitose. Le KOS-862
(épothilone D) (abstract 2024) présente une toxicité neuro-
logique. Les études précliniques suggèrent des taux plasmatiques
stables en perfusion longue : des schémas de perfusion de
24 heures et 72 heures sont testés.
Le XAA296A (discodermolide) est un stabilisateur naturel de
microtubules, potentiellement plus efficace que le paclitaxel dans
les études précliniques. Dans l’étude de phase I présentée (abs-
tract 2025), il présente un très bon profil de tolérance : pas de
toxicité neurologique ou hématologique sévère.
Le DO/NDR/02 est une nouvelle formulation du paclitaxel :
celui-ci est délivré en nanoparticules, cette formulation permet-
tant de ne pas ajouter de crémophore. La drogue est donc admi-
nistrée sans prémédication, à des doses croissantes, de 135 à
375 mg/m
2
dans cette étude de phase I(abstract 2026). La DMT
de cette nouvelle formulation de paclitaxel est de 375 mg/m
2
, et
un taux de réponse de 50 % a été atteint chez les patientes ayant
un cancer du sein lourdement prétraitées.
L’ABI-007 obéit au même principe : nanoparticules de paclitaxel,
administrées cette fois selon un schéma hebdomadaire dans une étude
de phase I(abstract 2027). La DMT chez les patients prétraités
est de 100 mg/m
2
, 150 mg/m
2
chez les patients non prétraités.
Enfin, on peut citer deux nouvelles taxanes orales :
le DJ-927, qui paraît plus puissant que le paclitaxel et le docé-
taxel dans les études précliniques. Le profil de toxicité est sem-
blable à celui des taxanes standard (abstract 2028).
le BMS-275183, qui a également un profil de toxicité attendu
pour cette classe de molécule (neuropathies périphériques et
neutropénies). Plusieurs réponses objectives très prometteuses ont
été observées dans cette étude de phase I: 5/8 patients atteints
de CBNPC, 1/1 patient atteint de sarcome, 1/1 patient atteint de
cancer de prostate (abstract 2029).
IMMUNOTHÉRAPIE
L’ASCO 2004 nous a fourni quelques résultats encourageants
dans le domaine de l’immunothérapie.
Les résultats les plus intéressants concernent l’inhibition du
Cytotoxic T Lymphocyte-associated Antigen 4 (CTLA4).
La tolérance immunitaire périphérique est responsable de l’inac-
tivation fonctionnelle des lymphocytes T. Le CTLA4 est un récep-
teur présent à la surface des lymphocytes T et qui entraîne une régu-
lation négative des réponses immunitaires cellulaires. Le blocage
du CTLA4 peut permettre de rompre la tolérance immunitaire et
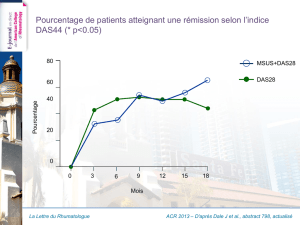
d’induire des réactions auto-immunes et antitumorales (figure 1).
Le CP-675206 est un anticorps bloquant le CTLA4. Dans l’étude
présentée par L.H. Camacho, du MD Anderson Cancer Center
(abstract 2505), les patients recevaient une injection i.v. unique
de CP-675206 à niveaux de dose croissants. Les doses étaient
de 0,01 mg/kg ( 3 patients), 0,1 mg/kg (3), 1 mg/kg (3), 3 m g / k g
(8), 6 mg/kg (5), 10 mg/kg (11) et 15 mg/kg (6), administrées en
une perfusion unique.
Les principaux effets indésirables étaient : réactions allergiques
cutanées (17 %), fatigue (17 %), prurit (11 %), diarrhée (11 %).
Les toxicités limitantes étaient la diarrhée et les réactions cutanées.
La DMT a été établie à 10 mg/kg en injection unique. Des réac-
tions auto-immunes mineures et réversibles ont été notées : vitiligo,
asthme, dermatite, diarrhée, hypophysite et hyperthyroïdie.
Quelques réponses spectaculaires ont été rapportées par les
a u t e u r s : 3 réponses complètes (durée de 13, 14 et 24 mois +), dont
u n e après chirurgie ; 2 réponses partielles (14 et 15 mois +) ; 5 s t a-
b i lisations, soit un bénéfice clinique de 25 % (10 patients sur 39).
Même si l’on peut se méfier de l’auto-immunité induite par le
traitement, les réponses observées après une injection unique
sont extrêmement prometteuses.
Un autre anticorps, le removab, présente un structure originale :
il s’agit d’un anticorps trifonctionnel. Il présente une fraction Fc
capable de se lier aux cellules présentatrices d’antigènes ; il est
bispécifique pour la molécule EpCAM présente à la surface des
cellules tumorales et pour le CD3 associé au récepteur T des
lymphocytes T.
L’équipe de Munich (abstract 2504) a évalué cet anticorps pour le
traitement de l’ascite tumorale des patientes atteintes de cancer de
l’ovaire. Ils ont traité 23 patientes qui ont reçu jusqu’à 5 i n j e c t i o n s
intrapéritonéales de removab sur une période de 13 jours. Le trai-
tement induisait une réduction significative du nombre de cellules
tumorales présentes dans l’ascite, après chaque injection. Toutes les
patientes présentaient à la fin du traitement un pourcentage de cel-
lules tumorales compris entre 0 et 0,1. Cela s’accompagnait d’une
diminution de la production d’ascite : 22 des 23 patientes ne néces-
sitaient plus de ponction à la fin de la période d’observation (J37).
147
La Lettre du Cancérologue - Volume XIII - n
o
3 - mai-juin 2004
N
O U V E L L E S A P P R O C H E S
Figure 1. Blocage du CTLA4.

Le G17DT est un immunogène de la gastrine qui entraîne la pro-
duction d’anticorps neutralisant la gastrine 17, impliquée dans la
physiopathologie des cancers du pancréas. Dans cette très grande
étude randomisée, réalisée chez des patients atteints de cancer
du pancréas inopérable non candidats à une chimiothérapie, les
auteurs comparent le G17DT à un placebo et observent un avan-
tage en survie (médiane de 151 jours contre 82, p = 0,03) et un
avantage en temps jusqu’à altération de l’état général (médiane
138 versus 78 jours, p =0,04). Le traitement était par ailleurs très
bien toléré. Le G17DT constitue donc une avancée thérapeutique
notable pour les patients atteints de cancer du pancréas.
D’autres stratégies d’immunothérapie utilisant des cibles large-
ment étudiées en préclinique sont maintenant en cours de déve-
loppement dans des essais de phase I. On peut citer :
la modulation des réponses immunitaires par l’élimination in
vivo des cellules T régulatrices immunosuppressives CD4+CD25+
par la molécule denileukin diftitox (abstract 2506) ;
la vaccination par cellules dendritiques transfectées avec l’ARN
de hTERT, dont l’objectif est d’induire des réponses immunitaires
dirigées vers la télomerase reverse transcriptase surexprimée dans
90 % des tumeurs solides.
CIBLES MOLÉCULAIRES
Le ciblage moléculaire est l’une des stratégies les plus exploitées
dans les nouvelles approches actuelles. On va présenter dans ce
paragraphe les voies alternatives ou les stratégies nouvelles de
ciblage moléculaire.
C’est le cas, par exemple, du ciblage du VEGF.
Outre le bévacizumab, dont il a été question plus haut, ainsi que
dans les autres chapitres de ce numéro, on peut inhiber l’action
du VEGF par l’utilisation d’un oligonucléotide antisens ciblant
le VEGF-A, -C, -D (Veglin
®
).
Dans l’étude de phase I réalisée chez 26 patients en échec de trai-
tement, Veglin
®
était administré en perfusion de 2 heures, à
niveaux de dose croissants, pendant 5 jours toutes les 2 s e m a i n e s .
Le traitement était très bien toléré, sans toxicité limitante ; la DMT
n’a pas été atteinte. Des réponses objectives ont été observées dès
la phase I (abstract 3008).
Une autre approche originale et prometteuse est le VEGF-Trap, qui
est constitué des portions des domaines extracellulaires de VEGFR1
et VEGFR2 fusionnées au domaine Fc de l’IgG1 humain. La molé-
cule chimérique ainsi constituée est capable de capter et d’inacti-
ver les formes circulantes et tissulaires de VEGF-A de façon bien
plus puissante que les anticorps monoclonaux. Dans l’étude de
p h a s e I présentée par J. Dupont et al. (abstract 3009 actualisé), l e
traitement induisait des effets indésirables à type d’hypertension et
de protéinurie. Des stabilisations prolongées ont été rapportées.
Les GIST représentent un modèle de développement des thérapeu-
tiques ciblées, avec l’imatinib, mais posent maintenant aussi la ques-
tion de la nécessité de trouver des voies alternatives de traitement.
En effet, de plus en plus de résistances secondaires à l’imatinib
apparaissent après réponse initiale. Ces résistances peuvent être cor-
rélées à l’apparition de mutations secondaires des TK de KIT ou
du PDGFRA ou à l’activation de voies de signalisation alternatives.
G.D. Demetri et al. (abstract 3001 actualisé) ont présenté un essai
de phase I/II avec le SU 11248 chez des patients progressant sous
imatinib. Des biopsies des tumeurs étaient réalisées, afin de
rechercher les mutations des kinases de KIT et PDGFRA ; une
imagerie anatomique (scanner ou IRM) et fonctionnelle (FDG-
PET) était couplée à l’étude.
Au total, 97 patients ont été inclus ; les données sont disponibles
pour 92 d’entre eux : il s’agissait de 88 patients en progression
et de 4 patients intolérants à l’imatinib.
Le traitement était bien toléré, avec, comme toxicités majeures :
fatigue (74 %), diarrhée (68 %), nausées (54 %), dépigmentation
cutanée (40 %), HTA grade 3-4 (13 %).
Les auteurs rapportent 7 réponses partielles (8 %), 53 stabilisa-
tions (58 %), soit un bénéfice clinique de 65 %. La médiane de
temps jusqu’à progression est de 34 s e m a i n e s ; la médiane de sur-
vie globale n’est pas atteinte. L’analyse moléculaire des tumeurs
a été réalisée chez 57 patients ayant plus de 6 mois de suivi et
des biopsies disponibles. Elle a permis de déterminer l’émer-
gence de clones résistants présentant des schémas de mutations
complexes de KIT ou PDGFR. Le SU 11248 peut donc permettre
de traiter les patients atteints de GIST devenus résistants à l’ima-
tinib et d’obtenir des stabilisations prolongées.
Une voie alternative de traitement des GIST devenus résistants
à l’imatinib peut être l’inhibition des voies de signalisation intra-
cellulaire en aval du récepteur.
La voie de mTOR présente, dans les modèles in vitro, une forte
interaction avec KIT. L’inhibition du récepteur couplée à l’inhi-
bition de la transduction du signal peut être réalisée en associant
l’imatinib et l’évérolimus, inhibiteur sélectif de mTOR.
Dans l’étude présentée par A.T. Van Oosterom et al. (abstract
3002 actualisé), les patients inclus étaient en progression après
au moins 24 mois de traitement par imatinib à dose optimale (et
avaient reçu au moins 2 mois de traitement à plus de 600 mg/j).
Après une période d’arrêt de l’imatinib (wash out), les patients rece-
vaient l’imatinib seul, puis l’évérolimus seul, puis l’association des
d e u x : cela permettait une évaluation pharmacocinétique de chaque
drogue seule, puis de l’association. Une évaluation radiologique
(IRM, FDG-PET) et une évaluation biologique (biopsies des
tumeurs) ont été également réalisées. Sur les 12 patients évalués en
pharmacocinétique, l’imatinib induisait une augmentation des taux
d’évérolimus, tandis que l’évérolimus n’influait pas sur les taux
d’imatinib ou de ses métabolites. Le traitement était très bien toléré.
L’arrêt de l’imatinib entraînait une augmentation importante de
l’hyperfixation sur le PET après l’arrêt, suivie d’une décroissance
sous traitement par l’association. Il n’a pas été observé de réponse
objective. Un patient a présenté une stabilisation prolongée. Le
message de cette étude est qu’il ne faut pas interrompre le traite-
ment par imatinib, qui permet de maintenir un contrôle de clones
sensibles résiduels. L’arrêt du traitement induit une réactivation de
ces clones. L’étude sera poursuivie avec un nouveau schéma : pas
d’arrêt de l’imatinib et escalade des doses d’évérolimus.
Enfin, dans le domaine du ciblage des récepteurs, il semble per-
tinent de multiplier les cibles que l’on va inhiber, afin d’agir sur
différentes voies de signalisation cellulaire.
Le GW 572016 en est un très bon exemple : il s’agit d’un inhi-
biteur oral, réversible et spécifique de la TK du récepteur d’ErbB1
(EGFR) et ErbB2 (HER-2/neu). ErbB1 et ErbB2 forment des hétéro-
148
La Lettre du Cancérologue - Volume XIII - n
o
3 - mai-juin 2004
N
O U V E L L E S A P P R O C H E S

dimères à la surface des cellules cancéreuses induisant un signal
de prolifération et de survie intracellulaire puissant.
Dans l’étude de phase II présentée par K.L. Blackwell et al. (abs-
tract 3006 actualisé), les patientes étaient atteintes de cancer du
sein métastatique HER2++ confirmé par FISH ou HER2+++ et
traitées préalablement par trastuzumab (médiane de durée de trai-
t e m e n t =4 6 semaines, variant de 6 à 144 semaines). Les patientes
étaient lourdement prétraitées : première ligne 100 %, deuxième
ligne 59 %, troisième ligne 22 %.
Le GW 572016 (lapatinib) était administré par voie orale à la dose
de 1 500 mg/j (initialement 1 250 mg, puis amendement après
1 3 patientes pour 1 5 0 0 mg). L’étude prévoit l’inclusion de
80 patientes ; l’évaluation intermédiaire prévue à 40 patientes a
été présentée.
Le traitement est très bien toléré (effets indésirables majeurs :
rash, fatigue, diarrhée, nausée, anorexie, vomissement). Il y a eu
2réponses partielles et 17 stabilisations à 8 semaines, soit un
bénéfice clinique de 46,3 %. Le taux de survie sans récidive à
8 semaines est de 46,3 %, et de 24,4 % à 16 semaines.
ET POUR FINIR… L’ACTUALITÉ INCONTOURNABLE
DES TUMEURS CÉRÉBRALES !
Comme en 2003, les tumeurs du système nerveux raflent une
place en session plénière grâce à une étude simple, pertinente et
bien menée.
Il s’agit de l’étude du groupe Brain de l’EORTC dans les glio-
blastomes (GBM), présentée par R. Stupp et al. (abstract 2 actua-
lisé).
Le traitement standard des GBM, après biopsie ou résection, est
la radiothérapie (RT). Le témozolomide (TMZ) est un nouvel
agent méthylant ayant démontré son activité dans les gliomes
malins en rechute. Le TMZ a un effet synergique en association
avec la radiothérapie dans les études in vitro et dans une précé-
dente étude de phase II.
Les patients étaient randomisés entre une RT standard (60 Gy en
3 0 fractions de 2 Gy) et la même RT en association au TMZ
concomitant (TMZ 75 m g / m
2
/j, pendant 42 jours), suivie de
6 cycles de TMZ adjuvant (150-200 m g / m
2
/j pendant 5 jours, tous
les 28 jours). Au total, 573 patients ont été traités. Les principales
toxicités du traitement sont : fatigue, rash, nausées-vomissements,
troubles de la vue ; la toxicité hématologique est minime. Le suivi
médian est de 2 ans. Quatre cent trente-six patients sont décédés.
Il y a une augmentation significative de la survie sans rechute :
5mois dans le bras RT versus 6,9 mois dans le bras RT-TMZ
(p < 0,0001).
Il y a une augmentation significative de la survie globale :
1 2 , 1 mois dans le bras RT versus 14,6 mois dans le bras RT-TMZ
(p < 0,0001).
Il s’agit donc là de la première étude démontrant un avantage en
survie conféré par la chimiothérapie dans les GBM.
Cette étude établit un nouveau standard de traitement.
149
La Lettre du Cancérologue - Volume XIII - n
o
3 - mai-juin 2004
N
O U V E L L E S A P P R O C H E S
N
O U V E L L E S D E L
’
I N D U S T R I E P H A R M A C E U T I Q U E
C o m m u n i q u é s d e s c o n f é r e n c e s d e p r e s s e , s y m p o s i u m s , m a n i f e s t a t i o n s o r g a n i s é s p a r l ’ i n d u s t r i e p h a r m a c e u t i q u e
Pfizer Oncologie lors du 40
e
Congrès
de l’ASCO
Le Congrès de l’ASCO 2004 a été l’occasion
de découvrir de nouveaux résultats prometteurs
pour certains produits de la gamme Pfizer
Oncologie, et notamment ceux du SU11248 et
d’Aromasine
®
.
Le SU11248 est un inhibiteur de quatre récep-
teurs à la tyrosine kinase: le VEGFR, le PDGFR,
le KIT et le FLT3, ce qui lui confère un effet anti-
tumoral doublé d’un effet antiangiogénique.
Le SU11248 est administré par voie orale à la
dose de 50 mg par jour. Un cycle de traitement
comporte une prise quotidienne pendant quatre
semaines suivies de deux semaines de repos.
Cette posologie a été recommandée par une
étude de phase I publiée à l’ASCO 2003 (Ray-
mond E, abstract 769).
Une étude de phase II ouverte multicentrique a
rapporté les résultats du SU11248 chez des
patients atteints d’un cancer du rein métasta-
tique prétraités par cytokines (abstract 4500).
Le taux de réponse objective sur 63 patients a
été de 33 %. Une stabilisation pendant plus de
3mois a été observée chez 23 patients (37 %).
de mutations : les malades avec une mutation de
l ’ e x o n 9 du c-KIT ont une réponse plus importante.
Une phase III est en cours dans cette indication.
Par ailleurs, de nouvelles données sur Aroma-
sine
®
ont été présentées à l’ASCO.
Une étude a rapporté l’efficacité de l’exe-
mestane en première ligne de traitement pour le
cancer du sein localement avancé ou métasta-
tique (abstract 515) : avec une SSP de 10,9 m o i s
versus 6,7 mois sous tamoxifène (p = 0,04), un
taux de RO de 44 % versus 29 % et un profil de
tolérance favorable, Aromasine
®
a démontré sa
place en première ligne dans le cancer du sein
localement avancé ou métastatique.
Une autre étude a démontré son faible impact
sur la densité osseuse, lors de son administra-
tion pendant deux ans en situation adjuvante
(abstract 518). Aucune patiente n’a développé
d’ostéoporose de novo, et il y a eu la même pro-
portion d’ostéoporose dans les deux bras chez
les patientes ostéopéniques. L’impact est nul sur
le rachis lombaire et faible sur le fémur. Cette
étude démontre ainsi l’absence d’effet majeur
sur l’os, notamment celle de majoration de
l’incidence des fractures.
APP
La survie sans progression (SSP) est à 8,3 mois
et la survie à un an à 65 %.
Peu d’effets indésirables de grade 3 ont été
observés, et aucun de grade 4.
La durée médiane de traitement a été de 9 mois
et les doses de certains patients ont pu être aug-
mentées. Cette efficacité clinique est remar-
quable par rapport aux séries historiques du
Memorial Sloan Kettering, qui ne dépassent pas
3mois de SSP (JCO 2004;24:454).
Le développement de la molécule se poursuit
par une étude de phase III randomisée en pre-
mière intention versus interféron.
Une étude de phase II a testé le SU11248 dans
les GIST résistants à l’imatinib (par mutations
acquises de c-KIT, et notamment sur l’exon 9
et 11 du récepteur) (abstract 3001).
Avec 8 % de réponses objectives (RO) et 58 %
de stabilisations, le bénéfice clinique est obtenu
dans 65 % des cas.
Le TTP est de 34 semaines et la médiane de sur-
vie n’est pas atteinte. Ces résultats sont remar-
quables chez des patients en dessous de toute res-
source thérapeutique. Une corrélation a été
retrouvée entre la réponse au traitement et le niveau
1
/
5
100%