L Imagerie des complications cardiaques des traitements anticancéreux

252 | La Lettre du Cancérologue • Vol. XVIII - n° 5 - mai 2009
DOSSIER THÉMATIQUE
Toxicité cardiovasculaire
des traitements anticancéreux
Imagerie des complications
cardiaques des traitements
anticancéreux
(médecine nucléaire, IRM)1
Imaging of chemotherapy-induced cardiotoxicity
(nuclear medicine, cardiac MRI)
A. Manrique*, D. Agostini**
1 © La Lettre du Cardiologue 2009;
421:14-5.
* Service commun des investigations
humaines, GIP Cyceron, Caen.
** Service de médecine nucléaire,
CHU de Caen.
L
es anthracyclines constituent une classe
thérapeutique essentielle dans la prise en
charge initiale des lymphomes et du cancer
du sein. Une autre molécule, le trastuzumab, s’est
récemment imposée comme un élément indis-
pensable dans l’arsenal thérapeutique du cancer
du sein.
La cardiotoxicité reste un effet indésirable sérieux
des anthracyclines comme du trastuzumab, lequel
peut être à l’origine d’une myocardiopathie présen-
tant les mêmes caractéristiques cliniques que celle
induite par les anthracyclines. Cette toxicité conduit
parfois à limiter, voire à interrompre, le traitement
malgré son efficacité sur le plan carcinologique.
Des données suggèrent que, lors du traitement des
lymphomes, la prévalence de la cardiotoxicité est
élevée et que les doses seuils au-delà desquelles elle
apparaît sont probablement sous-estimées. Ainsi,
la prévalence des complications cardiaques dans
l’année suivant une chimiothérapie par CHOP a été
estimée rétrospectivement à 20 % dans une série
de 135 patients atteints de lymphome non hodgki-
nien (1). Une dose cumulée supérieure à 200 mg/ m2
et un âge supérieur à 50 ans sont des facteurs de
risque importants (1). Une diminution précoce de
la fraction d’éjection évaluée par mesure isotopique
est détectable dès le seuil de 200 mg/ m2, et semble
prédictive d’une toxicité cardiaque tardive (2). La
surveillance en cours de traitement fait donc très
couramment appel aux méthodes d’imagerie pour
l’évaluation de la fraction d’éjection du ventricule
gauche (FEVG).
Scintigraphie
des cavités cardiaques
La ventriculographie isotopique, ou scintigra-
phie des cavités cardiaques, est un examen de
réalisation simple qui constitue depuis plus de
20 ans une méthode de référence pour calculer la
FEVG. L’examen est réalisé en respiration libre, en
oblique antérieur gauche à 45°, après marquage
des globules rouges in vivo au 99mTc. L’acquisi-
tion dure entre 6 et 10 minutes et ne nécessite
aucune préparation particulière. La synchronisation
à l’électrocardiogramme nécessite en principe que
le patient soit en rythme sinusal, mais l’examen
reste possible en cas de fibrillation auriculaire si le
rythme n’est pas trop irrégulier. Le traitement infor-
matique des données dure moins d’une minute, et
les outils automatisés, largement disponibles, assu-
rent une excellente reproductibilité interexamen
de la technique (< 5 %).
La réalisation d’un dépistage précoce, avant que
n’apparaissent les signes cliniques d’insuffisance
cardiaque, est de la plus haute importance. Chez
les patients traités par anthracyclines, l’attitude
couramment admise consiste à surveiller de façon
régulière la FEVG, dont la diminution précède et

La Lettre du Cancérologue • Vol. XVIII - n° 5 - mai 2009 | 253
Résumé
Les techniques scintigraphiques de surveillance des chimiothérapies restent dominées par l’angiographie
isotopique. La place de l’IRM reste encore à définir.
Mots-clés
Angiographie
isotopique
Résonance
magnétique
Summary
Among isotopic technics to
detect cardiac side-effects of
anticancer drugs, radionuclide
angiography remains in first
line. Although MR imaging
is also helpful, its indications
remain to be more acurately
defined.
Keywords
Radionuclide angiography
Magnetic resonance
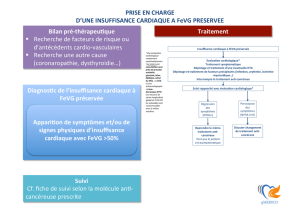
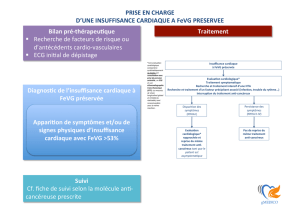
annonce la survenue retardée des signes cliniques
(3, 4). Il est proposé un arrêt du traitement lors
de l’apparition d’une dysfonction ventriculaire
gauche attestée par la combinaison d’une FEVG
inférieure à 50 % et d’une diminution d’au moins
10 % de la FEVG par rapport à la valeur initiale.
Cette attitude repose sur l’algorithme, proposé en
1987 par R.G. Schwartz et al. (5) : l’utilisation de
cet algorithme évalué sur 1 500 patients traités par
anthracyclines et suivis durant 7 ans, avait entraîné
une diminution d’un facteur 4 de l’incidence d’in-
suffisance cardiaque cliniquement avérée. Une
nouvelle évaluation de la FEVG est recommandée
après des doses cumulatives de 240-300 mg/m
2
et de 400-450 mg/m
2
de doxorubicine, puis après
chaque dose supplémentaire. Une surveillance plus
rapprochée est recommandée chez les patients
présentant une dysfonction ventriculaire gauche
à l’état de base ou une maladie cardiaque connue,
et en cas de radiothérapie concomitante ou anté-
rieure ou d’exposition simultanée à tout autre agent
cardiotoxique (6). Concernant le suivi des patients
sous trastuzumab, un algorithme de surveillance
rapprochée de la fraction d’éjection toutes les
12 semaines a été récemment proposé par l’équipe
de la Mayo Clinic (7), fondé sur la cinétique d’appa-
rition des complications cardiaques rapportées dans
les essais thérapeutiques, mais son efficacité pour
prévenir des complications tardives reste encore à
déterminer.
L’évaluation de la fraction d’éjection à l’effort
par méthode isotopique a été proposée avec un
certain succès, mais reste très limitée en pratique
en raison de l’état clinique de ces patients, souvent
altéré sous les effet conjugués de la maladie, de
la chimiothérapie et des pathologies associées
(anémie, etc.).
Autres techniques
scintigraphiques
Par le passé, la scintigraphie myocardique aux
anticorps antimyosine marqués avait permis de
différencier une lyse myocytaire authentique d’une
diminution transitoire et réversible de la FEVG après
chimiothérapie par anthracyclines (8, 9). En effet, il
avait été rapporté qu’une action inotrope négative
pouvait être responsable d’une altération transitoire
de la fonction contractile après une cure d’anthra-
cyclines, ce qui justifiait de ne mesurer la FEVG
qu’à distance de la dernière cure, avant la réali-
sation de la cure suivante. Les anticorps antimyo-
sine marqués à l’indium, ne se fixant au niveau du
myocarde qu’en cas d’externalisation de la myosine
intracellulaire consécutivement à la lyse cellulaire,
permettaient de mettre en évidence de façon non
invasive les lésions myocardiques secondaires à
la toxicité des anthracyclines. Cette technique,
pourtant prometteuse, a été abandonnée après le
retrait des anticorps antimyosine marqués, dont
le marché a été jugé trop étroit.
IRM
L’IRM cardiaque permet une analyse morpho-
logique des cavités cardiaques et le calcul
des fractions d’éjection des deux ventri-
cules. Sa complexité d’utilisation au regard de
la simplicité des méthodes échographiques
ou encore scintigraphiques n’en fait cependant qu’un
examen de seconde intention dans cette indication.
En revanche, l’IRM offre des possibilités originales
de caractérisation tissulaire. Il a été montré que, en
cas de lésion myocardique secondaire à un infarctus
ou à une myocardite, une augmentation importante
du signal survient 15 à 20 minutes après l’injection
d’un produit de contraste paramagnétique (sels de
gadolinium), augmentation qui permet de mettre
en évidence les lésions à un stade initial.
Dans une étude récente (10), une IRM cardiaque
a été effectuée chez 10 patientes présentant une
toxicité avérée au trastuzumab, dont le diagnostic
reposait sur une diminution de FEVG inférieure
à 40 % en scintigraphie ou en échographie. Les
10 patientes de cette étude présentaient toutes un
hypersignal tardif en IRM après injection de gado-
linium, prédominant au niveau de la paroi latérale,
et de siège sous-épicardique dans tous les cas. Ce
type de lésions est très similaire à ce qui est observé
dans les cas de myocardite. Cela est cohérent avec
la récupération fréquente d’une fonction ventricu-
laire gauche normale après interruption du traite-

Vol. I - N° 1
janv-fév-mars
2008
Société éditrice : DaTeBe SAS
CPPAP en cours - ISSN : en cours
Trimestriel
Périodique de formation en langue française
Vol. I - N° 1
janv-fév-mars
2008
Société éditrice : DaTeBe SAS
CPPAP en cours - ISSN : en cours
Trimestriel
Périodique de formation en langue française
20 revues
Rendez-vous sur le site
www.edimark.fr
Abonnez-vous
à La Lettre du Cancérologue
et accédez à plus de 20 revues
dont notre nouvelle revue
Il vous est possible de télécharger
gratuitement le premier exemplaire paru
Imagerie des complications cardiaques des traitements
anticancéreux (médecine nucléaire, IRM)
DOSSIER THÉMATIQUE
Toxicité cardiovasculaire
des traitements anticancéreux
ment chez ces patientes, rendant parfois possible la
reprise du traitement dans un second temps. Dans
cette dernière étude, 6 des 10 patientes ont vu leur
fonction ventriculaire gauche se normaliser après
interruption du trastuzumab. Cependant, les 4 autres
patientes présentaient des signes de dysfonction
persistante à 6 mois, et ce malgré un traitement
approprié de l’insuffisance cardiaque, incluant IEC
et bêtabloquants.
Conclusion
L’imagerie des complications cardiaques des chimio-
thérapies reste très largement fondée sur l’utilisation
de la fraction d’éjection isotopique. L’IRM cardiaque
avec injection est une technique prometteuse, parti-
culièrement pour l’évaluation des complications
liées à l’utilisation du trastuzumab chez les patientes
suivies pour un cancer du sein. ■
1. Limat S, Demesmay K, Voillat L et al. Early cardiotoxi-
city of the CHOP regimen in aggressive non-Hodgkin’s
lymphoma. Ann Oncol 2003;14:277-81.
2. Nousiainen T, Jantunen E, Vanninen E, Hartikainen J.
Early decline in left ventricular ejection fraction predicts
doxorubicin cardiotoxicity in lymphoma patients. Br J
Cancer 2002;86:1697-700.
3. Choi BW, Berger HJ, Schwartz PE et al. Serial radionu-
clide assessment of doxorubicin cardiotoxicity in cancer
patients with abnormal baseline resting left ventricular
performance. Am Heart J 1983;106:638-43.
4. Alexander J, Dainiak N, Berger HJ et al. Serial asses-
sment of doxorubicin cardiotoxicity with quantitative
radionuclide angiocardiography. N Engl J Med 1979;
300:278-83.
5. Schwartz RG, McKenzie WB, Alexander J et al. Congestive
heart failure and left ventricular dysfunction complicating
doxorubicin therapy. Seven-year experience using serial radio-
nuclide angiocardiography. Am J Med 1987;82:1109-18.
6. Panjrath GS, Jain D. Monitoring chemotherapy-induced
cardiotoxicity: role of cardiac nuclear imaging. J Nucl Cardiol
2006;13:415-26.
7. Sengupta PP, Northfelt DW, Gentile F, Zamorano JL,
Khandheria BK. Trastuzumab-induced cardiotoxicity: heart
failure at the crossroads. Mayo Clin Proc 2008;83:197-
203.
8. Valdes Olmos RA, Ten Bokkel Huinink WW, Ten Hoeve RF
et al. Usefulness of indium-111 antimyosin scintigraphy in
confirming myocardial injury in patients with anthracy-
cline-associated left ventricular dysfunction. Ann Oncol
1994;5:617-22.
9. Carrio I, Lopez-Pousa A, Estorch M et al. Detection of
doxorubicin cardiotoxicity in patients with sarcomas by
indium-111-antimyosin monoclonal antibody studies. J Nucl
Med 1993;34:1503-7.
10. Fallah-Rad N, Lytwyn M, Fang T, Kirkpatrick I, Jassal DS.
Delayed contrast enhancement cardiac magnetic resonance
imaging in trastuzumab induced cardiomyopathy. J Cardio-
vasc Magn Reson 2008;10:5.
Références bibliographiques
1
/
3
100%