Brèves… Brèv es… La néogenèse des cellules

139
Métabolismes Hormones Diabètes et Nutrition (VIII), n° 3, mai/juin 2004
Brèves…
Brèves…
La néogenèse des cellules
bêta du pancréas révisée
Le nombre de diabétiques dans le
monde devrait passer de quelque
150 millions aujourd’hui à 300 mil-
lions d’ici 2025. Il s’agit donc d’un
véritable problème de santé publique.
Le diabète de type 1 est une maladie
auto-immune touchant les cellules
sécrétant l’insuline (cellules β) dans
les îlots de Langerhans. Si l’injec-
tion d’insuline permet d’équilibrer
plus ou moins efficacement les taux
de glucose des diabétiques de type 1,
il ne s’agit pas d’un traitement curatif.
En revanche, les avancées récentes
de la thérapie cellulaire permettent
d’envisager une alternative poten-
tielle aux injections quotidiennes
d’insuline et constituent une pro-
messe d’amélioration du traitement
de cette maladie. Actuellement, la
greffe d’îlots de Langerhans, couplée
à des traitements immunosuppres-
seurs de bonne tolérance, est prati-
quée avec succès. Cependant, l’appli-
cation de cette thérapie à un nombre
élevé de patients est limitée par le
nombre de donneurs. De ce fait, le
développement de nouvelles straté-
gies visant à produire de nouvelles
cellules βà partir de cellules souches
capables de proliférer et de se diffé-
rentier pour régénérer les organes, ou
encore à partir de cellules embryon-
naires ou adultes, constitue un enjeu
majeur pour l’avenir.
Deux grandes hypothèses ont été
avancées jusqu’ici pour expliquer
l’origine des cellules βpancréatiques
adultes. Le premier modèle propose
l’existence de cellules souches loca-
lisées dans l’épithélium des canaux
pancréatiques et/ou dans les îlots de
Langerhans. Ces cellules pourraient
être à l’origine de nouvelles cel-
lules βdans des îlots de Langerhans
préexistants, et seraient également
capables, sous la forme d’agrégats,
de générer de nouveaux îlots (1-3).
L’autre hypothèse, basée sur des
expériences d’incorporation de thy-
midine tritiée, suggère que les cel-
lules endocrines pancréatiques adultes
appartiendraient à une classe de tis-
sus qui se régénèrent par division
des cellules déjà différenciées (self-
duplication) (4). Des travaux récents
émanant de l’équipe de D.A. Mel-
ton, à Cambridge (MA, États-Unis),
viennent étayer la seconde hypothèse
(5). Ils montrent en effet que des cel-
lules totalement différenciées conser-
vent une certaine aptitude à prolifé-
rer in vivo. La participation des
cellules souches dans la régénéra-
tion des cellules βdu pancréas est par
ailleurs fortement remise en ques-
tion au cours de cette étude.
L’originalité de ces travaux repose
sur l’approche dynamique utilisée,
qui permet de suivre le lignage des
cellules βpancréatiques adultes. Les
auteurs ont développé une méthode
ingénieuse qui permet de distinguer,
chez la souris adulte, les cellules β
dérivant des cellules souches de celles
dérivant des cellules βdifférenciées
(figure). Pour cela, ils ont conçu des
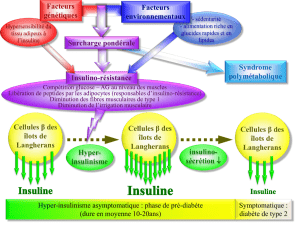
Figure. D’où viennent les cellules ß ? Dor et al. ont développé un modèle de souris bitrans-
génique permettant d’étudier le lignage des cellules ß. a) Les auteurs ont inséré chez la sou-
ris un gène qui présente la région promotrice du gène de l’insuline fusionnée à un gène codant
une recombinase. Ce gène chimère est exprimé spécifiquement dans les cellules ß du pancréas
et leur lignage. Par ailleurs, la recombinase pour laquelle il code n’est capable d’être activée
qu’en présence d’un analogue des estrogènes. L’administration d’un pulse d’hormone provoque
la translocation de la recombinase dans le noyau. Elle entraîne, au niveau du second trans-
gène, la délétion d’une région portant un codon stop et la production d’un marqueur (phos-
phatase alcaline). b) En réponse à l’hormone, de nombreuses cellules ß sont marquées au sein
d’un îlot. Les auteurs suivent ensuite le renouvellement des cellules ß. Trois cas de figure sont
possibles : 1) si les cellules souches (non marquées) génèrent de nouveaux îlots, des îlots non
marqués apparaîtraient au cours du temps ; 2) si des cellules souches régénèrent les cellules ß
dans des îlots préexistants, une dilution du marquage s’observerait lentement ; 3) si les cellules ß
s’autorépliquent, le nombre de cellules marquées devrait se maintenir au cours du temps,
puisqu’elles dérivent des cellules ß initialement marquées lors du pulse. Seule la troisième
situation a été observée.

Brèves…
Brèves…
140
Métabolismes Hormones Diabètes et Nutrition (VIII), n° 3, mai/juin 2004
souris transgéniques portant deux
transgènes : le premier code pour le
promoteur du gène de l’insuline
couplé au gène d’une recombinase
capable d’être transloquée au niveau
du noyau en présence d’estrogènes,
le deuxième code pour un gène mar-
queur dont l’expression est condi-
tionnée par l’expression de la recom-
binase. De cette manière, dans ce
modèle de souris bitransgénique, la
recombinase est exprimée spécique-
ment dans les cellules βtotalement
différenciées, et l’administration d’un
pulse d’un analogue des estrogènes
(cinq injections à l’âge de six à huit
semaines) entraîne la translocation
de la recombinase dans le noyau, et
l’expression spécifique du gène mar-
queur dans les cellules différenciées
et leur lignage.
Après 12 mois – la demi-vie moyenne
d’une souris –, tous les îlots expri-
ment le gène marqueur. L’idée selon
laquelle de nouveaux îlots seraient
formés chez l’adulte à partir des cel-
lules souches progénitrices (non mar-
quées) est donc démentie. Par ailleurs,
aucune dilution du nombre de cel-
lules marquées n’est observée, ce qui
suggère que les cellules βdérivent
de la division de cellules βpréexis-
tantes. De la même manière, ces
études montrent que la régénération
qui se met en place après une pan-
créatectomie se fait à partir de cel-
lules βdéjà en place, et non à partir
des cellules souches.
Ces travaux ouvrent des perspec-
tives intéressantes dans le domaine
de la thérapie cellulaire. Idéalement,
on pourrait en effet envisager de
prélever des cellules βpancréatiques
sur des personnes adultes décédées,
de stimuler leur division et de réim-
planter ces cellules en grandes quan-
tités chez des patients diabétiques. Il
reste cependant un long chemin à
parcourir, passant par des études fon-
damentales notamment, pour éluci-
der les mécanismes moléculaires qui
contrôlent la division des cellules β.
De plus, la question de l’extrapola-
tion des résultats de l’équipe de
D.A. Melton de la souris à l’homme
reste posée. En d’autres termes, les
cellules βadultes se divisent-elles à
partir des cellules βdifférenciées
chez l’homme comme chez la sou-
ris ? Selon K. Zaret (6), ces nouvelles
données ne doivent pas inciter à
abandonner les recherches qui sont
conduites sur la différenciation des
cellules βà partir des cellules souches.
En effet, le problème du nombre
limité de donneurs demeure. Par ail-
leurs, les cellules βprélevées post
mortem ont déjà un passé derrière
elles. De ce fait, elles ne pourront
peut-être pas prolonger leur vie sans
altérations chromosomiques qui les
rendraient insensibles au glucose ou
les transformeraient en cellules
tumorales.
I. Lihrmann,
INSERM U413,
université de Rouen
1. Bonner-Weir S, Sharma A. Pancreatic
stem cells. J Pathol 2002;197:519-26.
2. Zulewski H, Abraham EJ, Gerlach MJ et al.
Multipotential nestin-positive stem cells iso-
lated from adult pancreatic islets differen-
tiate ex vivo into pancreatic endocrine, exo-
crine, and hepatic phenotypes. Diabetes
1990;50:521-33.
3. Bonner-Weir S, Baxter LA, Schuppin GT,
Smith FE. A second pathway for regeneration
of adult exocrine and endocrine pancreas. A
possible recapitulation of embryonic deve-
lopment. Diabetes 1993;42:1715-20.
4. Tsubouchi S, Kano E, Suzuki H. Demons-
tration of expanding cell populations in
mouse pancreatic acini and islets. Anat Rec
1987;218:111-5.
5. Dor Y, Brow J, Martinez OI, Melton DA.
Adult pancreatic ß-cells are formed by self-
duplication rather than stem-cell differen-
tiation. Nature 2004;429:41-6.
6. Zaret K. Self-help for insulin cells. Nature
2004;429:30-1.
1
/
2
100%