89 n° L’ L’étude du nerf fémoro-cutané latéral

FICHE À DÉTACHER
278 | La Lettre du Neurologue Nerf & Muscle • Vol. XIII - n° 9 - octobre 2009
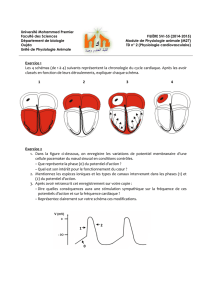
Figure 1. Repérage du trajet réel du NFCL au-dessous de l’épine iliaque antéro-
supérieure.
fiche
technique
Sous la responsabilité de son auteur
n° 89
P. Seror*
L’étude du nerf fémoro-cutané latéral
L’
étude du nerf fémoro-cutané latéral (NFCL) est restée pendant
de nombreuses années une technique réputée difficile, peu
fiable, et donc peu pratiquée par les neurophysiologistes.
Elle tentait d’observer la conduction nerveuse dans sa traversée de la
zone piège (arcade crurale).
Son étude plus distale (au-delà de la zone piège) est pourtant très
utile dans la pratique quotidienne pour affirmer une atteinte objective
devant un tableau évocateur de méralgie paresthésique. Cette dernière
est la pathologie nerveuse périphérique compressive la plus fréquente
des membres inférieurs, à égalité avec l’atteinte du nerf fibulaire au
col du péroné (SPE). Elle reste très mal connue des médecins généra-
listes et n’est pas toujours évoquée par les spécialistes (neurologues,
rhumatologues, rééducateurs ou chirurgiens orthopédistes) quand les
plaintes sensitives sont antérieures et miment une cruralgie. Il faut
donc que chaque neurophysiologiste pense à évoquer le diagnostic,
qu’il soit formé et devienne un expert dans la réalisation de ce test
électrophysiologique.
Ce dernier ne teste pas, comme cela est habituellement la règle dans
les syndromes canalaires, la conduction au niveau de la zone de
compression, mais au-delà. On ne recherche donc pas une diminu-
tion de la vitesse de conduction nerveuse, mais uniquement la perte
axonale sensitive évaluée par la perte d’amplitude du potentiel d’action
sensitif (PAS).
Réalisation
La réalisation pratique du test se déroule en 4 phases.
1. Repérage du trajet réel du NFCL au-dessous de l’épine iliaque antéro-
supérieure (EIAS).
2. Implantation des électrodes d’enregistrement.
3. Repérage du trajet réel du NFCL 12 cm au-dessous de la cathode
d’enregistrement.
4. Enregistrement du potentiel d’action sensitif
(figure 1)
.
* Neurophysiologiste, médecin rhumatologue, hôpital de la Pitié-Salpêtrière, Paris.
Description
On commence toujours par repérer l’EIAS de façon bilatérale à l’aide
d’un stylo à bille ou d’un crayon dermographique. On stimule alors
4 à 5 cm au-dessous de l’EIAS (ce qui correspond habituellement au
pli inguinal, là où le tissu sous-cutané est le plus fin) sur une ligne
allant de 5 à 6 cm latéralement jusqu’à 4 à 5 cm médialement. On
commence toujours par tester le côté sain. La stimulation est répétitive,
avec une fréquence de 3 Hz et une intensité de 15 mA. On explique
bien au patient qu’il va ressentir ces impulsions et que, suivant la
position du stimulateur, elles resteront locales ou descendront dans
la cuisse plus ou moins loin (éventuellement jusqu’au genou), sur sa
face latérale, antérieure ou interne. Il faut toujours commencer dans
une zone où la stimulation sera à distance du NFCL et restera locale,
et aller jusqu’au nerf fémoro-cutané médial. Une fois repéré le trajet
du NFCL à 15 mA, on diminuera l’intensité de stimulation jusqu’à 5
à 7 mA, stimulation minimale déclenchant encore une sensation à la
face latérale ou antérieure de la cuisse.

fiche technique n° 89
FICHE À DÉTACHER
La Lettre du Neurologue Nerf & Muscle • Vol. XIII - n° 9 - octobre 2009 | 279
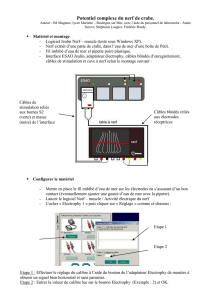
Figure 3. Repérage du trajet réel du NFCL 12 cm au-dessous de la cathode
d’enregistrement et enregistrement du potentiel d’action sensitif (PAS).
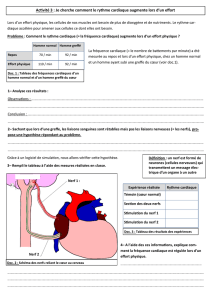
Figure 2. Implantation des électrodes d’enregistrement.
Questions/réponses
Pourquoi stimuler à 3 Hz et non à 1 Hz ?
Parce que, à 3 Hz, la sensation élicitée à distance dans la cuisse
jusqu’au-dessus du genou est beaucoup plus facilement perçue par
le patient qu’à la fréquence de 1 Hz.
Une fois le nerf repéré à 15 mA, pourquoi
diminuer l’intensité de la stimulation ?
À 15 mA chez un sujet non obèse, la stimulation diffuse au moins sur
2 cm autour de la cathode. En baissant l’intensité de la stimulation,
on arrive à un repérage plus précis et, parfois, on peut même repérer
2 branches de division déjà individualisées. Dans l’idéal, il faut que
la stimulation réalisée à 5 mm du trajet du nerf ne déclenche plus de
sensation à distance dans la cuisse.
Comment repérer le trajet du NFCL quand il est impossible
de déclencher une sensation à distance dans la cuisse du côté
pathologique?
Dans ce cas, on mesure, du côté sain, la distance entre le trajet du
NFCL et la ligne médiane sous-ombilicale et on teste le NFCL du côté
pathologique à la même distance de la ligne médiane. Quand aucune
sensation à distance ne peut être déclenchée uniquement du côté
pathologique, cela correspond à une perte axonale massive, et il est
très rare qu’un PAS soit enregistrable.
Une fois le repérage effectué, on implante 2 électrodes aiguilles mono-
polaires fines de 10 à 15 mm de longueur à 20 ou 25 mm de distance.
Il s’agit d’un geste très peu agressif, le pli inguinal n’étant pas une
région particulièrement douloureuse
(figure 2)
.
Chez les sujets particulièrement minces, peut-on réaliser
l’enregistrement avec une électrode bipolaire comme celle
utilisée pour enregistrer les autres PAS, par exemple celui du
nerf médian au poignet?
Oui, cela est possible, mais le problème majeur est alors de maintenir
en place cette électrode pendant l’enregistrement. Cela fait que l’uti-
lisation d’électrodes aiguilles est finalement le geste le plus simple
et surtout permet d’obtenir des potentiels de meilleure amplitude et
quasiment sans artefact de stimulation.
Pour repérer le NFCL à la cuisse, on trace une ligne qui joint la cathode
d’enregistrement et le milieu de la rotule
(figure 3A)
. Ensuite, 12 cm
au-dessous de la cathode d’enregistrement, on déplace le stimulateur de
part et d’autre de cette ligne sur 3 ou 4 cm jusqu’à obtenir le PAS avec
la meilleure amplitude. L’intensité de stimulation est habituellement de
15 à 25 mA et la fréquence de stimulation pendant l’enregistrement
est de 1 à 2 Hz
(figure 3B)
.
Pourquoi ne pas réaliser cette technique en antidromique, ce
qui donne habituellement des PAS de plus grande amplitude?
C’est possible, mais plus difficile. En effet, si le repérage du NFCL sous
l’EIAS reste le même, le repérage à la cuisse sans avoir l’enregistrement
du PAS à l’écran et en se fondant uniquement sur les sensations ressen-
ties par le patient dans la zone latérale du tiers inférieur de la cuisse est
beaucoup plus difficile, car les stimulations locales sont plus intenses,
donc plus désagréables, et gênent la perception des sensations à distance.
En pratique, il faudrait réaliser la technique orthodromique, puis profiter
du repérage distal (obtention du meilleur PAS) pour mettre en place les
aiguilles sous-cutanées à la cuisse et faire un deuxième enregistrement
en antidromique. Par ailleurs, les données de A. Lagueny et V. Laroy
en antidromique ne démontrent pas que l’amplitude du PAS soit plus
grande (moyenne : 12,1 µV pour A. Lagueny et 10,9 µV pour V. Laroy).
Comment faire chez les patients dont l’embonpoint est important?
L’embonpoint et l’obésité représentent la difficulté principale de la
technique d’enregistrement des PAS en général et du NFCL en parti-
culier. Pour la stimulation, il faut parfois augmenter l’intensité jusqu’à
30 ou 40 mA. Pour le recueil, il faut parfois enfoncer l’aiguille en
profondeur pour obtenir le PAS, et donc se faire aider (une troisième
main devenant indispensable), ou disposer d’aiguilles monopolaires
plus longues (20 à 35 mm).

fiche technique n° 89
FICHE À DÉTACHER
Résultats
Tableau I. Les valeurs normales
VCS
(m/s)
PAS Amp.
(µV) Ratio d’amplitude
D/G > 2,3***
Sujets normaux
(n = 30)
60 ± 5,3 16 ± 7 0
Les valeurs pathologiques
À partir des données normales, on peut considérer que tout PAS inférieur
à 3 µV est anormal si le patient n’est pas obèse et que l’enregistrement
est pratiqué avec des électrodes aiguilles. Cependant, comme l’atteinte
est le plus souvent unilatérale, le critère diagnostique le plus important
est l’asymétrie d’amplitude entre le côté sain et le côté pathologique, avec
un rapport d’amplitude qui doit être supérieur à 2,3
(figure 3)
. Notons
que cette valeur est tout à fait comparable à celle retenue par A. Lagueny.
L’application de ces critères chez les patients donne un taux de posi-
tivité supérieur à 90 %. En effet, compte tenu du retard diagnostique
habituel (3 ans en moyenne) et de la latence clinique fréquente,
les patients ont presque toujours le temps de constituer une perte
axonale importante pour être significative (perte axonale moyenne :
88 %)
[tableau II]
.
VCS
(m/s)
PAS Amp.
(µV) Ratio d’amplitude
D/G > 2,3***
Sujets pathologiques
(n = 120)
55,5 ± 6 1,97 ± 2,5 114
Les résultats chez les sujets pathologiques montrent clairement que
la vitesse de conduction nerveuse reste normale, le discret ralentisse-
ment (- 4,5 m/s) étant la conséquence exclusive de la perte des fibres
nerveuses de grand diamètre. ◾
Pour en savoir plus…
◾ Benaim LJ, Roche D, Magamon G et al. Apport de l’examen électrique dans les névralgies du fémoro-cutané. In: Deuxièmes
Journées languedociennes d’électromyographie. Montpellier : Ed. Eurand, 1981.
◾ Butler ET, Johnson EW, Kaye ZA. Normal conduction velocity in the lateral femoral cutaneous nerve. Arch Phys Med Rehabil
1974;74:31-2.
◾ Edelson R, Stevens P. Meralgia paresthetica in children. J Bone Joint Surg 1994;76-A:993-9.
◾ Kitchen C, Simpson J. Meralgia paresthetica, a review of 67 patients. Acta Neurol Scand 1972;48:547-55.
◾ Lagueny A, Deliac MM, Deliac P, Durandeau A. Diagnostic and prognostic value of electrophysiologic tests in meralgia paresthe-
tica. Muscle Nerve 1991;14:51-6.
◾ Laroy V, Knoops P, Semoulin P. The lateral femoral cutaneous nerve: nerve conduction technique. J Clin Neurophysiol 1999;16:161-3.
◾ Sarala PK, Nishihara T, Joong S. Meralgia paresthetica: Electrophysiologic study. Arch Phys Med Rehabil 1979;60:30-1.
◾ Seror P. Lateral femoral cutaneous nerve conduction versus somatosensory evoked potentials for meralgia paresthetica elec-
trodiagnosis. Am J Phys Med Rehabil 1999;78:313-6.
◾ Seror P, Seror R. Meralgia paresthetica: clinical and electrophysiological diagnosis in 120 cases). Muscle Nerve 2006;33:650-4.
◾ Seror P. Le nerf fémoro-cutané latéral. In: Les conductions nerveuses. Ed. Elsevier, 2005:143-6.
TEGELINE®: Composition : Immunoglobuline humaine normale 50 mg/ml, saccharose, chlorure de sodium (IgA ≤17 mg/g de protéines, traces de pepsine animale). Poudre et solvant (eau ppi) pour solution pour perfusion. Indications :
•Traitement de substitution : - déficits immunitaires primitifs avec hypogammaglobulinémie ou atteinte fonctionnelle de l’immunité humorale, - infections bactériennes récidivantes chez l’enfant infecté par le VIH, - déficits immunitaires
secondaires de l’immunité humorale, en particulier la leucémie lymphoïde chronique ou le myélome, avec hypogammaglobulinémie et associés à des infections à répétition, l’allogreffe de cellules souches hématopoïétiques avec
hypogammaglobulinémie associée à une infection. •Traitement immunomodulateur : - purpura thrombopénique idiopathique (PTI) chez l’adulte et l’enfant en cas de risque hémorragique important ou avant un acte médical ou chirurgical
pour corriger le taux de plaquettes, - rétinochoroïdite de Birdshot, - syndrome de Guillain et Barré de l’adulte, - neuropathie motrice multifocale (NMM). - polyradiculonévrites inflammatoires démyélinisantes chroniques (PIDC). •Maladie
de Kawasaki. Posologie* : La posologie et l’intervalle entre les administrations dépendent du traitement (substitution ou immunomodulation) et de la demi-vie de l’immunoglobuline humaine normale par voie intraveineuse (IgIV) in vivo
chez les patients atteints de déficit immunitaire. A titre indicatif : • Déficit immunitaire primitif (DIP) : Assurer un taux d’IgG résiduel d’au moins 6 g/l. La persistance des infections peut amener à respecter un seuil d’IgG résiduel de
8 voire 10 g/l. Dose de charge : 0,4 à 0,8 g/kg puis perfusion de 0,2 g/kg toutes les 3 semaines (doses d’IgIV nécessaires : 0,3 g/kg/mois, extrêmes de 0,2 à 0,8 g/kg/mois). Fréquence de perfusion de 15 jours à 1 mois. Perfusions plus
fréquentes si survenue d’infections. Doser les concentrations sériques d’IgG avant chaque perfusion pour contrôler l’activité du traitement et éventuellement ajuster la dose ou l’intervalle d’administration. • Déficit immunitaire secondaire
(DIS) : 0,2 à 0,4 g/kg toutes les 3 à 4 semaines. Le traitement de substitution dans les DIP et DIS peut être effectué à domicile chez les patients préalablement traités par TEGELINE pendant au moins 6 mois en milieu hospitalier sans
apparition d’effet indésirable. L’administration doit être initiée et surveillée par une infirmière ou une personne ayant satisfait à une formation spécifique par l’équipe hospitalière en charge du patient. •PTI:0,8 à 1 g/kg/j à J 1, éventuellement
répété à J 3, ou 0,4 g/kg/j pendant 2 à 5 jours. Peut être renouvelé en cas de réapparition d’une thrombopénie sévère. • Rétinochoroïdite de Birdshot : Posologie initiale de 1,6 g/kg sur 2 à 4 jours toutes les 4 semaines pendant 6 mois.
En entretien : 1,2 g/kg sur 2 à 4 jours, toutes les 4 à 10 semaines. • Syndrome de Guillain et Barré de l’adulte : 0,4 g/kg/j pendant 5 jours. • Neuropathie motrice multifocale (NMM) : Traitement d’attaque : 2 g/kg sur 2 à 5 jours
toutes les 4 semaines pendant 6 mois. En entretien : 2 g/kg sur 2 à 5 jours, intervalle et durée de traitement à adapter au délai individuel de réapparition des symptômes. En l’absence d’effet thérapeutique : arrêt du traitement après
3 mois ou avant 6 mois. • Polyradiculonévrites inflammatoires démyélinisantes chroniques (PIDC) : 2 g/kg sur 5 jours toutes les 4 semaines pendant 4 mois maximum en fonction de la réponse au traitement. L’absence d’effet
thérapeutique devra être évaluée à chaque cure et l’arrêt du traitement devra être envisagé après 3 mois de traitement sans effet. • Maladie de Kawasaki : 1,6 à 2,0 g/kg administrés en plusieurs doses réparties sur 2 à 5 jours ou 2 g/kg
en dose unique, associées à l’acide acétylsalicylique. Mode et voie d’administration* : Administrer par voie IV stricte, en une seule fois, immédiatement après reconstitution. Adapter le débit en fonction de la tolérance clinique, sans
dépasser 1 ml/kg/h pendant la première demi-heure, puis augmenter progressivement sans dépasser 4 ml/kg/h. Ne pas utiliser de solution trouble ou contenant un dépôt. Contre-indications : Hypersensibilité aux Ig, en particulier chez
les patients présentant un déficit en IgA et avec des anticorps circulants anti-IgA. Hypersensibilité connue à l’un des constituants de la préparation. Mises en garde spéciales et précautions particulières d’emploi* : Pour le diagnostic
de NMM : expertise clinique préalable dans un centre de référence labellisé. Pour les PIDC : initiation du traitement après avis d’un centre de référence labellisé. Surveiller attentivement le débit des perfusions. S’assurer initialement de
la tolérance par perfusion lente (1 ml/kg/h). Tenir compte de la teneur en saccharose (2 g/g d’IgG) et du taux de sodium (8 mg/10 ml) en cas de régime hyposodé strict, en cas de diabète latent, de diabète ou de régime hypoglucidique.
Garder les patients sous surveillance pendant toute la durée de la perfusion et les maintenir sous observation pendant au moins 20 min après la fin de la perfusion voire 1 h en cas de première perfusion. Chez les patients présentant un
des facteurs de risque, tels qu’une insuffisance rénale pré-existante, un diabète, une hypovolémie, une obésité, la prise concomitante de médicaments néphrotoxiques ou un âge supérieur à 65 ans, l’administration d’IgIV impose : - une
hydratation correcte avant administration d’IgIV, - de surveiller la diurèse, - de doser la créatininémie, - d’éviter d’associer des diurétiques de l’anse. Chez ces patients à risque, l’utilisation d’IgIV ne contenant pas de saccharose doit être
envisagée. En cas de réactions de type allergique ou anaphylactique, interrompre immédiatement la perfusion. En cas de choc instaurer un traitement symptomatique. Le risque de transmission d’agents infectieux, y compris ceux dont
la nature est encore inconnue, ne peut pas être définitivement exclu lorsque sont administrés des médicaments préparés à partir de sang ou de plasma humain. Ce risque est cependant limité par : - l’entretien médical avec les donneurs
et les contrôles et tests effectués sur chaque don, - la recherche du matériel génomique sur les pools de plasma, - les étapes d’élimination et inactivation virales du procédé, dûment validées. L’efficacité reste limitée vis-à-vis de certains
virus non enveloppés particulièrement résistants. Interactions* : Risque d’entraver l’efficacité des vaccins constitués de virus vivants atténués, attendre au minimum 6 semaines (de préférence 3 mois) avant administration. Augmentation
transitoire de la concentration de divers anticorps transférés (test de Coombs positif transitoirement). Grossesse et allaitement : Administrer chez la femme enceinte qu’en cas de nécessité bien établie. Passage dans le lait maternel.
Effets indésirables* : • Plus fréquents chez les malades atteints de déficits immunitaires primitifs. •Occasionnellement réactions de type frissons-hyperthermie parfois accompagnées de céphalées, nausées, vomissements, manifestations
allergiques, élévation ou chute de la pression artérielle, arthralgies, lombalgies et myalgies modérées. •Risque de réaction anaphylactique plus élevé en cas de perfusion IV rapide chez des patients agammaglobulinémiques avec déficit
en IgA ou hypogammaglobulinémiques qui n’ont jamais reçu d’immunoglobuline ou dont le dernier traitement par Ig IV remonte à plus de 8 semaines. Un débit rapide pourrait même être responsable d’accidents thrombotiques artériels
et veineux plus particulièrement chez le sujet à risque vasculaire. •Rares cas d’hypotension et de chocs anaphylactiques même chez des patients n’ayant pas présenté de réactions d’hypersensibilité lors d’injections antérieures. •Rares
cas de poussées hypertensives isolées. •Rares cas de réactions cutanées surtout eczématiformes, régressives, d’anémie hémolytique et(ou) d’hémolyse régressive, d’élévation de la créatinine et(ou) d’insuffisance rénale aiguë et très
rares cas d’augmentation transitoire des transaminases. •Réaction méningée aseptique, particulièrement chez les patients présentant un PTI, réversible en quelques jours après l’arrêt du traitement. •Rares cas de thrombose en majorité
chez les sujets âgés, et chez les patients présentant des risques d’ischémie cérébrale ou cardiaque, une surcharge pondérale ou atteints d’hypovolémie sévère. •Leuco-neutropénie asymptomatique, de survenue précoce et rapidement
réversible, en particulier chez les patients traités par de fortes doses. Surdosage* : Certains effets dose-dépendants pourraient être favorisés : méningite aseptique, insuffisance rénale, hyperviscosité sanguine. Incompatibilités :
Ne mélanger avec aucun autre produit et(ou) médicament. Conservation : 3 ans à température < 25°C, à l’abri de la lumière. Ne pas congeler. Produit reconstitué : administration immédiate. Titulaire de l’autorisation de mise sur le marché :
LFB BIOMEDICAMENTS - 3, Avenue des Tropiques - B.P. 305 - LES ULIS - 91958 Courtabœuf Cedex - FRANCE. AMM n° 559 899-9 (10 g/200 ml) -559 898-2 (5 g/100 ml) - 559 897-6 (2,5 g/50 ml) - 559 895-3 (0,5 g/10 ml).
JUILLET 1996 / JUILLET 2006. Conditions de prescription et de délivrance : Liste I. Médicament soumis à prescription hospitalière. La prescription par un médecin exerçant dans un établissement de transfusion sanguine autorisé à
dispenser des médicaments aux malades qui y sont traités est également autorisée. Agréé Coll. Indication dans polyradiculonévrites inflammatoires démyélinisantes chroniques (PIDC), agrément Collectivités : demande d'admission à l'étude.
* Pour une information complète, se reporter au Résumé des Caractéristiques du Produit disponible sur le site de l’AFSSAPS http://afssaps.fr/ FEVRIER 2009 - 06G0382/ 8.0
ML TEGELINE 180x130 100309:ML TEGELINE 180x130 6/04/09 17:14 Page 1
1
/
3
100%