Le traitement médicamenteux du diabète de type 2 dossier

Actualités pharmaceutiques
• n° 541 • décembre 2014 •23
Suivi du diabétique de type 2 à l’offi cine
dossier
Mots clés - diabète de type 2; traitement antidiabétique; stratégie thérapeutique
Keywords - anti-diabetic treatment; treatment strategy; type 2 diabetes
© 2014 Elsevier Masson SAS. Tous droits réservés
http://dx.doi.org/10.1016/j.actpha.2014.10.005
Le traitement médicamenteux
du diabète de type 2
L’objectif d’un traitement en diabétologie est de prévenir et de réduire les complications
de la maladie mais aussi d’améliorer la qualité de vie des patients. Actuellement, diverses
classes thérapeutiques permettent de traiter le diabète de type 2. Les médicaments les
plus récents sont particulièrement intéressants en termes de tolérance et de coût.
Pharmacological treatment of type 2 diabetes. The aim of a treatment for diabetes is to prevent
and reduce the complications of the disease as well as improve patients’ quality of life. There
are currently various therapeutic classes of drugs used to treat type 2 diabetes. The most
recent drugs are particularly interesting in terms of tolerance and cost.
© 2014 Elsevier Masson SAS. Tous droits réservés
© 2014 Elsevier Masson SAS. All rights reserved
François PILLONa,*
Pharmacologue
Kimny TANb
Professeur de chimie
thérapeutique
Priscilla JOUTYc
Diététicienne
Yannick FRULLANId
Docteur en pharmacie
*
Auteur correspondant.
Adresse e-mail :
[email protected] (F. Pillon).
a17 bd de Brosses,
21000 Dijon, France
b7 bd Jeanne-d’Arc,
21000 Dijon, France
c1 rue Guynemer,
21600 Longvic, France
d80 rue du Dr-Albert-Barraud,
33000 Bordeaux, France
La prise en charge initiale du diabète de type 2 doit
toujours reposer sur le régime et les modifications
des habitudes de vie avant de recourir aux traite-
ments médicamenteux. Lessulfamides, les biguanides,
les inhibiteurs des alphaglucosidases, les glinides, ainsi
que de nouveaux médicaments tels que les analogues
des glucagon-like peptide-1 (GLP-1), les inhibiteurs du
cotransporteur de la dipeptidyl-peptidase-4 (DPP-4) et
les inhibiteurs de sodium-glucose de type2 (SGLT2)
permettent de traiter le diabète de type 2.
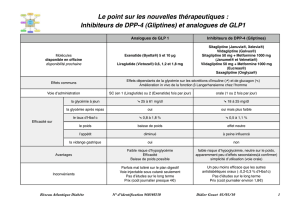
Les nouveaux traitements antidiabétiques disponibles
sur le marché présentent des avantages en termes de
tolérance et de coût par rapport aux traitements plus
anciens. Leurs dossiers d’autorisation de mise sur le
marché (AMM) se réfèrent à plusieurs études cliniques
incluant au moins 2000 patients, dont au moins un tiers
a bénéficié d’un suivi supérieur à un an.
Dans ces essais cliniques, les critères de jugement évaluent:
• les données métaboliquesavec l’équilibre glycémique
moyen (hémoglobine glyquée [HbA1c], variabilité
glycémique, nombre et sévérité des hypoglycémies);
• les complications microvasculairestelles que la
rétino pathie (fond d’œil, rétinographe), la néphropathie
(créatinémie, microalbuminurie des 24heures)et la
neuropathie (examen clinique);
• les complications macrovasculaires (nombre d’évène-
ments cardiovasculaires...).
Les diff érentes classes thérapeutiques
d’antidiabétiques
Parmi les antidiabétiques disponibles (tableau1), sont
distingués les antidiabétiques oraux (biguanides, sulfa-
mides hypoglycémiants, inhibiteurs des alphaglucosi-
dases, glinides, inhibiteurs de la DPP-4, inhibiteurs
deSGLT-2) et les antidiabétiques injectables (analogues
des GLP-1, insuline).
À propos des glitazones,
médicaments retirés du marché
Les glitazones ou thiazolidinediones sont des médica-
ments hypoglycémiants oraux relativement récents qui
ont été retirés du marché en 2011.
La première de ces molécules, la troglitazone, fut commer-
cialisée aux États-Unis en 1997 avant d’être interdite plus
tard en raison de son hépatotoxicité.
De nouveaux médicaments tels que les analogues
des glucagon-like peptide-1 permettent de traiter
le diabète de type 2.
© BSIP/Phototake

Actualités pharmaceutiques
• n° 541 • décembre 2014 •
24
Suivi du diabétique de type 2 à l’offi cine
dossier
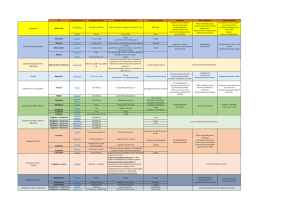
Tableau 1. Caractéristiques des antidiabétiques.
Classe
pharmacologique
Exemple
de molécules
Mécanisme d’action Voie Nombre de prises
par jour
Eff ets
cardiovasculaires
Avantages Inconvénients
Sulfamides
hypoglycémiants
Gliclazide,
glipizide,
glimépiride,
glibenclamide
Augmentation
de la sécrétion
d’insuline
Orale 1 à 2 prises/jour Pas de bénéfi ce
cardiovasculaire
montré dans
les études cliniques
Pas d’effets nocifs
démontrés
Bonne tolérance
Faible coût Hypoglycémie
Augmentation
du poids
Nécessité de surveiller
les glycémies
Initiation du traitement
de manière prudente
(nécessité
d’une titration)
Biguanides Metformine Effet
antihyperglycémiant Orale 1 à 3 fois/jour Réduction
de la morbi-mortalité
cardiovasculaire
(infarctus du myocarde)
dans l’étude clinique
United Kingdom
Prospective Diabetes
Study (UKPDS)
Bonne tolérance
à long terme
Pas de prise
de poids
Faible risque
d’hypoglycémie
Faible coût
Diarrhées +++
Possible lien
avec la survenue
d’une acidose lactique
À éviter en cas
d’insuffi sance rénale
sévère (clairance
de la créatinine
<30 mL/min)
Inhibiteurs
des alpha-
glucosidases
Acarbose,
miglitol Inhibition
des alpha-
glucosidases
intestinales:
diminution
de la dégradation
des carbohydrates
en monosaccharides
absorbables
Orale Jusqu’à 3 fois/jour Inconnu Pas de prise
de poids
Faible coût
Flatulences
Diarrhées
Glinides Répaglinide Stimulation
de la sécrétion
d’insuline
Orale Prise à chaque
repas Pas d’effets bénéfi ques
retrouvés Action
hypoglycémiante
rapide
Prise de poids
à long terme
Hypoglycémie
Nécessité
d’une surveillance
des glycémies
Analogues
du GLP-1
Exénatide,
liraglutide Augmentation
de la sécrétion
d’insuline
et suppression
de la sécrétion
du glucagon
Sous-cutanée 1 à 2 injections/
jour Inconnu
Les études chez
l’animal suggèrent
un effet bénéfi que
sur la survenue
d’un infarctus
du myocarde
et d’une insuffi sance
cardiaque congestive
Pas de prise
de poids
Faible risque
d’hypoglycémie
Pancréatite
Lien avec un cancer
médullaire
de la tyroïde
à confi rmer
À éviter en cas
d’insuffi sance rénale
Inhibiteurs
de la DPP-4
Sitagliptine,
vildagliptine,
saxagliptine
Augmentation
des concentrations
endogènes
d’incrétines
Orale 1 fois/jour Inconnu mais
pas d’évidence
d’effets néfastes
cardiovasculaires
Faible risque
d’hypoglycémie Pancréatite
Inhibiteurs
de SGLT-2
Dapaglifl ozine Réduction
de la réabsorption
du glucose au niveau
du tubule contourné
proximal
Orale 1 fois/jour Inconnu Perte de poids Polyurie
Insuffi sance rénale
fonctionnelle
par déshydratation
Hypotension artérielle
Infections urinaires
Mycoses vaginales
À éviter en cas
d’insuffi sance rénale
modérée à sévère
Insuline Active directement
le récepteur
à l’insuline
Sous-cutanée 1 à 4 injections/
jour en fonction
de la durée d’action
de l’insuline
Pas d’effets néfastes au
niveau cardiovasculaire Bon équilibre
glycémique
comparativement
aux autres
médicaments
Prise de poids
Hypoglycémies
Nécessité
d’une surveillance
des glycémies
DPP-4 : dipeptidyl peptidase-4 ; GLP-1: glucagon-like peptide-1 ; GLT-2 : sodium-glucose de type 2.

Actualités pharmaceutiques
• n° 541 • décembre 2014 •25
Suivi du diabétique de type 2 à l’offi cine
dossier
En France, deux glitazones ont été mises sur le marché
en 2002: la rosiglitazone et la pioglitazone (respective-
ment médicament d’exception jusqu’en 2003 et médi-
cament à prescription initiale restreinte jusqu’en 2004).
Lors de la réévaluation de la pioglitazone en 2008 par la
Commission de transparence, l’amélioration du service
médical rendu (ASMR) est passée de IV à V. Puis, en
septembre 2010, l’Agence européenne du médicament
(EMA) a demandé la suspension des autorisations de
mise sur le marché des médicaments contenant de la
rosiglitazone (Avandia® et Avandamet® en France) suite
aux résultats des réévaluations diligentées par le Comité
européen d’évaluation des médicaments à usage
humain (CHMP) ayant montré qu’elle était, par rapport
à d’autres antidiabétiques oraux, associée à une aug-
mentation du risque d’infarctus du myocarde et d’acci-
dents vasculaires cérébraux. Les bénéfices de la
pioglitazone avaient été initialement montrés sur le
contrôle glycémique, puis secondairement en termes
de morbi-mortalité: réduction de 18% de la survenue
d’un décès, d’un infarctus du myocarde ou d’un acci-
dent vasculaire cérébral. Mais en juillet 2011, ce médi-
cament fut suspendu en France en raison du risque de
survenue d’un cancer de la vessie surtout chez le sujet
de sexe masculin, en cas de durée d’exposition
>24mois, de dose cumulée >28 000 mg et de facteurs
de risque associés (tabagisme, amines aromatiques...).
Deplus, la pioglitazone serait liée à une augmentation
du risque de survenue de fractures, essentiellement
distales, et d’une insuffisance cardiaque.
Metformine et survenue
d’acidose lactique
L’acidose lactique est réputée comme étant la compli-
cation la plus grave du traitement par metformine avec
une mortalité proche de 50%. Son incidence est de
2à9/100 000 patients/an. Ellepeut survenir en cas
d’accumulation de metformine. Les cas rapportés chez
des patients traités par la metformine sont apparus
principalement chez des sujets diabétiques souffrant
d’une insuffisance rénale significative. L’incidence de
l’acidose lactique peut et doit être réduite par une éva-
luation des autres facteurs de risque associés, tels qu’un
diabète mal équilibré, une cétose, un jeûne prolongé,
l’éthylisme, une insuffisance hépatocellulaire, ainsi que
toute affection associée à une hypoxie.
L’acidose lactique est un état, comme son nom l’in-
dique, d’acidose métabolique lié à la libération d’ions H+
par l’acide lactique. Il s’agit d’un accident rare, mais
grave, mortel dans la moitié des cas et dû le plus souvent
à la prescription inappropriée de biguanides.
Le principal mécanisme expliquant le lien entre l’acidose
lactique et la metformine serait l’inhibition de la néo-
glucogenèse à partir de différents substrats, dont le
lactate. La metformine serait aussi capable d’augmenter
la production glycolytique de lactates au niveau intestinal.
Les autres causes d’acidose lactique doivent être prises
en compte dans l’analyse étiologique (état de choc et
autres affections associées à une hypoxie, insuffisance
hépatocellulaire et rénale, diabète mal équilibré, cétose,
jeûne prolongé, éthylisme…).
L’acidose lactique dite “associée à la metformine”
regroupe trois situations distinctes:
• dans le premier cas, il existe une cause sous-jacente
et la présence de la metformine n’est qu’anecdotique;
le pronostic est sombre;
• dans le deuxième cas, la metformine est la cause prin-
cipale de l’acidose lactique et le pronostic est plutôt
favorable;
• dans le dernier cas, le plus fréquent, l’acidose lactique
est aggravée par l’accumulation de metformine; le rôle
de l’insuffisance rénale est alors majeur.
Des acidoses lactiques ont été rapportées chez des
patients traités par metformine et par des médicaments
pouvant altérer la fonction rénale comme les anti-inflam-
matoires non stéroïdiens (AINS), les diurétiques, les
inhibiteurs de l’enzyme de conversion et les antago-
nistes de l’angiotensineII. In fine, toutes les situations à
risque imposent une interruption momentanée de la met-
formine, mais en aucun cas l’arrêt définitif du traitement.
Les inhibiteurs du SGLT-2, une nouvelle
classe d’hypoglycémiants oraux
La dapagliflozine est une nouvelle molécule ayant
obtenu une AMM dans l’Union européenne par
procédure centralisée (Forxiga® 5 et 10 mg, voie orale,
Note
1 Clcr = 140 - âge x poids x k
[Cr]
Clcr: estimation de la
clairance de la créatinine en
mL/min
[Cr]: créatininémie en μmol/L
Âge: âge en année
Poids: masse corporelle en kg
k: coeffi cient qui vaut 1,23
chez l’homme et 1,04 chez la
femme
Côté urinaire
(luminal)
Côté basolatéral
Glucose
Glucose Glucose
Na+
Na+
Na+
K+
K+
Pompe Na+/K+/ATPase
GLUT2
Figure 1. Cellule du tubule rénal proximal présentant, du côté luminal (urinaire), le transporteur
glucose-Na+-SGLT-2 et, du côté basolatéral, le transporteur GLUT-2. Il s’agit d’un transport actif
nécessitant de l’énergie fournie par la pompe Na+/K+/ATPase.
© F. Pillon

Actualités pharmaceutiques
• n° 541 • décembre 2014 •
26
Suivi du diabétique de type 2 à l’offi cine
dossier
1 prise/jour). Ils’agit d’un inhibiteur sélectif et réversible
du co transporteur SGLT-2 au niveau du tube contourné
proximal, diminuant ainsi la réabsorption du glucose, ce
qui provoque une augmentation de son excrétion uri-
naire (figure 1). Dans les essais cliniques, des effets
indésirables sont constatés: infections urinaires et géni-
tales, hypotension, insuffisance rénale fonctionnelle par
déshydratation, nausées, vertiges, etc. L’intérêt de cette
molécule est qu’elle s’attaque à une nouvelle cible (inno-
vante), mais il faudra étudier à long terme ses bénéfices
sur la morbi-mortalité cardiovasculaire et sa tolérance.
Les inhibiteurs de SGLT-2 sont des inhibiteurs compé-
titifs de SGLT-2, transporteur impliqué dans la réabsorp-
tion du glucose dans le tubule rénal proximal. L’action
des inhibiteurs de SGLT-2 ne dépend ni de la présence
d’insuline, ni de la sensibilité à l’insuline du tubule proxi-
mal. Cela permet d’envisager de traiter tous les diabé-
tiques, y compris les diabétiques de type 2 avec
insulinorésistance significative (patients insulinotraités
ou non), qui constituent actuellement la population cible
de cette nouvelle classe thérapeutique. Un sujet sain
filtre quotidiennement 180litres de plasma, soit environ
180 g de glucose par jour. Tant que la glycémie ne
dépasse pas 180mg/dL, la totalité du glucose filtré est
réabsorbée de telle sorte que la glucosurie est nulle.
Cetteréabsorption proximale du glucose est possible
grâce au transporteur SGLT-2 présent du côté de la
lumière du tubule (côté urinaire). Ce transport actif, qui
coûte donc de l’énergie, permet ensuite au glucose de
traverser la cellule tubulaire proximale et d’être excrété
dans la circulation sanguine par le côté basolatéral de
la cellule en échange d’un ion sodium (Na+). Ce transfert
basolatéral est possible grâce au transporteur de
glucose GLUT-2. Le SGLT-2 est donc un transporteur
glucose-Na+. Il existe également une faible réabsorption
du glucose dans une partie plus distale du tubule proxi-
mal par l’intermédiaire de SGLT-1 et GLUT-1. Les inhi-
biteurs de SGLT-2 étant des inhibiteurs compétitifs
sélectifs de SGLT-2, il en résulte une réduction des
capacités de réabsorption du glucose au niveau tubu-
laire proximal qui n’est qu’en partie compensée par le
transporteur SGLT-1.
Les diff érents schémas
thérapeutiques
De façon générale, tous les antidiabétiques oraux (ADO)
sont contre-indiqués ou déconseillés en cas de gros-
sesse ou d’allaitement. Seule la mise en place d’un
schéma insulinique optimisé pour atteindre l’objectif
glycémique strict (HbA1c <6,5%) est recommandée.
F Suite au diagnostic d’un diabète de type 2 ou non
insulinodépendant (DNID), le premier traitement est
un traitement non médicamenteux qui consiste en
l’éducation du patient (réduction pondérale en cas de
surcharge pondérale) avec mise en place de mesures
hygiéno-diététiques (restriction calorique, consomma-
tion de graisses insaturées au détriment des graisses
saturées et consommation d’aliments à faible index
glycémique) et d’exercices physiques réguliers, contrô-
lés et adaptés à chaque individu.
F Le but de cette prise en charge est d’atteindre
l’objectif glycémique cible déterminé [1]:
• cas général: HbA1c≤ 7%;
• patient diabétique de type 2, récemment diagnostiqué
sans antécédent cardiovasculaire et dont l’espérance
de vie est supérieure à 15 ans: HbA1c≤ 6,5%;
• patient âgé:
– “vigoureux”, en bon état de santé, HbA1c≤ 7%;
– “fragile”, à l’état de santé intermédiaire, HbA1c
≤8%;
– “malade”, en mauvais état de santé, HbA1c <9%;
• patient avec un antécédent de complication macro-
vasculaire:
– non évoluée, HbA1c ≤ 7%;
– évoluée, HbA1c ≤ 8%;
• patient insuffisant rénal:
– chronique modéré (débit de filtration glomé rulaire
[DFG en mL/min/1,73 m2] entre 30 et 59),
HbA1c≤7%;
– chronique sévère (DFG entre 15 et 29) ou terminal
(DFG <15), HbA1c ≤ 8%.
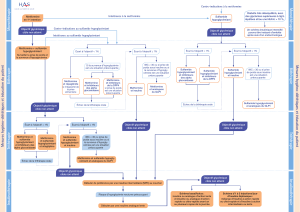
F Si l’objectif glycémique n’est pas atteint malgré la
mise en place de l’éducation du patient avec des
mesures hygiéno-diététiques et des exercices phy-
siques adaptés, un traitement médicamenteux sera mis
en place selon les recommandations de la Haute Auto-
rité de santé (HAS). Les mesures hygiéno-diététiques
devront être poursuivies tout le long de la prise en
charge médicamenteuse. Enl’absence de signes cli-
niques (syndrome polyuro-polydipsique, amaigris-
sement), le traitement sera débuté aux doses minimales
recommandées qui seront augmentées progressive-
ment jusqu’à atteindre l’objectif glycémique ou
jusqu’aux doses maximales tolérées. Le patient doit être
informé des avantages et inconvénients des traitements
proposés.
Monothérapie
F Les biguanides,dont le représentant en France est
la metformine (Glucophage®, Stagid®), sont utilisés en
première intention chez des diabétiques de type 2, en
particulier en cas de surcharge pondérale.
La met formine agit par l’intermédiaire de trois méca-
nismes: en réduisant la production hépatique du glu-
cose, en augmentant la sensibilité des cellules
musculaires à l’insuline et en retardant l’absorption
intestinale du glucose. Ainsi, la prise de ce médicament
n’entraîne pas d’hypoglycémie. La metformine a égale-

Actualités pharmaceutiques
• n° 541 • décembre 2014 •27
Suivi du diabétique de type 2 à l’offi cine
dossier
ment un effet favorable sur le métabolisme lipidique,
enréduisant le cholestérol total, le LDL-cholestérol et le
taux de triglycérides. Laprise de metformine se fait
aucours ou à la fin des repas. À l’instauration du traite-
ment, des perturbations du goût et des troubles gastro-
intestinaux (nausées, vomissements, diarrhées,
douleurs abdominales et perte d’appétit) peuvent appa-
raître, mais régressent spontanément dans la plupart
des cas.
F Un sulfamide hypoglycémiant est recommandé
(glibenclamide [Daonil®, Hémi-Daonil®], gliclazide [Dia-
micron®], glimépiride [Amarel®], glipizide [Glibénèse®,
Ozidia®]) en cas d’intolérance ou de contre-indication à
la metformine. Les sulfamides hypoglycémiants agis-
sent en stimulant les cellules bêta des îlots de Lange-
rhans qui sécrètent ainsi davantage d’insuline.
Parconséquent, il est important d’apprendre au patient
à prévenir, identifier et prendre en charge une hypo-
glycémie. Lemédicament doit être pris avant les princi-
paux repas (jamais en l’absence de repas)
F Un hypoglycémiant non sulfamidé ou un inhibiteur
des alphaglucosidases intestinales est conseillé en
cas d’intolérance ou de contre-indication à la metformine
et aux sulfamides hypoglycémiants. L’administration de
l’hypoglycémiant non sulfamidé, insulinosécréteur
(répaglinide [NovoNorm®]), se fait environ 15 à
30minutes avant chaque repas (jamais en l’absence de
prise alimentaire). Son action est rapide et l’effet hypo-
glycémiant dure tout au long du repas. La forte concen-
tration d’insuline ne persiste pas au-delà de la
stimulation liée au repas. Un inhibiteur des alphagluco-
sidases intestinales (acarbose [Glucor®]; miglitol
[Dia stobol®]) doit être pris au début des repas si la
survenue d’hypoglycémies est une situation préoccu-
pante. Cesmolécules diminuent la dégradation des
carbo hydrates et ainsi l’hyperglycémie postprandiale
sans entraîner d’hyperinsulinémie. Enraison de leurs
effets indésirables digestifs (flatulence, diarrhées,
douleurs gastro-intestinales et abdominales), ils ne doi-
vent pas être prescrits en cas de troubles de la digestion,
de l’absorption ou de maladies inflammatoires chro-
niques de l’intestin.
Bithérapie
F L’association metformine + sulfamide hypo-
glycémiant est recommandée si l’objectif glycémique
n’est pas atteint malgré la monothérapie et la poursuite
des mesures hygiéno-diététiques et des exercices phy-
siques adaptés, en surveillant la prise de poids et la
survenue d’hypoglycémies.
F En cas d’intolérance ou de contre-indication aux
sulfamides hypoglycémiants, il est recommandé:
• soit une association metformine + répaglinide;
• soit une association metformine + acarbose ou migli-
tol, si la survenue d’hypoglycémies est une situation
préoccupante;
• soit une association metformine + inhibiteur de la
DPP-4 (famille des gliptines, encadré 1) si la survenue
d’hypoglycémies ou la prise de poids sont préoccu-
pantes (saxagliptine [Onglyza®], 5 mg/jour; sitagliptine
[Januvia®, Xelevia®], 100 mg/jour; vildagliptine
[ Galvus®], 100 mg/jour en deux prises, soit 50 mg le
matin et 50 mg le soir, la prise étant indépendante des
repas);
• soit une association metformine + analogue du GLP-1
(encadré 1) en solution injectable sous-cutanée (exé-
natide [Byetta®], deux injections/jour une heure avant
les deux principaux repas, espacées de six heures
minimum; liraglutide [Victoza®], une injection/jour
indépendamment des repas) si l’indice de masse cor-
porelle (IMC) est supérieur ou égal à 30.
F En cas d’intolérance ou de contre-indication à la
metformine sera conseillée:
• soit une association sulfamide hypoglycémiant +
acarbose ou miglitol (en cas d’hypoglycémie provo-
quée par le sulfamide, un sucrage au glucose est
nécessaire);
• soit une association sulfamide hypoglycémiant + inhibi-
teur de la DPP-4 (pour la vildagliptine, 50mg/jour le
matin);
• soit une association sulfamide hypoglycémiant + ana-
logue du GLP-1, en cas d’IMC ≥ 30.
Trithérapie
F Si l’objectif glycémique n’est pas atteint malgré
la bithérapie et la poursuite des mesures hygiéno-
diététiques et des exercices physiques adaptés,
ilfaudra s’orienter vers:
• soit l’association metformine + sulfamide hypoglycé-
miant + acarbose ou miglitol (en cas d’hypoglycémie
provoquée par le sulfamide, un sucrage au glucose
est nécessaire);
Encadré 1. À savoir
F La famille des gliptines inhibe la principale enzyme DPP-4
(dipeptidyl peptidase-4) qui détruit, entre autres, le GLP-1 physio-
logique (glucagon-like peptide-1 ou incrétine physiologique),
prolongeant ainsi la durée de vie de ce dernier.
F Le GLP-1 est le plus puissant stimulant de la sécrétion
d’insuline par des cellules bêta du pancréas. Pour contrer l’action
destructrice de la DPP-4 sur le GLP-1, une autre famille de molé-
cules synthétiques est proposée, il s’agit des analogues du GLP-1,
les incrétinomimétiques, résistants à l’action de la DPP-4, ago-
nistes des récepteurs GLP-1, utilisés en solution injectable
sous-cutanée.
 6
6
1
/
6
100%