Télécharger le poster (PDF)

Interet de l'angio scanner dans
l'exploration des atrésies
pulmonaires à septum ouvert
Hôpital la Rabta.
TUNIS - TUNISIE
Correspondance: Dr Habiba MIZOUNI

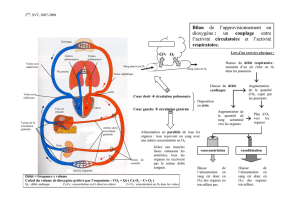
L’atrésie pulmonaire à septum ouvert APSO est une forme
extrême de tétralogie de Fallot avec sténose sévère de la
voie pulmonaire
Définition et physiopathologie
……….Hypertrophie ventriculaire droite
…………….CIV
………..Sténose de la voie pulmonaire
…….Glissement à droite et en avant de l’aorte
…..Développement de collatérales

Conséquences: Développement d’une
circulation de suppléance systémico-
pulmonaire :
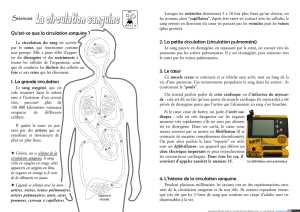
9
Persistance du canal artériel
.
Persistance du canal artériel
.
9Artères collatérales aorto-pulmonaires. MAPCAs: Major
aorto pulmonary collateral Arteries.
9Autres artères de suppléance mineures d’origine
bronchique, intercostale ou diaphragmatique

CLASSIFICATION
La classification des APSO en 3 types est basée sur la
cartographie vasculaire pulmonaire:
Type A: Les artères pulmonaires natives sont présentes et sont
suppliées par la persistance du canal artériel
Type B:
Type B:
les artères segmentaires naissent des artères pulmonaires
et des MAPCAs
Type C: les artères segmentaires naissent exclusivement des
MAPCAs
Tchervenkov CI, Roy, N. Congenital Heart Surgery Nomenclature and Database
Project: pulmonary atresia—ventricular septal defect.
Ann Thorac Surg 2000;
69[4 suppl]:S97–S105

Le traitement chirurgical dépend de la morphologie
des artères pulmonaires
Si les artères pulmonaires sont développées:
fermeture de la CIV, rétablissement de la continuité
entre le VD et l’AP et mise d’un tube prothétique.
Traitements chirurgicaux
entre le VD et l’AP et mise d’un tube prothétique.
Dans le cas ou les artères pulmonaires sont très
hypoplasiques et la circulation pulmonaire est
assurée par les MAPCAs:
Chirurgie palliative, dans l’espoir d’une cure complète ultérieure
Les objectifs étant le plus souvent d’augmenter le débit
pulmonaire par des anastomoses et de reconstruire un arbre
artériel en réimplantant les MAPCAs sur les branches artérielles:
Unifocalisation
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
1
/
47
100%