Le cancer bronchopulmonaire en France : quels changements en 10 ans ?

Le cancer bronchopulmonaire
en France : quels changements
en 10 ans ?
Lung cancer in France: what changes in 10 years?
C. Locher*, D. Debieuvre**, G. Leveiller***, J.Y. Le Tinier****, C. Bernier*****,
F. Blanchon*, M. Grivaux*
* Service de pneumologie, hôpital de Meaux. ** Service de pneumologie, hôpital général, Mulhouse.
*** Service de pneumologie, hôpital de Saint-Brieuc. **** Service de pneumologie, centre médical de Bligny,
Briis-sous-Forges. ***** Service de pneumologie, hôpital de Dinan.
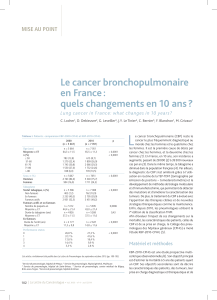
Tableau I. Patients : comparaison KBP-2000-CPHG et KBP-2010-CPHG.
2000
(n = 5667)
2010
(n = 7051)
p
Âge (ans)
Moyenne ± ET
n (%)
≤ 50
51-60
61-70
71-80
> 80
n = 5664
64,3 ± 11,5
783 (13,8)
1270 (22,4)
1743 (30,8)
1530 (27,0)
338 (6,0)
n = 7051
65,5 ± 11,3
615 (8,7)
1899 (26,9)
2066 (29,3)
1732 (24,6)
739 (10,5)
< 0,0001
< 0,0001
Sexe, n (%)
Hommes
Femmes
n = 5 667
4763 (84,0)
904 (16,0)
n = 7051
5340 (75,7)
1711 (24,3)
< 0,0001
Tabagisme
Statut tabagique, n (%)
Non-fumeurs
Ex-fumeurs
Fumeurs actifs
Fumeurs actifs et ex-fumeurs
Nombre de paquets-an
Moyenne ± ET
Durée du tabagisme (ans)
Moyenne ± ET
Ex-fumeurs
Durée de l’arrêt (ans)
Moyenne ± ET
n = 5586
402 (7,2)
2253 (40,3)
2931 (52,5)
n = 5112
44,4 ± 21,4
n = 4 926
37,3 ± 11,5
n = 2177
11,3 ± 9,8
n = 7008
762 (10,9)
2795 (39,9)
3451 (49,2)
n = 5 945
43,0 ± 21,4
n = 5 268
37,5 ± 11,6
n = 2647
14,8 ± 11,6
< 0,0001
0,0006
0,43
< 0,0001
Performance status
0
1
2
3
4
26,8%
37,7%
17,8%
14,4%
3,3%
27,3%
41,6%
18,4%
9,9%
2,8%
<0,0001
L
e cancer bronchopulmonaire (CBP) reste le cancer
le plus fréquemment diagnostiqué au monde chez
les hommes et le quatrième chez les femmes.
Il est la première cause de décès par cancer chez les
hommes, et la deuxième chez les femmes (1). En France,
en 10 ans, son incidence a augmenté, passant de
28 000 (2) à 39 500 nouveaux cas par an (3). Dans le
même temps, le tabagisme a diminué dans la popu-
lation française (4). Par ailleurs, le diagnostic du CBP
s’est amélioré grâce à l’utilisation en routine de la
TEP-TDM (tomographie par émission de positons −
tomodensitométrie) et le développement de méthodes
de biologie moléculaire et d’immuno histochimie, qui
permettent de détecter des mutations et d’améliorer
la caractérisation des tumeurs. De plus, le traitement
du CBP a évolué avec l’apparition des thérapies ciblées
et de nouvelles stratégies thérapeutiques comme la
maintenance. Enfin, depuis 2010, les pneumologues
utilisent la 7e édition de la classification TNM.
Afin d’évaluer l’impact de ces changements sur la
mortalité, les caractéristiques des patients, celles du
CBP et de sa prise en charge, le Collège des pneu-
mologues des hôpitaux généraux (CPHG) a mené
l’étude KBP-2010-CPHG (5).
Matériel et méthodes
KBP-2010-CPHG est une étude prospective multi-
centrique observationnelle (6). Son objectif principal
est d’estimer la mortalité à 5 ans des patients ayant
un CBP. Ses objectifs secondaires sont de décrire
les caractéristiques des patients, des tumeurs, leur
La Lettre du Pneumologue • Vol. XVI - n° 5 - septembre-octobre 2013 | 189
ONCO-PNEUMOLOGIE
LPN5 septembre-octobre 2013.indd 189 25/10/13 09:48

»
L’étude KBP-2010-CPHG est une étude prospective observationnelle conduite sur 7 051patients dans
104services de pneumologie des hôpitaux généraux français.
»Elle montre qu’en 10ans les caractéristiques du cancer bronchopulmonaire (CBP) primitif ont changé,
avec principalement une augmentation de l’âge des patients, de la proportion des femmes, des non-fumeurs,
des adénocarcinomes et des tumeurs de stade IV.
»
L’augmentation des adénocarcinomes est indépendante du sexe, de l’âge et du statut tabagique, confir-
mant l’évolution histologique du CBP.
»Il existe également une amélioration de la survie à 1 an, essentiellement dans les cancers bronchiques
non à petites cellules (CBNPC).
Mots-clés
Adénocarcinome
Cancer
bronchopulmonaire
Épidémiologie
Mortalité
Highlights
»
The KBP-2010-CPHG prospec-
tive observational study was
conducted on 7,051patients in
the respiratory departments of
104 French general hospitals.
»
The study showed that the
characteristics of the primary
lung cancer have changed in
10years, with increases notably in
patient age, and the percentages
of women, non-smokers, adeno-
carcinoma and stage IV tumours.
»
The increase in the number of
adenocarcinomas was indepen-
dent of sex, age and smoking
status, confirming changes in
lung cancer histology.
»
The study also showed
improved 1-year survival, mainly
in non-small-cell lung cancer.
Keywords
Adenocarcinoma
Epidemiology
Lung cancer
Mortality
prise en charge diagnostique et thérapeutique et de
comparer ces caractéristiques à celles d’une étude
similaire réalisée en 2000, KBP-2000-CPHG (7).
La survie à 1, 4 et 5 ans sera également évaluée et
comparée à celle rapportée en 2000.
Tous les pneumologues membres du CPHG ont été
contactés par courrier afin d’être investigateurs pour
l’étude. Ils devaient inclure consécutivement tous les
patients consentants (accord oral), âgés de plus de
18 ans, avec un CBP primitif diagnostiqué histologi-
quement ou cytologiquement entre le 1
er
janvier et
le 31 décembre 2010 et suivis dans le centre investi-
gateur. Pour chaque patient inclus, un questionnaire
anonyme était rempli, comprenant des questions
sur les caractéristiques du patient, de sa tumeur et
de sa prise en charge thérapeutique. Le statut vital
du patient à 1 an était recherché en interrogeant
l’investigateur ou la mairie de naissance du patient.
Résultats
En 2010, 119 centres ont accepté de participer à
l’étude et ont inclus 7 610 patients. Quinze centres
et 559 patients (7,3 %) ont été exclus en raison de
déviations majeures ou d’un manque d’exhausti-
vité dans les inclusions. Finalement, l’analyse a été
effectuée sur 7 051 patients issus de 104 centres.
Les principales caractéristiques des patients et de
leurs tumeurs sont présentées dans les tableaux I
p. 189, II et III. Elles sont comparées à celles de
2000. La survie à 1 an était de 43,6 % en 2010 versus
38,2 % en 2000 (figure 1, tableau IV p. 193).
Discussion
La comparaison des résultats des 2 études KBP-
2000-CPHG et KBP-2010-CPHG montre que, en
10 ans, la proportion de femmes et de non-fumeurs
a augmenté chez les patients ayant un CBP primitif,
que l’adénocarcinome est devenu le type histo-
logique le plus fréquent, que l’âge des patients au
moment du diagnostic a augmenté et que le CBP
continue à être diagnostiqué tardivement à un stade
avancé.
La conception similaire des 2 études KBP-
2000-CPHG et KBP-2010-CPHG, la taille et la
composition des 2 cohortes ont permis de faire une
description et une comparaison représentatives du
CBP en France. Dans les centres hospitaliers géné-
raux (CHG), environ 200 services de pneumologie
prennent en charge les CBP. Dans les études de
2000 et de 2010, environ la moitié des services de
pneumologie des CHG ont inclus près de 20 % des
nouveaux cas de CBP diagnostiqués en France et
plus de la moitié des nouveaux cas diagnostiqués
et suivis dans les CHG (7, 8). La répartition géogra-
phique des centres participants (figure 2, p. 192)
suggère que le recrutement était représentatif des
services de pneumologie des CHG sur l’ensemble
du territoire français. L’exhaustivité des inclusions
et de la collecte des données a été vérifiée par le
comité de pilotage de l’étude. Le schéma de l’étude
permettait d’assurer une collecte des données de
bonne qualité, avec un seul formulaire à remplir au
moment du diagnostic, et un nombre de questions
limité. La qualité de la collecte des données a été
renforcée par l’expérience des enquêteurs, puisque
80 centres ont participé aux 2 études.
Les patients avec un CBP étaient en moyenne plus
âgés en 2010 qu’en 2000, avec un âge moyen au
moment du diagnostic de 65,5 versus 64,3 ans
respectivement (p < 0,0001). Cette évolution est
Tableau II. Tumeurs : comparaison KBP-2000-CPHG et KBP-2010-CPHG.
2000
(n = 5667)
2010
(n = 7051)
p
Histologie*, n (%)
Cancer à petites cellules
Carcinome épidermoïde
Adénocarcinome
Carcinome à grandes cellules
Bronchiolo-alvéolaire
Autre
Combinaison de plusieurs types
n = 5650
930 (16,5)
2193 (38,8)
1640 (29,0)
667 (11,8)
44 (0,8)
88 (1,6)
88 (1,6)
n = 7051
950 (13,5)
1852 (26,3)
3199 (45,4)
754 (10,7)
59 (0,8)
148 (2,1)
89 (1,3)
<0,0001
Stade**, n (%)
0
IA
IB
IIA
IIB
IIIA
IIIB
IV
n = 4411***
22 (0,5)
210 (4,8)
432 (9,8)
35 (0,8)
311 (7,1)
623 (14,1)
899 (20,4)
1879 (42,6)
n = 6046****
11 (0,2)
355 (5,9)
252 (4,2)
253 (4,2)
230 (3,8)
846 (14,0)
574 (9,5)
3524 (58,3)
<0,0001
* 1 seule variable ; ** cancer bronchopulmonaire non à petites cellules uniquement ; *** TNM 6eédi-
tion ; **** TNM 7e édition.
190 | La Lettre du Pneumologue • Vol. XVI - n° 5 - septembre-octobre 2013
Points forts
LPN5 septembre-octobre 2013.indd 190 25/10/13 09:48

Tableau III. Risque d’adénocarcinome chez les patients avec un cancer bronchopulmonaire
non à petites cellules.
Risque relatif IC95 p
Modèle univarié
KBP-2000-CPHG
KBP-2010-CPHG
1
2,07 (1,92-2,24) < 0,0001
Modèle multivarié*
KBP-2000-CPHG
KBP-2010-CPHG
1
2,06 (1,90-2,23) < 0,0001
* Ajustement sur l’âge, le sexe et le tabagisme.
Figure 1. Survie à 1 an.
Cohorte
KBP-2000-CPHG
(n = 5 667)
Cohorte
KBP-2010-CPHG
(n = 7 051)
Perdus de vue
(n = 100) [1,8 %]
Perdus de vue
(n = 70) [1,0 %]
Décédés avant 1 an
(61,8 %)
Décédés avant 1 an
(56,4 %)
Statut vital connu
à 1 an
(n = 5 567) [98,2 %]
Statut vital connu
à 1 an
(n = 6 981) [99,0 %]
Vivants à 1 an
(38,2 %)
Vivants à 1 an
(43,6 %)
La Lettre du Pneumologue • Vol. XVI - n° 5 - septembre-octobre 2013 | 191
ONCO-PNEUMOLOGIE
due à la fois à une plus faible proportion de patients
jeunes (≤ 50 ans : 8,7 versus 13,8 %, respectivement)
et à une proportion plus élevée de patients très âgés
(> 80 ans : 10,5 versus 6 %, respectivement). L’aug-
mentation du nombre de patients âgés s’explique
en partie par l’augmentation de l’espérance de vie,
mais aussi par une plus grande prise en charge des
patients âgés, qui sont de plus en plus demandeurs
de diagnostic, de soins et de traitements.
La proportion de femmes suivies pour un CBP
est passée de 16,0 % en 2000 à 24,3 % en 2010
(p < 0,0001), confirmant une tendance observée
depuis plusieurs années en France, en Europe, et
dans la plupart des pays dans le monde (9-11). En
France, depuis les années 1990, l’incidence du CBP
s’est stabilisée chez les hommes (taux mondial
standard : 52 pour 100 000 personnes-années) alors
qu’elle a presque doublé chez les femmes (9,7 pour
100 000 personnes-années en 2000 versus 17,8 en
2010) [4, 12]. Cette différence est probablement
liée à l’évolution différente du tabagisme chez
les hommes et les femmes. Chez les hommes, le
tabagisme diminue depuis 1995, alors que chez les
femmes, il n’a commencé à diminuer que depuis
2005 (13). Cependant, le vieillissement de la popu-
lation et la plus grande espérance de vie des femmes
par rapport aux hommes peuvent aussi contribuer
à cette augmentation de la proportion de femmes
atteintes de CBP.
Le pourcentage de personnes n’ayant jamais
fumé est passé de 7,2 % en 2000 à 10,9 % en 2010
(p < 0,0001). En fait, ces chiffres reflètent principale-
ment une augmentation du pourcentage d’hommes
non fumeurs (4,7 % en 2010 versus 2,5 % en 2000,
p < 0,0001) alors que le pourcentage de femmes non
fumeuses est stable (34,2 % en 2010 versus 36,1 %
en 2000, p = 0,32). Le tabagisme reste la première
cause de CBP : quelqu’un qui a fumé toute sa vie a
un risque de CBP au moins 20 fois supérieur à une
personne qui n’a jamais fumé (14). Cependant, dans
la littérature, le CBP du non-fumeur est évalué à
10 % à 25 % des CBP (15) et est aujourd’hui consi-
déré comme une entité en soi. Il prédomine chez les
femmes et se présente généralement sous la forme
d’un adénocarcinome. Plusieurs facteurs seraient
incriminés dans cette augmentation : le tabagisme
passif, les facteurs environnementaux tels que l’ex-
position au radon dans les pays industrialisés, la
pollution intérieure due à la combustion du charbon,
de la biomasse ou des fumées d’huile de cuisson
dans les pays pauvres, l’exposition professionnelle
à l’amiante, l’arsenic, la silice ou les pesticides,
l’exposition à la pollution extérieure (notamment
les microparticules des gaz d’échappement des véhi-
cules à moteur Diesel classés parmi les carcinogènes
par l’Organisation mondiale de la santé [OMS] en
2012), et les maladies pulmonaires préexistantes
comme la tuberculose ou l’emphysème, avec ou sans
maladie pulmonaire obstructive chronique associée.
Les facteurs liés à l’alimentation, tels que l’obésité,
ou, inversement, l’action protectrice des fruits et
des légumes ont également été mentionnés. Dans la
présente étude, 158 des 762 patients n’ayant jamais
fumé (20,7 %) ont déclaré avoir été exposés à un
tabagisme passif.
Le diagnostic du CBP demeure tardif. Le taux de
tumeurs de stade IV est passé de 42,6 % en 2000
à 58,3 % en 2010. Cependant, cette augmentation
est probablement, en partie, le résultat de plusieurs
biais. En effet, dans la nouvelle classification TNM (7e
édition) des CBP mise en place en 2010, les atteintes
pleurales et péricardiques sont classées M1a, et donc
stade IV, alors qu’elles étaient classées T4, et donc
stade IIIB, dans l’édition précédente utilisée en 2000.
En outre, le TEP-TDM, désormais utilisé en routine,
améliore la détection des métastases. Des recom-
mandations françaises sur son utilisation ont d’ail-
leurs été publiées entre 2000 et 2010 (16). En outre,
les changements des caractéristiques histologiques
LPN5 septembre-octobre 2013.indd 191 25/10/13 09:48

Figure 2. Répartition géographique des centres d’études.
192 | La Lettre du Pneumologue • Vol. XVI - n° 5 - septembre-octobre 2013
ONCO-PNEUMOLOGIE Le cancer bronchopulmonaire en France : quels changements en 10ans ?
du CBP peuvent entraîner une apparition plus tardive
des premiers symptômes et une évolution plus rapide
de la tumeur liée à une plus grande agressivité de la
maladie. Enfin, la répartition géographique inégale
des médecins, rapportée au cours des dernières
années en France, a peut-être conduit à retarder
certains diagnostics.
Le changement le plus remarquable constaté entre
2000 et 2010 est l’augmentation du pourcentage
d’adénocarcinomes (29,0 versus 45,4 %, respecti-
vement, p < 0,0001), comparativement aux carci-
nomes épidermoïdes (38,8 versus 26,3 %). Cette
évolution histologique du CBP a déjà été rapportée
dans plusieurs pays (9, 11, 17). L’adénocarcinome
est la forme histologique la plus fréquente chez
les femmes, qu’elles aient fumé ou non, et chez
les hommes n’ayant jamais fumé (18). Cependant,
l’augmentation du pourcentage d’adénocarcinomes
entre 2000 et 2010 n’est pas seulement due à l’aug-
mentation de la proportion de femmes et d’hommes
n’ayant jamais fumé. En effet, il existe une augmen-
tation du risque d’adénocarcinome indépendam-
ment du sexe, du statut tabagique ou de l’âge
(OR = 2,06 [1,90 à 2,23], p < 0,0001) [tableau III,
p. 191]. D’autres facteurs sont donc impliqués dans
cette évolution de l’histologie. Certains auteurs
mettent en cause des changements dans la fabri-
cation des cigarettes (utilisation de filtres et chan-
gements de composition) et donc dans la fumée
inhalée : le taux de nicotine et de goudron a diminué
alors que les concentrations en composés nitrés ont
augmenté. La diminution de la teneur en nicotine
peut conduire le fumeur à inhaler plus profondé-
ment, ce qui augmente l’exposition du poumon
périphérique aux oncogènes et donc l’apparition
préférentielle d’adéno carcinomes. La réduction de
la consommation de cigarettes, observée chez les
fumeurs et ex-fumeurs en 10 ans, et l’augmentation
de l’intervalle entre le sevrage tabagique et l’appari-
tion du CBP suggèrent que d’autres oncogènes ayant
un temps d’action plus long peuvent également être
impliqués. La baisse de l’âge à la première cigarette
LPN5 septembre-octobre 2013.indd 192 25/10/13 09:48

Tableau IV. Survie à 1 an en fonction du type de cancer.
2000 2010 p
Tous cancers 38,2 43,6 <0,01
Cancers à petites cellules 33,1 35,8 0,44
Cancers non à petites cellules 39,3 44,8 <0,01
La Lettre du Pneumologue • Vol. XVI - n° 5 - septembre-octobre 2013 | 193
ONCO-PNEUMOLOGIE
(surtout chez les femmes) peut également jouer un
rôle. Enfin, l’utilisation de marqueurs immunohisto-
chimiques plus spécifiques (TTF1, P63, CK5-6) par les
pathologistes pourrait participer à l’augmentation du
pourcentage d’adénocarcinomes en 2010 (19, 20).
L’autre résultat marquant de cette comparaison est
l’amélioration de la survie à 1 an, qui est passée de
façon significative de 38,2 % en 2000 à 43,6 % en
2010 (p < 0,01) [tableau IV]. Cette amélioration ne
concerne que les CBNPC. On pourrait conclure un
peu rapidement qu’elle est liée à une meilleure prise
en charge thérapeutique des patients ; cependant,
elle peut également être le résultat des modifications
des caractéristiques épidémiologiques des patients
et de leurs tumeurs. Des analyses statistiques
complémentaires sont en cours pour assurer une
interprétation correcte de ce résultat. Par ailleurs, il
sera intéressant de vérifier si cette amélioration de
la survie des patients atteints de CBP se confirme
avec l’analyse de la survie à 4 et à 5 ans planifiée
dans l’étude.
Conclusion
Au cours des 10 dernières années, en France, le
profil du CBP a évolué avec un plus grand nombre
d’adénocarcinomes, de femmes, de non-fumeurs,
de tumeurs de stade IV et des patients plus âgés.
L’augmentation du risque d’adénocarcinome est indé-
pendante du sexe, de l’âge et du statut tabagique
des patients. Ces résultats confirment l’intérêt du
ciblage des femmes dans les campagnes antitabac,
de la recherche de nouvelles substances oncogènes
et du débat autour du dépistage du CBP. La survie
à 1 an des patients atteints de CBP s’est améliorée,
mais ce résultat doit être interprété avec prudence et
nécessite des analyses statistiques complémentaires
pour en déterminer les causes. ■
Liens d’intérêts
Cette étude a été promue par le Collège des pneumologues des
hôpitaux généraux (CPHG) avec l’aide du fonds de dotation de
recherche en santé respiratoire. Elle a été financée par AstraZeneca,
Boehringer Ingelheim, Chugai, GlaxoSmithKline, Lilly France, Pierre
Fabre Oncologie, Pfizer, Pneumologie Développement, Roche et
Sanofi-Aventis. Les sponsors de l’étude n’ont pas été impliqués
dans la conception de l’étude, la collecte de données, l’analyse des
données, l’interprétation des données, la rédaction de rapports, ou
la décision de soumettre pour publication. Les auteurs n’ont pas
de relation financière et personnelle avec d’autres personnes ou
organisations qui pourraient biaiser ce travail.
Remerciements
Les auteurs tiennent à remercier
tous les membres du comité
scientifique et tous les pneumo-
logues qui ont activement
participé à cette étude.
Ils remercient égale-
ment MargauxOrange et
FabiennePéretz pour leur aide
dans la gestion de l’étude et
laprépa ration de cet article.
1. Jemal A, Bray F, Center M, Ferlay J, Ward E, Forman D.
Global cancer statistics. CA Cancer J Clin 2011;61(2):69-90.
2. Molinié F, Velten M, Remontet L, Bercelli P, et le réseau
FRANCIM. Évolution de l’incidence du cancer broncho-
pulmonaire en France (1978-2000). Rev Mal Respir
2006;23(2 Pt 1):127-34.
3. Institut de veille sanitaire (InVS). Projections de l’incidence
et de la mortalité par cancer en France en 2010. http://
www.invs.sante.fr/applications/cancers/projections2010
4. Institut national du cancer (INCa). Actions de lutte contre
le tabagisme. http://lesdonnees.e-cancer.fr/les-fiches-de-
synthese/3-facteurs-risque/41-tabac/69-actions-lutte-
contre-tabagisme.html
5. Locher C, Debieuvre D, Coëtmeur D et al. Major changes
in lung cancer over the last ten years in France: The KBP-
CPHG studies. Lung Cancer 2013;81(1):32-8.
6. Grivaux M, Locher C, Bombaron P et al. Étude KBP-
2010-CPHG : recueil des nouveaux cas de cancer bron-
chopulmonaire primitif diagnostiqués dans les services de
pneumologie des centres hospitaliers généraux du 1er janvier
au 31 décembre 2010. Rev Pneumol Clin 2010;66(6):375-82.
7. Blanchon F, Grivaux M, Collon T et al. Épidémiologie
du cancer bronchique primitif pris en charge dans les
centres hospitaliers généraux français. Rev Mal Respir
2002;19(6):727-34.
8. INCa. La situation du cancer en France en 2010. Boulogne-
Billancourt : InCA, collection Rapports et synthèses, 2010,
288 p.
9. Montesinos J, Bare M, Dalmau E et al. The changing
pattern of non-small cell lung cancer between the 90 and
2000 decades. Open Respir Med J 2011;5:24-30.
10. International Agency for Research on Cancer (IARC).
Globocan 2008. Lung cancer incidence and mortality
worldwide in 2008. http://globocan.iarc.fr/factsheets/
cancers/lung.asp
11. Jiang X, de Groh M, Liu S, Liang H, Morrison H. Rising
incidence of adenocarcinoma of the lung in Canada. Lung
Cancer 2012;78(1):16-22.
12. Belot A, Grosclaude P, Bossard N et al. Cancer incidence
and mortality in France over the period 1980-2005. Rev
Epidemiol Santé Publique 2008;56(3):159-75.
13. InVS. Numéro thématique - Journée mondiale sans tabac,
31 mai 2010]. Bull Epidemiol Hebd 2010;19-20:209-24.
14. Tyczynski JE, Bray F, Parkin DM. Lung cancer in Europe
in 2000: epidemiology, prevention, and early detection.
Lancet Oncol 2003;4(1):45-55.
15. Fitting JW. Lung cancer among non-smokers. Int J Tuberc
Lung Dis 2012;16(4):429.
16. Bourguet P, Groupe de travail SOR. Recommandations
pour la pratique clinique : standards, options et recomman-
dations 2003 pour l’utilisation de la tomographie par émis-
sion de positons au 18F-FDG (TEP-FDG) en cancérologie
(rapport intégral). Bull Cancer 2003;90(Spec No):S5-17.
17. Wynder EL, Muscat JE. The changing epidemiology of
smoking and lung cancer histology. Environ Health Perspect
1995;103(Suppl 8):143-8.
18. Samet JM, Avila-Tang E, Boffetta P et al. Lung cancer in
never smokers: clinical epidemiology and environmental risk
factors. Clin Cancer Res 2009;15(18):5626-45.
19. Travis WD, Brambilla E, Noguchi M et al. International
association for the study of lung cancer/American thoracic
society/European respiratory society international multi-
disciplinary classification of lung adenocarcinoma. J Thorac
Oncol 2011;6(2):244-85.
20. Nicholson AG, Gonzalez D, Shah P et al. Refining the
diagnosis and EGFR status of non-small cell lung carcinoma
in biopsy and cytologic material, using a panel of mucin stai-
ning, TTF-1, cytokeratin 5/6, and P63, and EGFR mutation
analysis. J Thorac Oncol 2010;5(4):436-41.
Références bibliographiques
LPN5 septembre-octobre 2013.indd 193 25/10/13 09:48
1
/
5
100%