A Réunion de l’Amicale des cardiologues de Paris I
publicité
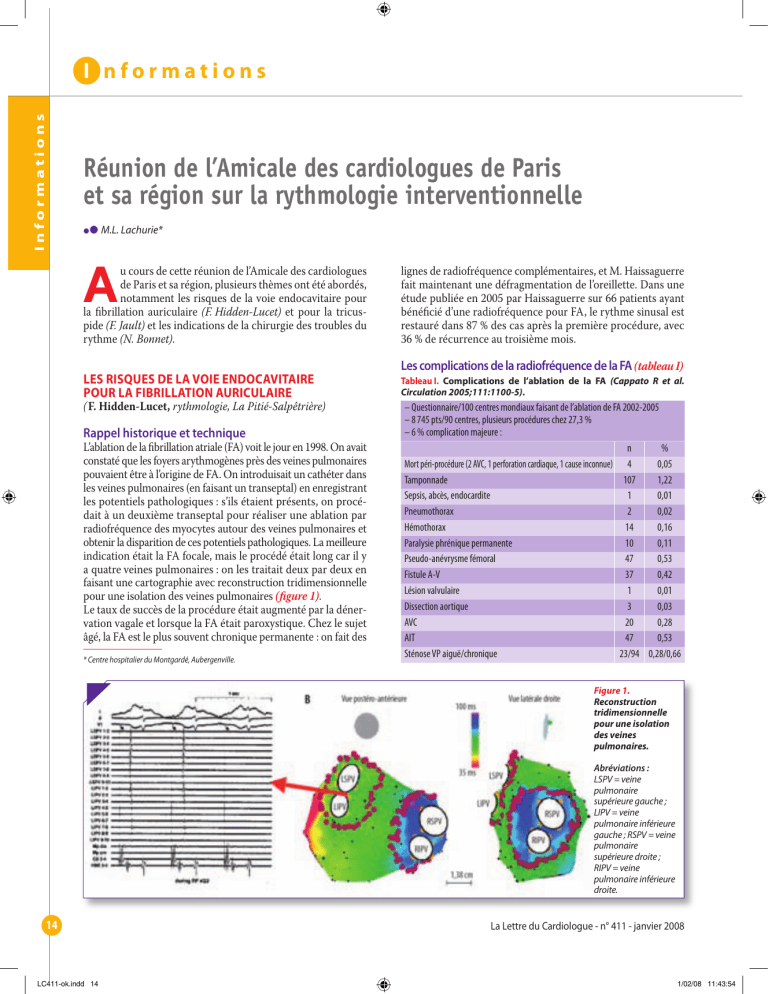
Informations I nformations Réunion de l’Amicale des cardiologues de Paris et sa région sur la rythmologie interventionnelle IP M.L. Lachurie* A u cours de cette réunion de l’Amicale des cardiologues de Paris et sa région, plusieurs thèmes ont été abordés, notamment les risques de la voie endocavitaire pour la fibrillation auriculaire (F. Hidden-Lucet) et pour la tricuspide (F. Jault) et les indications de la chirurgie des troubles du rythme (N. Bonnet). Les risques de la voie endocavitaire pour la fibrillation auriculaire ( F. Hidden-Lucet, rythmologie, La Pitié-Salpêtrière) Rappel historique et technique L’ablation de la fibrillation atriale (FA) voit le jour en 1998. On avait constaté que les foyers arythmogènes près des veines pulmonaires pouvaient être à l’origine de FA. On introduisait un cathéter dans les veines pulmonaires (en faisant un transeptal) en enregistrant les potentiels pathologiques : s’ils étaient présents, on procédait à un deuxième transeptal pour réaliser une ablation par radiofréquence des myocytes autour des veines pulmonaires et obtenir la disparition de ces potentiels pathologiques. La meilleure indication était la FA focale, mais le procédé était long car il y a quatre veines pulmonaires : on les traitait deux par deux en faisant une cartographie avec reconstruction tridimensionnelle pour une isolation des veines pulmonaires (figure 1). Le taux de succès de la procédure était augmenté par la dénervation vagale et lorsque la FA était paroxystique. Chez le sujet âgé, la FA est le plus souvent chronique permanente : on fait des * Centre hospitalier du Montgardé, Aubergenville. lignes de radiofréquence complémentaires, et M. Haissaguerre fait maintenant une défragmentation de l’oreillette. Dans une étude publiée en 2005 par Haissaguerre sur 66 patients ayant bénéficié d’une radiofréquence pour FA, le rythme sinusal est restauré dans 87 % des cas après la première procédure, avec 36 % de récurrence au troisième mois. Les complications de la radiofréquence de la FA (tableau I) Tableau I. Complications de l’ablation de la FA (Cappato R et al. Circulation 2005;111:1100-5). – Questionnaire/100 centres mondiaux faisant de l’ablation de FA 2002-2005 – 8 745 pts/90 centres, plusieurs procédures chez 27,3 % – 6 % complication majeure : n % Mort péri-procédure (2 AVC, 1 perforation cardiaque, 1 cause inconnue) 4 0,05 Tamponnade 107 1,22 Sepsis, abcès, endocardite 1 0,01 Pneumothorax 2 0,02 Hémothorax 14 0,16 Paralysie phrénique permanente 10 0,11 Pseudo-anévrysme fémoral 47 0,53 Fistule A-V 37 0,42 Lésion valvulaire 1 0,01 Dissection aortique 3 0,03 AVC 20 0,28 AIT 47 0,53 Sténose VP aiguë/chronique 23/94 0,28/0,66 Figure 1. Reconstruction tridimensionnelle pour une isolation des veines pulmonaires. Abréviations : LSPV = veine pulmonaire supérieure gauche ; LIPV = veine pulmonaire inférieure gauche ; RSPV = veine pulmonaire supérieure droite ; RIPV = veine pulmonaire inférieure droite. 14 LC411-ok.indd 14 La Lettre du Cardiologue - n° 411 - janvier 2008 1/02/08 11:43:54 On note 6 % de complications majeures : sténoses des veines pulmonaires, tamponnades (patients sous anticoagulant), infections (sepsis, abcès, endocardite), thrombo-embolies (gazeuses) et aussi hémothorax, paralysie phrénique, etc. La limitation de la puissance délivrée lors de l’ablation a permis de diminuer le risque de tamponnade, sans le supprimer. Concernant le risque d’AIT et d’AVC, un antiagrégant plaquettaire en complément de l’anticoagulation efficace n’a pas diminué le risque. La paralysie phrénique s’explique par sa proximité avec les veines pulmonaires ; elle est le plus souvent droite (0,48 % dans l’isolement de la veine pulmonaire supérieure droite), plus rarement gauche (suite à une application près de l’auricule gauche). L’évolution se fait sans séquelles dans 66 % des cas, et dans 33 % des cas on note la persistance partielle ou complète de la paralysie. Les sténoses pulmonaires (complications graves) apparaissent une à 48 semaines après la procédure, se manifestant par une toux, une hémoptysie, une dyspnée, une douleur thoracique (pour que le patient devienne symptomatique, il faut plusieurs sténoses pulmonaires). Le traitement par dilatation se complique de resténose et l’implantation de stent se complique de thrombose… La fistule atrio-œsophagienne est rare mais mortelle. Elle se situe à l’endroit où l’on a fait des applications répétées (surtout près de la veine pulmonaire supérieure gauche) : on essaye de diminuer le risque en repérant l’œsophage, en diminuant la durée des applications et en réduisant la puissance pour limiter la profondeur de la lésion. Les tachycardies atriales gauches par réentrée post-radiofréquence touchent 2,5 à 22 % des patients : on recommence alors la procédure. Ablation par radiofréquence pour qui ? D’après l’étude de C. Pappone et al., le traitement de la FA par radiofréquence est responsable de moins d’effets secondaires que ne l’est le traitement médical (8 % versus 19 %), d’une survie améliorée (94 % versus 86 %) et d’une plus grande efficacité (figure 2). 100 Survie sans récidive de FA (%) 80 78 p < 0,001 60 40 37 20 0 Effets indésirables (abl/méd) : 8 %/19 % Survie (abl/méd) : 94 %/86 % p < 0,001 0 Nombre de patients Ablation 589 Traitement 582 médical 180 360 507 456 479 354 540 720 Délai de suivi (jours) 379 277 282 207 Groupe avec ablation Groupe avec traitement médical (méd) 900 1 080 217 141 135 97 Figure 2. Comparaison traitement médical versus ablation dans la prévention de la récidive de FA (Pappone C, Rosanio S, Augello G et al. Mortality, morbidity and quality of life after circumferential pulmonary vein ablation for atrial fibrillation: outcomes from a controlled nonrandomized long-term stydy. J Am Coll Cardiol 2003;42:185-97). La Lettre du Cardiologue - n° 411 - janvier 2008 LC411-ok.indd 15 Les risques de la voie endocavitaire pour la tricuspide ( F. Jault, chirurgie thoracique et cardiovasculaire, La Pitié-Salpêtrière) Les complications sur la tricuspide en présence d’un pacemaker (PM) ou d’un multisite sont essentiellement : – infectieuses (nécessitant l’ablation du matériel par voie percutanée ou chirurgicale et une antibiothérapie prolongée) ; – thrombo-emboliques ; – valvulaires : rétrécissement tricuspide (suite à une fibrose), insuffisance tricuspide (IT) en dehors de toute atteinte infectieuse. F. Jault a insisté sur la nécessité d’évoquer une insuffisance tricuspide chez des patients avec un PM en tableau clinique de défaillance cardiaque à prédominance droite. L’échocardiographie transœsophagienne préopératoire permet de constater l’IT, mais son mécanisme n’est retrouvé que dans environ 45 % des cas. Le traitement, qui nécessite une chirurgie tricuspide, montre, en per-opératoire, des lésions à type d’adhérences et de perforations (Ling G et al. JACC 2005). Informations I nformations Les indications de la chirurgie des troubles du rythme ( N. Bonnet, chirurgie thoracique et cardiovasculaire, La Pitié-Salpêtrière) Les troubles de la conduction Le premier pacemaker (PM) extracorporel date de 1955 (P. Zoll et W. Lillehei) ; le premier PM implanté par voie sous-épicardique date de 1958 (P. Elmqvist et A. Sennig) ; par la suite, l’implantation des PM s’est faite par voie endocavitaire. Il existe cependant des indications pour lesquelles l’abord direct du cœur pour stimulation en cas de bloc auriculoventriculaire est nécessaire : en cas de problème de voie d’abord (thrombose cave supérieure, anatomie particulière acquise ou congénitale) ou en pédiatrie, en cas d’endocardite. Sur le plan technique, la voie d’abord chirurgicale est une thoracoscopie, une thoracotomie droite ou gauche, ou une sternotomie ; l’abord cardiaque est épicardique ou endocardique ; il est possible de stimuler l’une des cavités cardiaques. Dans le cas d’une endocardite sur sonde, il peut s’agir d’une extraction simple ou sous CEC (échec de l’extraction simple, végétation volumineuse ou nécessité d’un geste chirurgical associé). Dans l’implantation de multisite, on fait une mini-thoracotomie antérieure gauche, un mapping du ventricule gauche. La voie épicardique est choisie lorsqu’une chirurgie cardiaque combinée par sternotomie est prévue (ce qui inclut les endocardites sur sonde), ou en cas d’échec ou de contre-indication à la voie du sinus coronaire. L’intérêt de la technique est d’augmenter le nombre de patients effectivement resynchronisés, d’aller vers une standardisation de la procédure multisite, et de rechercher les facteurs prédictifs de difficultés techniques de la voie du sinus coronaire. 15 1/02/08 11:43:55 Informations I nformations Tableau II. Résultats de l’ablation chirurgicale de la FA (AC/FA) par sternotomie, puis section-suture des chemins électriques (CoxMaze III, RJ Damiano et al., JTCS 2005). • 276 procédures, dont 41 % combinées – AC/FA paroxystique – AC/FA permanente 58 % 42 % • Résultats – Mortalité opératoire – Récurrence précoce AC/FA – Trouble de conduction 1,4 % 44,6 % 16,7 % • Long terme (6,0 ± 3,6 ans) – Récurrence tardive AC/FA – Traitement antiarythmique 7,8 % 20 % • Échec corrélé durée de l’AC/FA préopératoire Les troubles du rythme Plusieurs techniques ont été proposées : thyroïdectomie, stellectomie, chirurgie du Kent, ventriculotomie d’exclusion, chirurgie Figure 3. Exclusion chirurgicale de l’auricule gauche (LAA). de la FA. La chirurgie de la FA garde essentiellement sa place dans la chirurgie combinée, surtout dans la chirurgie valvulaire mitrale, moins souvent dans les pontages aorto-coronaires, et plus rarement dans la FA isolée (thoracoscopie, Cox-Maze, exclusion de l’auricule gauche) [tableau II et figure 3]. ■ 6WdccZo"kdjhZiWc[^X^Zo YZhXgY^ihYZ;dgbVi^dcBY^XVaZ 8dci^cjZ :Y^bVg`HVcikdjhegdedhZYZhG:KJ:HYZ;DGB6I>DC $JcXdb^iYZgYVXi^dchX^Zci^ÒfjZZijcXdb^iYZaZXijgZfj^egdedhZciYZhVgi^XaZhh^\cheVgaZhVjiZjgh\VgVcih YZaÉ^cYZmVi^dcVXXdbeV\chYZaZjghXddgYdccZh $9Zhg[gZcXZhW^Wa^d\gVe]^fjZhhnhibVi^fjZbZciVeeZaZhYVchaZiZmiZ $AVcdi^dcYZÆXdcÓ^iYÉ^cigiÆXaV^gZbZci^cY^fjZVÒcYZ\VgVci^gaÉdW_ZXi^k^i!aVfjVa^iZiaÉ^cYeZcYVcXZhX^Zci^ÒfjZ YZhVgi^XaZhejWa^h $JcZejWa^X^ik^hjZaaZZi$djgYVXi^dccZaaZYjbY^XVbZciZiYjbVig^ZabY^XVaeVg[V^iZbZci^YZci^ÒZ! hVch^ciZggdbegZaVXdci^cj^iYÉjcVgi^XaZ $AZhVgi^XaZhYÉdgYgZhX^Zci^ÒfjZZiY^YVXi^fjZXdchi^ijZciaÉZhhZci^ZaYjXdciZcjgYVXi^dccZa <V\cZo)XgY^iheVgVcZckdjhVWdccVciYhbV^ciZcVci|jcZYZcdhejWa^XVi^dch kd^gcdigZWjaaZi^cYÉVWdccZbZcieV\Z'* AV[VXijgZdjjcZViiZhiVi^dckVa^YZgdcikdigZ;B8 C#7#AZWVgbZYZhXgY^ihYZ;B8ejWa^eVgaZb^c^higZYZaVHVci YXgZiYj&(_j^aaZi'%%+!eVgjVj?djgcVad[ÒX^ZaaZ.Vdi'%%+egdedhZfjVigZ XVi\dg^ZhYÉVXi^dcYZ;B8ZiYÉkVajVi^dcYZhegVi^fjZhegd[Zhh^dccZaaZhYdciaVXVi\dg^Z'!XdbegZcVciaZh[dgbVi^dch^cY^k^YjZaaZhZi|Y^hiVcXZji^a^hVci idjihjeedgibVig^ZadjaZXigdc^fjZ!cdiVbbZciaZhVWdccZbZcih|YZheg^dY^fjZhdjaÉVXfj^h^i^dcYÉdjkgV\ZhbY^XVjm# 16 BANDO FMC REVUE-L-Q.indd 1 LC411-ok.indd 16 1/02/08 10:41:06 La Lettre du Cardiologue - n° 411 - janvier 2008 1/02/08 11:43:56