Antibioprophylaxie chirurgicale - Infectio

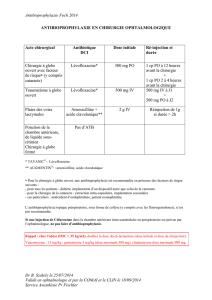
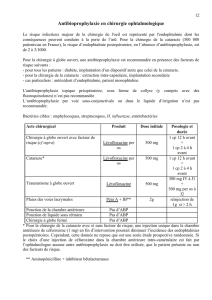
ANTIBIOPROPHYLAXIE
CHIRURGICALE

Un peu d'histoire
Infections du site opératoire = première
complication de la chirurgie.
1961 : L'antibioprophylaxie permet la réduction des
ISO
Contribue à la réduction d'un risque infectieux
hypothétique, mais toujours complémentaire des
règles d'hygiène hospitalière et d'asepsie
chirurgicale.

Infection du site opératoire
Les services de chirurgie ont la plus forte incidence d’infections
nosocomiales derrière la réanimation
Les infections post-opératoires représentent la 1ère cause de mortalité et de
morbidité en chirurgie, les interventions étant de plus en plus lourdes et
pratiquées chez des malades de plus en plus graves et/ou immunodéprimés
3ème cause d’infection nosocomiale (11% des infections nosocomiales)
Taux d’incidence 3 à 7% dans la littérature et d’environ 3% d’après les
réseaux de surveillance (inter-région nord) mais très variable en fonction de
la pathologie, du type de chirurgie et des différents facteurs de risque

0,94
0,58
0,87
0,89
0,73
1,28
1,11
1,42
1,52
0,99
0,46
0,55
1,04
0,51
0,93
0,67
0,0
0,2
0,4
0,6
0,8
1,0
1,2
1,4
1,6
2004 2005 2006 2007 2008 2009 2010 2011
Taux d'ISO global Taux d'ISO en NNIS-0

 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
1
/
51
100%