évaluation

Classe de première STL
ÉVALUATION
ÉVALUATION
Physique (.../ 9)
Données
●indice de réfraction de l'air : 1,00
●indice de réfraction de l'eau : 1,33
●indice de réfraction du diamant : 2,40
Questions Cours (QC): 1 point par question
QC1. Proposer une phrase permettant de définir simplement le phénomène de réfraction.
Lors d'un changement de milieu, la lumière peut subir une déviation. Ce phénomène porte le nom
de réfraction.
QC2. Qu'est-ce qu'un dioptre?
Un dioptre est la surface de séparation entre deux milieux transparents d'indices de réfraction
différents.
QC3. Enoncer les lois de Snell-Descartes.
1ère loi : Le rayon réfracté et le rayon réfléchi sont dans le plan d'incidence. Ce dernier est défini
par le rayon incident et la normale au dioptre.
2ème loi : le rapport des sinus des angles incident et réfracté est une constante ne dépendant que des
indices de réfraction des milieux. On note en général cette relation:
n1.sini1 = n2.sini2
3ème loi : Lors de la réflexion d'un rayon lumineux, l'angle réfléchi est égal à l'angle incident.
Questions Applications (QA): 3 points par question
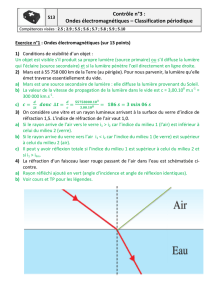
QA1. Calculer la valeur de l'angle de réfraction i2 sachant que l'angle incident i1 vaut 20°. Le
milieu incident noté 1 est l'air, l'autre milieu noté 2 est de l'eau. Vous accompagnerez votre
réponse d'un schéma clair, légendé et à l'échelle pour les angles.
On applique la deuxième loi de Snell-Descartes:
n1.sini1 = n2.sini2
1 * sin(20) = 1,33 *sini2
sini2=sin(20)/ 1,33
i2=15°
Schéma

QA2. Un faisceau laser sort d'un morceau de diamant et se retrouve dans l'air. L'angle d'incidence
du faisceau laser peut-il être quelconque sinon quels sont les angles d'incidence permettant
au faisceau laser de sortir du diamant? Justifier votre réponse.
Le milieu incident étant plus réfringent que le milieu réfracté, il existe un angle limite au delà du
quel la lumière ne peut plus sortir mais est réfléchie par le dioptre.
n1.sini1 = n2.sini2
2,4 * sini1 = 1 *sin90
sini1=1/2,4
i1=24,6° = 25°
L'angle limite dans ce cas est 25° où on observera l'émergence rasante. Pour les angles supérieurs à
25°, on observera une réflexion de la lumière.
Chimie (.../11)
Données
Elément chimique Hydrogène Carbone Oxygène Phosphore
Numéro atomique 1 6 8 15
Masse molaire
atomique 1 12 16 31
Questions de cours (QC): 1 point par question
QC1. Quelles sont les particules constituant un atome possèdant une charge électrique?
Un atome est constitué de trois types de particules (protons, neutrons et électrons) dont deux types
seulement sont chargés : les protons (chargés positivement) et les électrons (chargés négativement).
QC2. Un atome peut-il être chargé électriquement?
Non, par définition un atome est électriquement neutre.
QC3. Enoncer la règle du duet et de l'octet.
Les éléments chimiques tendent à acquérir la structure électronique des gaz nobles (c'est-à-dire un
état stable). Ils cherchent donc à compléter leur couche externe soit à 2 électrons (règle du duet) soit
à 8 électrons (règle de l'octet). Pour cela, ils forment soit des ions, soit par association avec d'autres
atomes, ils forment des liaisons covalentes.
QC4. Qu'est-ce que deux isomères?
Deux molécules de même formule brute mais de constitution différente sont appelées isomères.
Questions Applications (QA): 1 point par question
QA1. Quel est le nombre de protons et d'électrons constituant un atome de phosphore?
Un atome de phosphore contient 15 protons d'après son numéro atomique Z. Etant électriquement
neutre, il contient donc 15 électrons.

QA2. Quelle est la valence de l'atome de phosphore. Vous détaillerez votre démarche.
La valence étant le nombre de liaisons covalentes que peut faire un atome, je recherche la structure
électronique de P.
K2L8M5 soit 5 électrons externes.
Pour respecter la règle de l'octet, l'atome de phosphore (comme l'azote de la même famille) devra
former 3 liaisons covalentes. Il lui restera un doublet non liant.
Sa valence est 3.
QA3. Dans le tableau de données précédent, un oubli a été commis. Lequel?
L'unité de la masse molaire atomique est g/mol.
QA4. Donner la représentation de Lewis de la molécule de dioxyde de carbone.
QA5. Donner la formule topologique des molécules suivantes:
CH3-CH2-CH2-CH3CH3-CH2-CH2-OH
QA6. Donner la représentation de Cram de la molécule d'éthane CH3-CH3.
QA7. Calculer la masse molaire moléculaire de la molécule d'éthanol CH3-CH2-OH.
M(C2H6O)=2.M(C)+6.M(H)+M(O) = 46 g/mol
O=C=O
1
/
3
100%