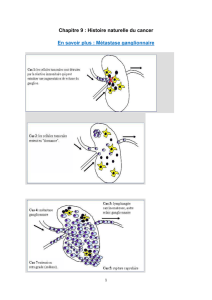
Contribution sympathique au plexus cardiaque

1
&RQWULEXWLRQV\PSDWKLTXHDXSOH[XV
FDUGLDTXH
N. PATHER, P. PARTAB, B. SINGH ET K.S. SATYAPAL
,QWURGXFWLRQ
Le traitement des patients présentant une angine de poitrine réfractaire et une
maladie coronarienne, qui ne peuvent être proposés à une revascularisation
coronaire conventionnelle, est de plus en plus cosidéré par les cardiologues
comme un problème sérieux et croissant. De plus, les patients ayant bénéficié d'un
pontage coronaire vivent plus longtemps et, grâce à l'augmentation de l'espérance
de vie par greffe veineuse, développent ensuite une angine de poitrine liée au
blocage ou à l'atteinte de la greffe par la maladie [4]. Ces patients sont réfractaires
aux modalités thérapeutiques habituellement utilisées et sont très débilités,
nécessitent des hospitalisations fréquentes et consomment d'importantes
ressources économiques. Grâce aux avancées actuelles des techniques
chirurgicales sous endoscopie, le succès de l'interruption chirurgicale des voies
sympathiques pour traiter la douleur angineuse chez ces patients a été récemment
montré [1, 4, 11].
La dénervation sympathique cardiaque réalisée en chirurgie vidéo-assistée sous
thoracoscopie sur des patients présentant une angine de poitrine réfractaire et qui
ne peuvent être proposés à la revascularisation conventionnelle a été rapportée
comme une option thérapeutique sûre et efficace avec de bons résultats tant
subjectifs qu'objectifs. La sympathectomie gauche est toujours réalisée d'abord
pour éviter une arythmie [11].
L'angine d'effort a la même origine que la claudication intermittente cas les nerfs
sympathiques, qui conduisent les influx douloureux jusqu'au cerveau sont
identiques aux fibres sensitives somatiques [10]. Ils naissent des terminaisons
nerveuses périartérielles et épicardiques dans le cœur et cheminent par les plexus
cardiaques et les nerfs cervicaux moyens et inférieurs jusqu'aux ganglions
cervicaux moyens et inférieurs par l'intermédiaire desquels ils passent sans

2
interruption et continuent leur chemin par le tronc sympathique jusqu'à la moelle
épinière via les rameaux communicants des 4 ou 5 premières racines thoraciques.
Il est probable que d'autres routes existent courant directement du plexus profond
aux 4 ou 5 premiers ganglions thoraciques, mais on connaît peu de choses sur les
voies alternatives [10].
La résection sélective bilatérale des troncs sympathiques cervicaux, du deuxième
au quatrième ganglions avec préservation du ganglion cervico-thoracique (GCT)
ou ganglion stellaire, c'est-à-dire la fusion du ganglion cervical inférieur (GCI) et
du ganglion T1, et des rameaux cardiaques cervicaux a montré son efficacité pour
arrêter les signes d'alerte de l'angine "une sensation d'oppression inconfortable"
[4].
La littérature rapporte que les nerfs sympathiques cardiaques sont extrêmement
variables dans leur topographie [5, 7]. Leur disposition complexe et diverse peut
rendre compte des contradictions morphologiques contenues dans la littérature
que nous avons revue. Le succès d'une dénervation cardiaque sympathique pour
traiter la douleur, un champ souvent entaché d'échecs, dépend de la connaissance
morphologique précise des rameaux cardiaques cervicaux et thoraciques [2]. Le
but de cette étude était de documenter l'origine et la fréquence des contributions
sympathiques cervicales et thoraciques aux plexus cardiaques.
0DWpULHOHWPpWKRGH
Les parties cervicales et thoraciques des troncs sympathiques de 21fœtus formolés
(âge gestationnel variant de 16 semaines au terme complet, 11 garçons 10 filles) et
8 adultes formolés (âge variant de 18 à 55 ans, 4 hommes, 4 femmes) provenant
du département d'anatomie de l'université de Durban Westville, ont été disséqués
des deux côtés sous loupe grossissante, et documentés (n = 58, 29 droits et 29
gauches). Un appareil Sony Digicam 9 a été utilisé pour les documents
photographiques.
Le tronc sympathique était identifié et les rameaux communicants pour chaque
rameau ventral étaient exposés. Les branches médiales issues des segments

3
cervical et thoracique du tronc sympathique étaient alors disséquées et suivies
jusqu'au plexus cardiaque.
Les ganglions fusionnés, les segments de rameaux cardiaques et de segments
inter-ganglionnaires entre GCI, T1 et T2, ont été biopsiés et colorés à
l'hématoxyline-éosine, inclus dans la paraffine et sectionnés à 0.1 µ pour étude
microscopique. L'authenticité des structures biopsiées a ainsi été confirmée
histologiquement.
5pVXOWDWV
,QFLGHQFHGHVJDQJOLRQVFHUYLFDX[
L'incidence des ganglions cervicaux était la suivante :
- Ganglion cervical supérieur (GCS) : 100 % (fœtus 100 %, adultes
100 %)
- Ganglion cervical moyen (GCM) : 81,1 % (fœtus 83,4 %, adultes
75 %)
- Ganglion stellaire ou cervico-thoracique : (GCT) 84,5 % (fœtus
90,5 %, adultes 68,8 %)
En cas d'absence du GCT, des ganglions séparés GCI et T1 ont été notés dans
15,5 % des cas.
L'étude histologique du segment inter-ganglionnaire montrait l'absence de corps
cellulaire ganglionnaire et confirmait l'existence de ganglions non fusionnés.
5DPHDX[FDUGLDTXHV
Les rameaux sympathiques cardiaques ont été différenciés en fonction de leur
origine à partir des parties cervicale et thoracique du tronc sympathique en trois
groupes : rameaux sympathiques cardiaques cervicaux (RCC), rameau cardiaque
cervico-thoracique (RCCT) et rameaux cardiaques thoraciques (RCT).
Les rameaux cardiaques ont été étudiés des deux côtés. Les résultats sont
regroupés sur le tableau 1 et la fig. 1 . L'origine des rameaux cardiaques à partir

4
du tronc sympathique était extrêmement variable et asymétrique, c'est-à-dire que
sur aucun spécimen la disposition était identique à droite et à gauche.
5DPHDX[FDUGLDTXHVFHUYLFDX[5&&
La fréquence du rameau cardiaque cervical supérieur (RCCS) était de 100 % et
l'origine du RCCS siégeait au niveau du GCS dans 31 cas sur 58, soit 53.4 % (16
cas sur 29, soit 55,2 % à droite et 15 cas sur 29 à gauche soit 51,7 %) (fig. 2 ) ou
du segment interganglionnaire du tronc au-dessous du ganglion dans 27 cas sur
58, soit 46,6 %, 13 cas sur 29 soit 44,8 % à droite et 14 cas sur 29 soit 48,3 à
gauche. Parmi ceux-là, la distance séparant le pôle inférieur du GCS de l'origine
du RCCS variait de 4,8 à 19,3 mm (moyenne 17,3 mm).
Le rameau cardiaque cervical moyen (RCCM) était présent 51 fois sur 58, soit
87,9 %. L'origine du LRCC siégeait au niveau du LCG dans 41 cas, soit 70,7 %
(fig. 2) ou au niveau du segment interganglionnaire dans 10 cas sur 58 soit 17,2 %
(4 cas sur 29, soit 13,8 % à droite et 6 cas sur 29, soit 20, 7 % à gauche). Dans ce
dernier cas, la distance qui séparait l'origine du pôle inférieur du ganglion variait
de 3,8 à 47,2 mm (3,96 mm en moyenne). Quand le GCM était absent, le
deuxième rameau cardiaque issu du segment interganglionnaire entre le GCS et le
GCT était supposé être le RCCM. Le RCCM était le plus gros de tous les rameaux
cardiaques cervicaux.
5DPHDX[FDUGLDTXHVFHUYLFRWKRUDFLTXHV5&&7
Les rameaux cardiaques issus du GCT ou, en son absence, du GCI et du ganglion
T1, ont été regroupés sous le terme de RCCT et différenciés comme « RCCT
propre » (rameau cardiaque cervico-thoracique propre), « RCCI propre » (rameau
cardiaque cervicae inférieur propre), et « RCT1 propre» (rameau cardiaque
thoracique 1). Les RCCI propres et RCCT propres n'ont pu être étudiés que sur 9
côtés (5 droits et 4 gauches) en raison de la faible incidence des GCI documentés
dans ce travail.
Le RCCI propre naissait du GCI 4 fois sur 9 soit 44.5 % (3 fois sur 5 soit 60 % à
droite, et 1 fois sur 4 soit 25 % à gauche). Le RCT1 propre naissait du ganglion 6
fois sur 9 soit 66,6 % (4 fois sur 5 soit 80 % à droite, et 2 fois sur 4 soit 50 % à

5
gauche). 2 fois sur 9, soit 22.2 %, le RCC1 propre naissait de la moitié supérieure
du segment inter-ganglionnaire du tronc sympathique au-dessous du ganglion T1.
Le RCC propre a été étudié sur les 49 côtés sur 48 qui présentaient un GCT.
L'incidence du RCCT était de 100 %. Il naissait du GCT 41 fois sur 49 soit 83,7
% (21 fois sur 24 soit 87,5 % à droite et 20 fois sur 25 soit 80 % à gauche). Dans
37 cas soit 90,2 %, il y avait 2 RCCT alors que dans 4 cas (9,8 %) il n'y avait
qu'un seul rameau. Sur 3 de ces cas, un deuxième rameau fut trouvé naissant du
tronc au-dessous du GCT. Sur 9 cas sur 49, soit 16,3 %, le RCCT naissait du
segment inter-ganglionnaire du tronc au-dessous du ganglion. La distance
séparant son origine du pôle inférieur du ganglion variait de 1,2 à 2,6 mm (2,1
mm en moyenne).
5DPHDX[FDUGLDTXHVWKRUDFLTXHV5&7
Dans la région thoracique, 4 RCT naissaient du tronc sympathique thoracique au-
dessous du GCT ou du ganglion T1 (fig. ). L'origine de ces rameaux cardiaques se
situait à la fois sur le ganglion et le segment inter-ganglionnaire. Les RCT ont été
dénommés séquentiellement après l'identification du RCT 1.
L'incidence d'un deuxième rameau cardiaque thoracique (RCT2) est de 84,5 % se
décomposant en 29 cas sur 58, soit 50 % d'origine ganglionnaire et de 20 cas sur
58 soit 34,5 % d'origine inter-ganglionnaire.
L'origine inter-ganglionnaire variait comme suit : entre les deuxième et troisième
ganglions thoraciques 13 fois sur 20 soit 65 % (5 cas sur 8 soit 62,5 % à droite et
2 cas sur 12 soit 66,6 % à gauche), entre le GCT et le deuxième ganglion
thoracique 5 fois sur 20 soit 25 % (3 fois sur 8, soit 37,5 % à droite et 2 fois sur 12
soit 16,6 % à gauche) et entre le deuxième ganglion thoracique et les troisième et
quatrième ganglions thoraciques fusionnés 2 fois sur 20, soit 10 % (0 cas sur 8
soit 0 % à droite et 2 cas sur 12, soit 16,6 % à gauche).
Un troisième rameau cardiaque (RCT3) était présent dans 70,7 % des cas, il
naissait 25 fois sur 58 soit 43,1 % du ganglion, 7 fois sur 58 soit 27,6 % du
segment inter-ganglionnaire. L'origine inter-ganglionnaire se répartissait comme
 6
6
 7
7
 8
8
 9
9
1
/
9
100%