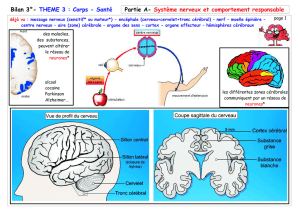
2015-2016 Le système nerveux

Lycée-Collège de la Planta, Sion
Biologie
Option spécifique (OS) 5
ème
(programme maturité)
La neurobiologie
Julien Dubuis

2
« L’homme naît avec des sens et des facultés ; mais il n’apporte avec lui en naissant aucune idée : son
cerveau est table rase qui n’a reçu aucune impression, mais qui est préparé pour en recevoir. »
Antoine-Laurent de Lavoisier, chimiste français (1743-1794)
La neurobiologie s’occupe de la structure et des fonctions des cellules sensorielles et nerveuses. Elle
étudie la transformation des stimuli sensoriels en signaux nerveux, la propagation de ces derniers le
long de la fibre nerveuse, la transmission de signaux d’une cellule nerveuse à l’autre ou encore la
coopération de cellules nerveuses en réseaux complexes. Le contrôle nerveux de l’activité musculaire
appartient également à son champ de recherche. Un des buts principaux de la neurobiologie est de
comprendre les mécanismes du traitement de l’information par le cerveau ainsi que ceux de la
mémoire.
Le système nerveux (SN) est le centre de régulation et de communication de l’organisme ; nos
pensées, nos actions, nos émotions attestent son activité. Ses cellules communiquent au moyen de
signaux électriques rapides et spécifiques qui entraînent des réponses presque immédiates.
Le SN remplit trois fonctions étroitement liées (figure 1).
- Premièrement, par l’intermédiaire de ses millions de récepteurs sensoriels, il reçoit de
l’information sur les changements qui se produisent tant à l’intérieur qu’à l’extérieur de
l’organisme. Ces changements sont appelés stimulus, et l’information recueillie porte le nom
d’information sensorielle.
- Deuxièmement, il traite et interprète l’information sensorielle et détermine l’action à
entreprendre à tout moment, ce qui constitue le processus de l’intégration.
- Troisièmement, il fournit une réponse motrice qui active des muscles ou des glandes
(effecteurs).
Figure 1 : Les fonctions du système nerveux
Illustrons l’accomplissement de ces fonctions par un exemple.
Quand vous êtes au volant et que vous voyez un feu rouge devant vous (l’information sensorielle),
votre système nerveux assimile (intégration) cette information (le feu rouge signifie « arrêtez ») et
émet un influx moteur en direction des muscles de votre jambe droite, lesquels actionnent votre pied
pour qu’il enfonce la pédale de frein (réponse motrice).
1 I
NTRODUCTION

3
Contrairement aux messages nerveux qui sont transmis avec rapidité et précision par un réseau câblé,
les messages hormonaux sont transmis par les hormones, des molécules synthétisées par les glandes
endocrines et transportées par le sang ou la lymphe. Elles diffusent dans tout l’organisme, mais
n’exercent leur action que sur leurs cellules cibles. Parmi les glandes endocrines, l’hypothalamus
occupe une place prépondérante par son rôle d’interface entre le système nerveux et le système
hormonal. Ces deux systèmes permettent de maintenir l’homéostasie.
Les premiers neurones sont vraisemblablement apparus à partir de cellules de l’ectoderme des
premiers animaux multicellulaires, un phénomène qui a eu lieu il y a environ 650 millions d’années.
L’interconnexion de ces cellules a d’abord formé un système nerveux simple, en réseau diffus, comme
celui des hydres ou des méduses.
Avec l’apparition d’animaux à symétrie bilatérale, chez lesquels on peut distinguer l’avant et l’arrière,
ces cellules nerveuses se sont accumulées dans la région antérieure et ont formé un cerveau primitif.
Par exemple chez Platynereis, un ver marin, on observe un cerveau dont certaines structures rappellent
celles du cerveau des vertébrés.
Les nouvelles méthodes de recherche ont beaucoup contribué aux succès de la neurobiologie moderne.
Des techniques particulières de microscopie permettent de marquer des molécules spécifiques à
l’intérieur même des neurones et de les observer in vivo. Il est ainsi possible de visualiser directement
des processus moléculaires ou cellulaires. Par ces techniques, on a pu étudier les modalités de la
croissance des neurones et de l’établissement des réseaux neuronaux durant le développement
embryonnaire. Les recherches sur le contrôle de la croissance des fibres nerveuses présentent un
intérêt particulier, car la connaissance de ces processus pourrait contribuer à trouver des solutions pour
aider les personnes paralysées par suite d’un accident.
Les méthodes d’imagerie actuelles permettent non seulement de visualiser des structures cervicales,
mais aussi de mesurer leur activité. On peut donc dire que ces méthodes rendent visibles des activités
cérébrales qui, jusqu’ici, n’étaient que subjectives. Désormais, on peut « voir » un cerveau en train de
penser.
Les applications de la recherche en neurobiologie trouvent leurs principaux débouchés en médecine.
L’imagerie permet le diagnostic précoce de certaines maladies, parfois avant même les premiers
symptômes cliniques, comme dans le cas de la maladie d’Alzheimer. On peut donc débuter rapidement
une thérapie et en contrôler l’efficacité.
Médecins et ingénieurs travaillent ensemble à développer de nouvelles prothèses. Des chercheurs ont
développé des microchips photosensibles à implanter sous la rétine des personnes qui ont perdu la vue
à la suite d’une maladie de la rétine. Les premiers essais ont démontré que des patients ayant reçu ce
genre d’implants sont capables de distinguer des objets et même de lire.

4
Grâce au système nerveux, les animaux et donc les humains peuvent percevoir leur environnement
ainsi que leur propre corps, et agir en fonction de ces informations. Chez les vertébrés, le cerveau et
la moelle épinière forment le système nerveux central, qui communique avec le reste du corps grâce
au système nerveux périphérique (figure 2)
Figure 2 : L’organisation du SN
En dépit de sa complexité, le tissu nerveux est composé de deux principaux types de cellules
seulement et de capillaires sanguins :
• Les gliocytes ou cellules gliales
• Les neurones
L'encéphale humain est extrêmement complexe. On y trouve environ 100 milliards de neurones,
chacun relié aux autres par, en moyenne, 10’000 contacts.
2
STRUCTURE ET FONCTION DES CELLULES NERVEUSES

5
Le neurone dérive d'une cellule souche embryonnaire appelée neuroblaste. On pensait que le capital de
neurones était fixé dès la naissance, et qu’aucune autre division de la cellule souche ne pouvait donner
de nouveaux neurones. Toute destruction de neurones après la naissance était définitive. De nouveaux
travaux ont montré qu’il existerait des cellules souches adultes, capables de régénération.
2.1 Les cellules gliales
Neuf fois plus nombreux que les neurones, les cellules gliales forment dans le SNC la névroglie
(signifiant littéralement « colle nerveuse »). Les différents types de cellules gliales soutiennent,
isolent et protègent les fragiles neurones (figure 3), et remplit des fonctions particulières. La
névroglie est composée des cellules suivantes :
- Les astrocytes : les plus abondants sont les astrocytes en forme d’étoile. Leurs nombreux
prolongements ont des extrémités renflées qui s’attachent aux neurones et les ancrent à leur
source d’approvisionnement en nutriments, les capillaires sanguins (figure 3a). Les astrocytes
interviennent dans les échanges entre les capillaires et les neurones, et forment entre ces deux
types de structures une barrière vivante. Ils protègent ainsi les neurones contre les substances
nocives qui pourraient se trouver dans le sang. Les astrocytes participent aussi à la régulation
du milieu chimique cérébral en récupérant les ions en excès et en effectuant le recaptage des
neurotransmetteurs libérés.
- Les microglies : en forme d’araignée, sont des macrophagocytes qui éliminent les débris tels
que les cellules mortes de l’encéphale et les bactéries (figure 3b).
- Les épendymocytes : sont des cellules de type épithélial tapissant les cavités de l’encéphale et
de la moelle épinière (figure 3c). Le battement de leur cils facilite la circulation du liquide
cérébrospinal qui remplit ces cavités et forme un coussin protecteur autour du SNC.
- Les oligodendrocytes : sont pourvus de prolongements aplatis qui s’enroulent fermement
autour des neurofibres du SNC. Ils constituent ainsi des enveloppes lipidiques isolantes
appelées gaines de myéline (figure 3d).
Les cellules gliales sont semblables aux neurones sur le plan de la structure (comme eux, ils ont des
prolongements cellulaires), mais, contrairement à ces derniers, ils ne transmettent pas d’influx nerveux
et ne perdent jamais la capacité à se diviser. Par conséquent, la plupart des tumeurs cérébrales, qu’elles
soient bénignes ou malignes, sont des gliomes, c’est-à-dire des masses formées à partir de cellules
gliales (des astrocytes le plus souvent).
Les cellules gliales présentes dans le SNP sont (figure 3e) :
- les neurolemmocytes ou cellules de Schwann, forment les gaines de myéline autour des
neurofibres du SNP
- les cellules gliales ganglionnaires entourent l’amas de corps cellulaires dans les ganglions.
On pourrait garder l’idée que les cellules gliales ne sont que de vulgaires cellules de soutien. Mais ne
concluons pas trop vite ! Des recherches récentes laissent croire qu’ils peuvent détecter l’activité des
neurones et communiquer entre eux, formant en quelque sorte un réseau parallèle aux neurones qui
participerait aussi au traitement de l’information. Curieusement, on a trouvé dans certaines régions du
cerveau d’Einstein un nombre de cellules gliales bien au-dessus de la moyenne !
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
1
/
21
100%