P2-UE8-Belmonte-Staphylocoques-20.02-pdf

1
UE8 – De l’agent infectieux à l’hôte
Olivier BELMONTE
Date : 20/02/2017 Plage horaire : 14h – 16h
Promo : 2016/2017 Enseignant : Dr. BELMONTE
Ronéistes : BIROTA Ameline/ PION Léo
Les staphylocoques
Introduction
I. Habitat et épidémiologie
II. Le Staphylococcus Aureus (SA) (staphylocoque doré)
1. Caractéristiques
A. Pouvoir d’invasion et d’adhésion
B. Pouvoir enzymatique
C. Pouvoir toxinique
2. Les pathologies liées au SA
A. Infections suppuratives superficielles (loco-régionales) et
profondes
B. Infections non suppuratives d’origine toxinique
▪ Syndrome cutané staphylococcique
▪ Choc toxique staphylococcique
▪ Infection à leucocidine de Panton-Valentine
▪ Intoxications alimentaires
3. Diagnostic au laboratoire
A. Examen direct et culture
B. Techniques d’identification
C. Analyse moléculaire
4. Traitement

2
III. Les staphylocoques à coagulase négative (SCN)
IV. Sensibilité et Résistances aux antibiotiques
1. Sensibilité aux antibiotiques
2. Résistance aux antibiotiques
3. Données épidémiologiques concernant le niveau de résistance de
Staphylococcus aureus
Conclusion

3
Rappel : la différence entre bactéries Gram+/- qui est une coloration permettant de mettre en avant des
différences dans la structure de leur paroi. C'est, en pathologie humaine, important de savoir sur quel type
de germe on est face à une infection ce qui permet en général d'avoir une idée de l'orientation
thérapeutique à mettre en place. On se base souvent là-dessus car les informations arrivent rapidement et
donc il est plus facile de poser un traitement.
On va surtout parler aujourd’hui des staphylocoques et des streptocoques qui sont des coccis Gram+. Ces
bactéries sont retrouvées de manière très fréquente dans les pathologies humaines, notamment sur les
infections communautaires (en ville), et les streptocoques ont une place importante dans les infections
materno-fœtales soit en pré-, néo ou post-natal.
Introduction
Les staphylocoques, du genre Staphylococcus ont été identifiés en 1800 par Pasteur, et comptent
parmi les premières bactéries qui ont été découvertes. Ils appartiennent à la grande famille des
micrococcacae, dans laquelle le staphylocoque est le principal pathogène.
On identifie plus d’une 40aine d’espèces différentes dans le genre Staphylococcus. Elles sont
impliquées dans de nombreuses pathologies. Cependant on s’intéressera davantage à une espèce, le
staphylococcus aureus.
Les staphylocoques sont des coccis Gram+, identifiables à l’examen direct microscopique dès J0, ayant
tendance à se disposer en amas et à se colorer en violet. On parle de la grappe de raisins. Quand on voit
sur un rapport de bactériologie : « présence de coccis Gram+ en amas ou grappe de raisins », il faudra
penser directement à présence de staphylocoques.
Notion extrêmement importante à retenir : coccis Gram+ en amas = staphylocoques !!!
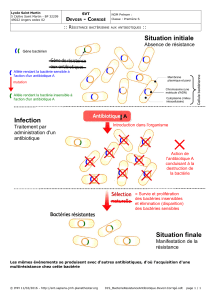
Quand vous aurez une infection où il
est précisé « prélèvement purulent
avec des coccis en amas », vous
conclurez qu’il faudra mettre en place,
quoi qu’il arrive, une antibiothérapie
couvrant les staphylocoques. Certes il
pourra y avoir parfois d’autres germes
associés, mais il ne faudra pas
négliger les staphylocoques, qui
restent néanmoins une des espèces les
plus virulentes. On pourra donc mettre
une antibiothérapie couvrant les
staphylo et ce dès le premier jour.
Ces staphylocoques ont d’autres
caractéristiques qui ne sont pas
essentielles à retenir, notamment une
catalase positive (technique de
laboratoire, abordée plus loin dans le
cours).

4
Par contre, il est important de connaitre qu’il s’agit d’un germe aéro-anaérobie, donc elles se développent
en absence ou en présence d'oxygène, elles préfèrent quand il y en a mais elles arrivent aussi à pousser en
anéarobiose.
Ce n'est pas le cas de toutes les bactéries : certaines bactéries poussent en anaérobie stricte, se développant
donc qu’en absence d’oxygène et qu’on ne retrouvera pas dans tout type d’infection mais plutôt dans celles
profondes ou digestives.
Mais les aéro-anaérobies, que ce soit les staphylocoques ou les streptocoques, sont des germes présents
dans une multitude d’infections, en tout cas ce ne sont pas les conditions atmosphériques qui vont les
empêcher de se développer. Son caractère aéro-anaérobie facilite sa mise en culture au laboratoire.
On observe des formes arrondies violacées en amas,
oriente rapidement vers le genre Staphylococcus. On ne
distingue pas à ce stade s’il s’agit d’une souche Aureus ou
autre.
I. Habitat / Epidémiologie
Les staphylocoques sont des germes commensaux (y compris le S. Aureus) dont l'Homme et les
animaux à sang chaud sont des réservoirs naturels, c’est-à-dire qu'ils sont trouvés de manière
systématique chez eux.
Il faut savoir que 30% de la population humaine est porteuse chronique de S. doré, le
Staphyloccoque le plus virulent impliqué en pathologie humaine. On a un donc un portage endogène
de staphylocoques dorés dans un tiers de la population de manière systématique.
Mais attention, le fait de le porter n'est pas synonyme d'être infecté. Nous sommes tous porteurs
de centaines de milliers de staphylocoques, ce n’est pas pour autant qu’on se porte mal. Il y a en fait une
colonisation cutanée essentiellement dans les régions chaudes et humides : le périnée, le vagin,
l'intestin, au niveau de la gorge, de la peau des
mains (transmission manuportée!!) et surtout
au niveau des fosses nasales +++. Le portage est
transitoire pour certains, persistant pour
d’autres (on a parfois un clone qui persiste chez
un individu très longtemps sans qu’il y ait de
complications, mais qui permet la diffusion des
germes. Il existe des clones différents de
staphylocoque aureus. Les porteurs chroniques
portent souvent toujours le même clone, il y’a une
certaine affinité. Il a également une charge
bactérienne plus élevée que le porteur transitoire,
c’est-à-dire plus de bactéries.).

5
Remarque sur le schéma : à gauche se trouve un porteur transitoire. Le SA est souvent retrouvé
dans les fosses nasales, que le porteur soit transitoire ou chronique.
On se sert de la caractéristique de leur présence dans les fosses nasales pour dépister les porteurs
de SA en faisant un écouvillonnage. On chercher à dépister les porteurs de SA dans certains services
cliniques pour prévenir des complications d'infections après certaines chirurgies dites à risques,
notamment cardiaques et orthopédiques. Il s’agit de faire une décontamination préventive des porteurs de
manière à éviter les infections post-opératoires, car les porteurs chroniques de SA sont plus à risques
d'infections. Chez les porteurs chroniques, il est déconseillé de faire une décontamination à part pour les
chirurgies à risques, parce que les patients reçoivent énormément d’antibiotiques pour très peu de
résultats. En effet, le porteur chronique risque de se faire recoloniser.
Dans certains cas de figure, on fait également du dépistage dans des unités à risques pour vérifier
que les patients ne soient pas porteurs de bactéries multirésistantes (BMR). Parmi ces BMR, il y'a le
staphylocoque doré multiresistant. S’il est détecté, on ne va pas essayer de le décoloniser, mais plutôt de
prendre des mesures complémentaires pour éviter au patient A porteur de transmettre la bactérie à un
autre patient du service, qui est fragile et qui serait amené à être infecté.
On a un donc un portage endogène de staphylocoques dorés dans un tiers de la population de manière
systématique. Alors que les staphylococcus non aureus, qu’on appelle blancs ou à coagulase non
négative, prolifèrent beaucoup sur la peau, au niveau de la flore cutanée. Ils sont non pathogènes (mais
ce sont des bactéries opportunistes qui savent profiter, pour proliférer, d’un état particulier du patient,
souvent des états d’immunodépression avec des défenses immunitaires qui sont un petit peu moins
efficientes qu’elles ne devraient). Et il y a à peu près 100% de porteurs. Parfois, ils vont pouvoir
contaminer certains types de prélèvements qu’on sera amené à réaliser chez le patient.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
1
/
28
100%