methoxyflurane : PENTHROX

!"#$%&'()*+,"-.-/01234567-
!"#"$%&'(%#)*(+)','")##
-$%*#.(#-*+/'#'"#01(*2'#3'#.(#3$%.'%*#(%4#%*2'"0'/#
/*8-0*9:-;<0=-
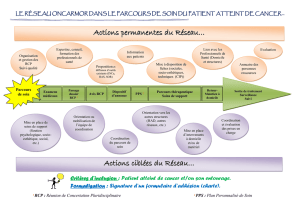
5'")*'#367&(.%(8$"#9#:*(+)','")#3'#.(#;$%.'%*#

MÉTHOXYFLURANE
Caractéristiques
Historique
Mode d’action
Pharmacocinétique

Méthoxyflurane
Un éther halogéné particulier 4,5,6
! Effet anesthésique à des doses élevées
! Propriétés antalgiques à faibles doses*
5(*(0)<*+/8=%'/#
• >+=%+3'#0.(+*#
• ?*'/=%'#+"0$.$*'#
• @$.(8.'#
• A3'%*#0(*(0)<*+/8=%'#
• 5.(//'#)1<*(-'%8=%'#B#(%)*'/#
("(.2</+=%'/#')#("8-C*<8=%'/#
7)1'*#1(.$2<"<##
METHOXYFLURANE
Caractéristiques
* Penthrox® est indiqué dans le soulagement d’urgence des douleurs modérées à sévères associées
à un traumatisme chez des patients adultes conscients
4. D5?#?'")1*$4EF# 5. :$,+#GH#
"#-+>8-
I.)'*(8$"#$J#-(+"#)1*'/1$.3#("3#-/C01$,$)$*#*'/-$"/'#(//$0+()'3#K+)1#/%L("('/)1'80#0$"0'")*(8$"/#$J#+"1(.(8$"#("'/)1'80/#+"#1%,("/
8-?*-@-A,+"B#C-
MNNOPQRSTUB#TVWXVTF##
6. 5$Y'C#ZH#
"#-+>8-
[:A?\B#(#*("3$,+/'3H#3$%L.'XL.+"3H#-.(0'L$X0$")*$..'3#/)%3C#$J#)1'#']0(0C#("3#/(J')C#$J#,')1$4C^%*("'#J$*#)1'#)*'(),'")#$J#(0%)'#-(+"F#
0!"*D-E"F-@8-
_RMWPOMSVUBTMOXVF#`)%3'#&'*/<'#a#.6Ibb#')#(%#
3$//+'*#3'#)*("/-(*'"0'F#

Méthoxyflurane
Son passé d’anesthésique
#MNT_# #MNTT#MNQR/#
Lancement comme
anesthésique inhalé7
Cas de
néphrotoxicité
post-opératoire
rapportés8
Effet antalgique au-delà de la période post-opératoire,
qui permet de réduire les besoins en opioïdes 5,6
OBSERVATION
CLINIQUE
METHOXYFLURANE
Historique
Diminution de
l’utilisation du
méthoxyflurane comme
anesthésique en raison du
risque de néphrotoxicité et
de la disponibilité de
nouveaux agents9
5. :$,+#GH#
"#-+>8-
I.)'*(8$"#$J#-(+"#)1*'/1$.3#("3#-/C01$,$)$*#*'/-$"/'#(//$0+()'3#K+)1#/%L("('/)1'80#0$"0'")*(8$"/#$J#+"1(.(8$"#("'/)1'80/#+"#1%,("/
8-?*-@-A,+"B#C-
MNNOPQRSTUB#TVWXVTF 6. 5$Y'C#ZH#
"#-
+>8-
[:A?\B#(#*("3$,+/'3H#3$%L.'XL.+"3H#-.(0'L$X0$")*$..'3#/)%3C#$J#)1'#']0(0C#("3#/(J')C#$J#,')1$4C^%*("'#J$*#)1'#)*'(),'")#$J#(0%)'#-(+"F#
0!"*D-E"F-@8-
_RMWPOMSVUBTMOXVF#`)%3'#&'*/<'#a#.6Ibb#')#(%#
3$//+'*#3'#)*("/-(*'"0'F##7. ?1(*,(0'%80(.#,("%J(0)%*+"2#'"0C0.$-'3+(F#:1+*3#'3+8$"F#@$.%,'#WB#cXdH#e"0+3'/F#_RRQF#f+..+(,#I"3*'K#?%L.+/1+"2H#g$*K+01H#D$C(%,'X!"+F##8. b(hh'#DeF#Z.%$*+"()'3#
("('/)1'80#"'-1*$)$4+0+)CB#("#%-3()'F#
G+,-A,+"B#$-H%:-@8-
MNVWP#OMSOUBiMTX__F#9. ;(C("#I;F#I"(.2'/+0#!/'#$J#e"1(.'3#b')1$4C^%*("'B#7&(.%(8$"#$J#+)/#?$)'"8(.#g'-1*$)$4+0+)CF#
3)!-0&I-2%&9:%>
H#
_RMTPOiSMUB#NMXMRR

Méthoxyflurane
Son héritage antalgique9
!8.+/(8$"#3%#,<)1$4C^%*("'##
a#J(+L.'#3$/'#!gec!7b7g:#
'"#)(")#=%6(")(.2+=%'#01'h#.'/#
-(8'")/#0$"/0+'")/#'"#I%/)*(.+'#
')#'"#g$%&'..'Xd<.("3'#
E"F9:+>-J"K">%I!",#B-<,#"*,+L%,+>-=9!9#"FC-
;9:#%*9+C-A)B#*+>9"-
Utilisation fréquente depuis 20 ans
MNQi#
?(*#'4',-.'#B##
• !*2'"0'/#-*<X1$/-+)(.+j*'/#
• !*2'"0'/#+")*(X1$/-+)(.+j*'/#
• !*2'"0'/#,+.+)(+*'/#
#
METHOXYFLURANE
Historique
7"#Z*("0'H#?'")1*$4E#'/)#+"3+=%<#3("/#.'#/$%.(2','")#3'/#3$%.'%*/#,$3<*<'/#a#
/<&j*'/#(//$0+<'/#a#%"#)*(%,(8/,'#01'h#3'/#-(8'")/#(3%.)'/#0$"/0+'")/F##
9.#;(C("#I;F#I"(.2'/+0#!/'#$J#e"1(.'3#b')1$4C^%*("'B#7&(.%(8$"#$J#+)/#?$)'"8(.#g'-1*$)$4+0+)CF#
3)!-0&I-2%&9:%>
H#_RMTPOiSMUB#NMXMRRF#
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
1
/
39
100%