La Douleur

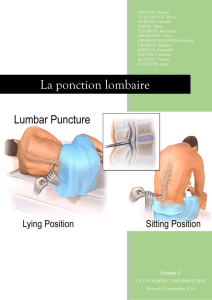
La rachianesthésie
1 Définition
La rachianesthésie est une ponction lombaire avec administration d'un anesthésique
local dans le liquide céphalorachidien (LCR).
Cette technique n'étant pas ou peu utilisée en médecine vétérinaire, il apparaît
indispensable de la présenter en médecine humaine, avant de d'exposer la technique chez les
animaux, notamment chez les bovins.
2 La rachianesthésie en médecine humaine
2.1 Historique
A Kiel, le 16 août 1898, le chirurgien Auguste Bier (1861-1949) injectait par voie
lombaire 3 ml de cocaïne à 0,5% dans l'espace sous arachnoïdien d'un homme de 34 ans,
tuberculeux. Il attendit 20 minutes et réséqua l'articulation de la cheville gauche de son patient
sans aucune plainte ou manifestation douloureuse de celui-ci. La moitié inférieure du corps
était totalement "insensibilisée": c'était la première anesthésie rachidienne chirurgicale.
Publiée en 1899 (Bier, 1899), cette observation complétée par sept autres anesthésies
rachidiennes, dont une pratiquée sur lui-même et une sur son assistant Hildebrandt, entraîna
un grand enthousiasme en France et aux Etats-Unis. Bier fut déclaré l'inventeur de la
technique.
Cependant, dès 1901, Léonard Corning (1855-1923), neurologue américain, contesta la
priorité du chirurgien allemand dans le domaine de l'anesthésie rachidienne. En fait, en 1885,
Corning avait publié "a spinal anesthesia and local medication of the cord" (Corning, 1885)
pratiqué sur un homme par injection locale de cocaïne après l'avoir pratiqué sur le chien. Ne
pouvant approcher la moelle sans enlever l'arc vertébral postérieur, Corning injecta la solution
de cocaïne dans l'espace inter-épineux D11-D12 en espérant que la cocaïne serait absorbée
par les petites veines qui longent le canal vertébral et transportée jusqu'à la moelle. Il obtint au
bout de vingt minutes une anesthésie des membres inférieurs, de la région lombaire et des
organes génitaux externes, sans pénétrer dans l'espace sous-arachnoïdien. Sans doute venait-il
de réaliser la première anesthésie péridurale.
La comparaison des deux observations historiques de Bier et de Corning permet
d'établir une différence fondamentale.
Tableau II : Comparaison des méthodes de Bier et Corning
BIER (1898) CORNING (1885)
Site d’injection Ponction lombaire Injection inter-épineuse
Présence de LCR + 0
Dose de cocaïne 15 mg 120 mg
Délai d’action Entre 2 et 12 minutes > 15 minutes
Effets secondaires
Vomissements
sévères
Céphalées
Céphalées violentes
Vertiges légers
44

Il s'agit donc d'une anesthésie rachidienne pour Bier et d'une anesthésie extra durale
pour Corning. Ceci est d'autant plus certain que la ponction lombaire, découverte
simultanément par Winter en Angleterre et Quincke en Allemagne en 1891, n'était pas connue
de Corning. La technique de Bier connaît alors un immense succès, tant en Allemagne qu'en
France et aux Etats-Unis.
En France, en mai 1899, Sicard expérimente les injections intraratéchales de nombreux
produits chez l'homme et le chien, y compris la cocaïne.
En novembre 1899, le chirurgien Tuffier publie la description magistrale de
"l'anesthésie médullaire chirurgicale par injection sous-arachnoïdienne lombaire de cocaïne"
(Tuffier, 1899) s'appuyant sur la méthode de Bier. Il décrit de façon exhaustive et illustrée
toutes les étapes de la procédure : le matériel utilisé (aiguille de platine et seringue de Pravaz),
la préparation et la stérilisation de la solution de cocaïne, la technique opératoire avec la
position du patient, les repères anatomiques et les gestes du chirurgien, la dose injectée, le
délai d'action, le niveau d'analgésie, les incidents et échecs, les accidents (surtout les
vomissements et les céphalées postopératoires), les indications (chirurgie des membres
inférieurs et du petit bassin), les contre-indications (les femmes hystériques et les enfants). Il a
déjà opéré 60 patients devant des collègues français ou étrangers qui le considèrent comme le
brillant champion de l’anesthésie rachidienne.
En décembre 1899, Matas publie la première anesthésie spinale américaine qu'il réalise
à la Nouvelle Orléans. Il fut également le premier à injecter de la morphine (en quantité
infinitésimale) associée à la cocaïne dans l'espace sous-arachnoïdien. En 1900, il précise les
indications de l'anesthésie rachidienne. Il retient les patients devant subir des interventions
pour lesquels l'anesthésie locale ou locorégionale est insuffisante, les insuffisants respiratoires
et les opérations de durée inférieure à 1h30.
Puis Goldan, également américain, se préoccupe d'avoir un matériel adéquat,
performant et spécifique à l'anesthésie rachidienne et insiste sur la nécessité d'obtenir des
observations complètes relatant le déroulement de chaque cas pour pouvoir évaluer la
méthode. Il propose des critères de surveillance toujours en vigueur de nos jours.
Enfin, les statistiques arrivent et les accidents publiés font reculer Bier lui-même qui ne
comprend plus l'enthousiasme de Tuffier. Six ou huit morts sont à déplorer sur deux mille
injections sous-arachnoïdiennes alors que l'on relève un mort sur deux mille
chloroformisations et un sur sept mille éthérisations d'après Reclus.
En conclusion, dans le tournant du siècle, la technique et les complications de la
rachianesthésie sont connues et décrites. Les auteurs s'accordent sur l'origine des céphalées
postopératoires comme étant bien la fuite du LCR et essaient de la limiter. Le mécanisme
d'action des anesthésiques locaux et la physiologie de l'anesthésie rachidienne restent à
explorer. La mise au point d'autres anesthésiques locaux sera nécessaire. La prévention et le
traitement des complications seront à inventer. Mais déjà, les perspectives d'avenir paraissent
immenses à ces chirurgiens souvent confrontés à une anesthésie générale par l'éther ou le
chloroforme qu'ils ne maîtrisent pas et leur donne de "terribles alertes".
L'anesthésie rachidienne leur apparaît comme "simple, facile, prompte et sans danger,
nécessitant des doses infinitésimales de poison et permettant une restitution ad integrum qui
se fait graduellement, métamériquement et d'une manière complète" (Cadol, 1900).
45

2.2 Anatomie humaine
(d’après Adams, 2001)
2.2.1 Structures ostéoligamentaires
La colonne vertébrale se compose de 33 vertèbres séparées par des disques
intervertébraux.
De nombreuses structures ligamentaires participent à la stabilité du rachis.
Dorsalement, on rencontre, de la superficie à la profondeur le ligament surépineux et les
ligaments jaunes qui limitent en arrière le canal rachidien.
Ligament
interépineux
Trou
intervertébral
Disque
intervertébral Ligament commun
p
ostérieu
r
Ligament
surépineux
Ligament
commun
antérieur
(D’après Adams, 2001)
Figure 5 : Structure ligamentaires de la colonne vertébrale (vue latérale)
46
Ligament commun
p
ostérieu
r
Ligaments jaunes
Disque intervertébral
(D’après Adams, 2001)
Figure 6 : Structures ligamentaires de la colonne vertébrale (vue dorsale,
ligament surépineux retiré)

2.2.2 Contenu du canal rachidien
La moelle épinière s’étend de la première vertèbre cervicale à la deuxième vertèbre
lombaire. Dans le canal rachidien, la moelle et les racines sont protégées par les enveloppes
méningées.
La pie-mère est un feuillet très fin et richement vascularisé qui adhère étroitement à la
moelle et aux racines qu’elle suit jusqu’à leur émergence du trou intervertébral qu'elle suit
jusqu'à leur émergence du trou intervertébral.
Latéralement de chaque côté de la moelle, la pie-mère envoie une expansion jusqu'à la
dure-mère, sur laquelle elle se fixe de façon discontinue, pour former le ligament dentelé qui
sépare de chaque côté les racines antérieures des racines postérieures.
La dure-mère est une membrane fibreuse épaisse qui tapisse le canal rachidien jusqu'au
sacrum. Elle est séparée des vertèbres par un espace graisseux très riche en vaisseaux: l'espace
péridural. La dure-mère est traversée par les nerfs rachidiens qu'elle engaine jusqu'à la sortie
du trou intervertébral. La face interne de la dure-mère est tapissée par une fine membrane,
l'arachnoïde, dont elle est séparée par un espace virtuel. L’arachnoïde est séparée de la pie-
mère par un large espace rempli de liquide céphalorachidien (LCR) : l'espace sous-
arachnoïdien.
(d’après Lee et Atkinson)
Figure 7 : Colonne vertébrale au niveau L3-L4 (coupe longitudinale, vue latérale)
L’espace compris entre le cône
terminal de la moelle (L2) et l'extrémité
inférieure du sac dural est occupé par les
derniers nerfs lombaires et les nerfs
sacrococcygiens constituant la queue de
cheval.
Figure 8 : Vue postérieure au niveau lombo-sacro-coccygien (coupe longitudinale)
Dure-mère et Arachnoïde
Ligament jaune
Espace péridural
Ligament interépineux
Ligament surépineux
Dure-mère
Cône terminal de la
moelle
Queue de cheval
(D’après Adams, 2001)
47

48
2.3 Indications et contre-indications
2.3.1 Indications
Les indications de la rachianesthésie dépendent du type d'intervention, de sa durée et de
l'état général du patient.
Classiquement, la rachianesthésie est indiquée pour les interventions sous ombilicales,
notamment la chirurgie portant sur le périnée.
Le sujet restant conscient pendant l'intervention, elle permet dans la chirurgie
endoscopique vésicoprostatique de déceler les symptômes de résorption du liquide d'irrigation
ou les perforations vésicales.
La chirurgie des membres inférieurs est une très bonne indication de la rachianesthésie
qui diminue le saignement per opératoire et participe à la thromboprophylaxie.
La rachianesthésie induit un bloc moteur qui peut se révéler utile dans la chirurgie
pariétale abdominale.
Les avantages de la rachianesthésie en obstétrique reposent sur la simplicité de la
technique, la rapidité d'installation, la qualité du bloc moteur associé au bloc sensitif et
l'utilisation de faibles doses d'anesthésiques locaux, ce qui minimise le risque fœtotoxique.
Pour une césarienne, le bloc doit être étendu (T4 à S5). Les manœuvres intra-utérines
sont possibles avec un bloc moins étendu (T10 à S5).
La rachianesthésie peut se révéler particulièrement utile dans certaines pathologies:
asthme, hyperthermie maligne, porphyries, myopathies, allergie, insuffisances rénale et
hépatique.
2.3.2 Contre indications
La rachianesthésie est formellement contre-indiquée dans les situations suivantes :
• Le refus du patient,
• l'exceptionnelle allergie aux anesthésiques locaux de type amino-amides,
• l'état de choc,
• l'hypovolémie,
• l'hypertension artérielle instable,
• l'insuffisance cardiaque décompensée,
• le rétrécissement aortique ou mitral serré,
• l'hypertension intracrânienne,
• l'infection au voisinage du point de ponction,
• les troubles de l'hémostase,
• l'urgence obstétricale avec instabilité hémodynamique.
Un terrain migraineux, une affection neurologique évolutive ou une chirurgie
rachidienne antérieure sont des contre-indications relatives. Il faut dans ces cas évaluer le
rapport risque/bénéfice de la rachianesthésie pour chaque patient.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
1
/
15
100%