Risque embolique des endocardites infectieuses

Revue
Risque embolique
des endocardites infectieuses
Gilbert Habib
1
, Ariel Cohen
2
1
Hôpital de la Timone, département de cardiologie, boulevard Jean-Moulin, 13005 Marseille
2
Hôpital Saint-Antoine, service de cardiologie, 184, rue du Faubourg Saint-Antoine,
75012 Paris
Résumé
Les embolies constituent une complication fréquente et grave (20 à 40 % des cas) de
l’endocardite infectieuse et sont associées à une morbidité et une mortalité élevées. Les
embolies peuvent cependant être silencieuses dans 20 % des cas et doivent être recherchées
par des examens non invasifs systématiques. La prédiction du risque embolique est un enjeu
majeur dans l’endocardite infectieuse, car elle peut conduire à proposer un traitement
chirurgical précoce pour prévenir ce risque. La prédiction individuelle du risque embolique
reste très difficile, mais les prédicteurs de risque les plus puissants sont la taille et la mobilité de
la végétation mesurées en échocardiographie. La valeur de 15 mm doit être retenue, car elle
est associée à la fois à un risque embolique majoré et à un mauvais pronostic, mais le risque
embolique est majoré pour les végétations de longueur supérieure à 10 mm. L’échocardiogra-
phie joue donc un rôle capital pour le diagnostic, mais aussi pour l’évaluation du risque
embolique et du pronostic dans l’endocardite infectieuse.
Mots clés : endocardite infectieuse, échocardiographie, embolie, pronostic, végétation
Abstract. Embolic events in infective endocarditis
Embolic events are a frequent and life-threatening complication of infective endocarditis and
are associated with a high morbidity and mortality. Embolic events may be silent in 20 % of
patients and detected only with systematic non invasive imaging. The prediction of embolic
risk is crucial in infective endocarditis and may lead to early surgical management. However,
the individual prediction of the embolic risk remains a challenge. The best predictors of
embolism are the size and mobility of vegetations, as measured by two-dimensional echocar-
diography. Large vegetations (> 15 mm) are associated with both a higher risk of embolic
events (already for vegetation length > 10 mm) and death. Thus, echocardiography plays a key
role in the diagnostic and prognostic assessment of patients with endocarditis, and in the
prediction of embolic events.
Key words: infective endocarditis, echocardiography, embolism, prognosis, vegetation
Les embolies constituent une des
plus graves complications de l’en-
docardite infectieuse (EI) [1]. Elles sont
en rapport avec la migration de végé-
tations valvulaires dans la circulation
générale. Malgré des modifications
épidémiologiques importantes [2] et
des progrès considérables dans le do-
maine du diagnostic et du traitement
de l’EI, les complications emboliques
restent fréquentes et associées à une
morbidité et une mortalité élevées [3].
La prédiction du risque embolique est
donc un enjeu majeur dans l’EI [4].
L’échocardiographie occupe une
place privilégiée dans la prise en
charge de l’EI, à la fois pour son éva-
luation diagnostique et pronostique.
L’apport de l’échographie transœso-
phagienne (ETO) a encore amélioré sa
sensibilité et sa spécificité. La valeur
de cet examen pour prédire le risque
embolique reste cependant débattue.
m
t
c
Tirés à part : G. Habib
mt cardio 2005 ; 1 : 236-42
mt cardio, vol. 1, n° 3, mai-juin 2005
236
Copyright © 2017 John Libbey Eurotext. Downloaded by a robot coming from 88.99.165.207 on 25/05/2017.

Le but de cette revue est de faire le point sur le risque
embolique actuel dans l’EI, d’en rappeler les déterminants
et de préciser le rôle de l’échographie dans son évaluation
et sa prévention.
Incidence et conséquences
des accidents emboliques
dans l’endocardite infectieuse
Les événements emboliques (EE) sont associés à un
excès important de morbidité et de mortalité dans l’EI [3].
La fréquence des EE dépend de la localisation de
l’infection au sein des cavités cardiaques, alors que leurs
conséquences cliniques varient grandement en fonction
du siège de l’embolie. Les EE sont le plus souvent localisés
dans le cerveau et la rate pour les EI du cœur gauche, dans
les poumons pour les EI du cœur droit et sur pacemaker.
Les embolies cérébrales sont de loin les plus fréquentes,
parfois inaugurales, et associées au pronostic le plus mau-
vais ; leur incidence varie de 25 à 56 % selon les études
avec une mortalité de 21 à 81 % [5]. Les embolies coro-
naires sont également de très mauvais pronostic mais
exceptionnelles. À l’inverse, les embolies spléniques et
certaines embolies cérébrales sont fréquemment totale-
ment asymptomatiques et découvertes par des examens
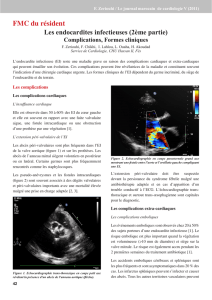
paracliniques systématiques [1] (figure 1).
L’incidence réelle des EE est inconnue, avec des esti-
mations allant de 10 à 50 % des EI [6-10]. Cette grande
disparité entre les séries a plusieurs explications :
–inclusion des embolies silencieuses ; leur incidence
a certainement été sous-estimée dans la littérature ; dans
notre expérience, sur une série de 178 endocardites
confirmées, une exploration scanographique cérébrale et
abdominale a été pratiquée systématiquement 95 % des
cas ; l’incidence des embolies observées est de 37 %,
parmi lesquelles 21 % sont des embolies silencieuses [1] ;
–inclusion des EE survenus avant le début du traite-
ment antibiotique. Si le risque embolique global est élevé,
le risque de survenue d’un accident embolique après
l’instauration du traitement antibiotique est beaucoup
plus faible, de l’ordre de6à21%[1,8,11-13], et ce
risque existe essentiellement durant les deux premières
semaines de traitement [7] ;
–attitude thérapeutique plus ou moins agressive selon
les centres et selon les périodes d’étude : la pratique d’un
traitement chirurgical plus fréquent et plus précoce dans
certains centres peut avoir modifié l’histoire naturelle de
l’EI [1] ;
–caractéristiques de la population étudiée : elles peu-
vent aussi interférer avec le risque embolique (âge, type de
cardiopathie sous-jacente prédominante, type de germes
rencontrés) ;
–enfin, la définition elle-même de l’EI a évolué avec le
temps et peut expliquer des disparités entre les études
[14-17].
Pour toutes ces raisons, l’incidence réelle des EE reste
inconnue et sera tantôt sous-estimée, tantôt surestimée
selon les études. L’estimation actuelle la plus exacte situe
ce risque embolique entre 30 et 50 % pour l’ensemble des
EE et entre 9 et 21 % pour les EE survenus sous traitement
antibiotique. Vu la fréquence des EE asymptomatiques et
l’influence potentielle de leur détection sur l’attitude thé-
rapeutique, leur dépistage systématique par scanner et/ou
échographie nous paraît souhaitable lorsqu’il est possible.
Liste des abréviations
EE : événements emboliques
EI : endocardite infectieuse
ETO : échocardiographie transœsophagienne
ETT : échocardiographie transthoracique
AB
Figure 1.Embolies splénique (A) et cérébrale (B) (flèches) asymptomatiques détectées au scanner au cours d’une endocardite infectieuse.
mt cardio, vol. 1, n° 3, mai-juin 2005 237
Copyright © 2017 John Libbey Eurotext. Downloaded by a robot coming from 88.99.165.207 on 25/05/2017.

Échocardiographie
et risque embolique
L’utilisation de l’échographie pour prédire le risque
embolique a fait l’objet de multiples travaux, de résultats
souvent contradictoires. Plusieurs caractéristiques des vé-
gétations ont été soupçonnées d’être associées à un risque
embolique plus élevé, comme leur présence, leur taille,
leur mobilité, leur localisation et leur échogénicité.
Présence d’une végétation
La visualisation échographique d’une végétation cons-
titue un critère diagnostique majeur d’EI (figure 2) [15] et
son diagnostic est le plus souvent aisé par l’échographie
transthoracique (ETT) ou l’ETO, dont la sensibilité dépasse
les 90 %. Dans la mesure où les EE sont liés à la migration
d’un fragment de végétation dans la circulation sanguine,
il paraîtrait logique de penser qu’il existe un lien entre
présence d’une végétation échographique et risque embo-
lique. Pourtant, la signification d’une végétation détectée
par l’échographie est longtemps restée controversée [1,
7-9, 18-21].
Les séries les plus anciennes, comme celles de Stec-
kelberg et al. [7] ou de Lutas et al. [18], n’ont pas trouvé de
lien statistique entre risque embolique et présence d’une
végétation. Il faut cependant noter que ces études n’utili-
saient que l’ETT et que certains des examens échographi-
ques étaient pratiqués après la survenue de l’EE ; certaines
végétations étaient donc probablement non détectables
parce qu’ayant déjà embolisé. Les études les plus récentes
utilisant systématiquement l’ETO ont décrit une incidence
de végétations beaucoup plus élevée et une corrélation
franche entre risque embolique et présence d’une végéta-
tion échographique [1-6]. La présence d’une végétation a
aussi été associée à un mauvais pronostic dans la série
récente de Wallace et al. [22].
Taille et mobilité des végétations
Si la relation entre taille et mobilité d’une végétation et
risque embolique paraît intuitivement évidente, cette sup-
position a fait l’objet de nombreux travaux dont les résul-
tats sont contradictoires, expliquant que les recommanda-
tions successives sur ce sujet soient également très
variables [5-9, 11-13, 22-29] (tableau 1).
Sans reprendre en détail toutes les études qui sont
résumées dans le tableau 1, leurs résultats discordants
trouvent de nombreuses explications, variant selon les
études : faible nombre de patients inclus, absence d’utili-
sation systématique de l’ETO, absence de recherche
d’embolies asymptomatiques, prise en compte des embo-
lies survenant avant l’institution du traitement, absence de
standardisation des critères diagnostiques [4].
Dans notre première étude [1], une relation statistique
forte a été observée entre taille des végétations et risque
embolique ; sur les 178 endocardites étudiées, un acci-
dent embolique a été noté dans 37 % des cas. En analyse
univariée, les facteurs significativement liés au risque em-
bolique plus élevé étaient la présence, la taille et la
mobilité de la végétation, les végétations du cœur droit et
les endocardites à staphylocoque. En analyse multivariée,
les seuls paramètres indépendamment et significative-
ment liés à un risque embolique majoré étaient la mobilité
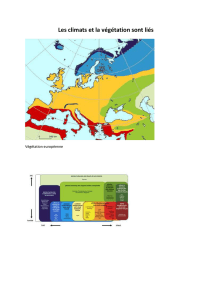
et la longueur de la végétation (figure 3). En revanche, le
siège aortique ou mitral de la végétation n’était pas discri-
minant. Il faut cependant noter que cette étude présentait
pour limitation importante d’inclure les EE survenant
avant et après initiation du traitement antibiotique.
Pour résoudre cette question, nous avons mené une
étude multicentrique incluant 384 patients étudiés pros-
pectivement, et étudié les EE survenant avant ou après
traitement [23]. Un EE a été observé chez 131 (34,1 %)
patients, dont 28 (7,3 %) après début de l’antibiothérapie.
Par analyse multivariée, les facteurs associés à un risque
de survenue d’un événement embolique sous traitement
VGVG
OGOG
AoAo
ABC
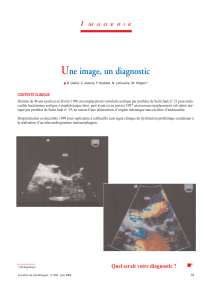
Figure 2.Végétations aortiques (flèches) en ETO : en systole (A) et diastole (B). C) Végétations aortiques (flèches) : aspects anatomiques chez le
même patient que les figures Aet B. VG : ventricule gauche, OG : oreillette gauche, Ao : aorte.
Risque embolique des endocardites infectieuses
mt cardio, vol. 1, n° 3, mai-juin 2005
238
Copyright © 2017 John Libbey Eurotext. Downloaded by a robot coming from 88.99.165.207 on 25/05/2017.

étaient la présence d’une végétation de longueur supé-
rieure à 10 mm (OR = 9) ou de mobilité importante
(OR = 2,4). Dans cette série, la présence d’une végétation
volumineuse ( > 15 mm) était également un facteur pro-
nostique indépendant puissant (risque relatif = 1,8,
p = 0,02), à côté des marqueurs pronostiques classiques
comme l’âge, l’existence d’une insuffisance rénale biolo-
gique, l’existence d’une insuffisance cardiaque ou une
atteinte d’origine staphylococcique [23]. La figure 4 mon-
tre ainsi que le risque de mortalité hospitalière augmente
avec la taille de la végétation, et la figure 5 montre que les
végétations de longueur supérieure à 15 mm sont égale-
ment associées à une mortalité à long terme plus élevée.
En résumé, l’expérience publiée cumulée plaide en
faveur d’un lien entre la taille de la végétation et le risque
embolique bien que, pour certains auteurs, ce risque soit
limité aux EI mitrales [21] ou staphylococciques [13]. Une
méta-analyse parue en 1997 confirme ces résultats [30].
L’échocardiographie participe donc à l’identification
d’une population à haut risque de complications et de
mortalité, et chez qui une attitude thérapeutique agressive
mérite d’être envisagée.
Localisation des végétations
Plusieurs études ont noté que la localisation mitrale de
la végétation était associée à un risque embolique majoré
[11, 12, 20]. Mügge et al. [11] avaient observé que le
risque d’EE associé aux végétations les plus larges n’était
observé qu’en cas de localisation mitrale, sans que les
raisons évoquées soient convaincantes [12]. D’autres étu-
des plus récentes n’ont pas confirmé cette observation.
Wallace et al. [22] ont montré que la localisation de la
Tableau 1.Relation entre taille de la végétation et risque embolique
Auteur Année Écho-
cardiographie
Patients
(n)
Végétations Embolies Embolies sous
traitement (%)
Relation entre embolie
et taille de la végétation
Lutas et al.
[18]
1986 ETT 77 56 22 ND Négative
Mugge et al.
[3]
1989 ETO 105 91 31 19 Positive
Sanfilippo et al.
[19]
1991 ETT 204 75 33 ND Positive
Steckelberg et al.
[7]
1991 ETT 207 38 13 13 Négative
Rohmann et al.
[12]
1992 ETO 118 42 26 21 Positive
Heinle et al.
[9]
1994 ETT 41 73 49 49 Négative
Werner et al.
[28]
1996 ETT 106 92 35 ND Positive
De Castro et al.
[8]
1997 ETO 57 80 44 44 Négative
Di Salvo et al.
[1]
2001 ETO 176 75 37 9 Positive
Cabell et al.
[27]
2001 ETO 145 80 23 11 Positive
Vilacosta et al.
[13]
2002 ETO 211 85 33 13 Positive
Thuny et al.
[23]
2005 ETO 384 83 34 7 Positive
90
80
70
60
50
40
30
20
10
0
90
80
70
60
50
40
30
20
10
0
% Embolies% Embolies
Mobilité de la végétationTaille de la végétation
9/45
17/66
10/24
30/43
12/53
9/52
11/31
34/42
Absente Absente Faible Modérée Sévère< 10 mm 10-15 mm > 15 mm
Figure 3.Risque embolique selon la taille et la mobilité de la végétation (d’après Di Salvo et al. [1] with permission from American College of
Cardiology Foundation).
mt cardio, vol. 1, n° 3, mai-juin 2005 239
Copyright © 2017 John Libbey Eurotext. Downloaded by a robot coming from 88.99.165.207 on 25/05/2017.

végétation n’influençait pas la mortalité dans une série de
208 patients. De la même façon, dans la série de 211 cas
de Vilacosta et al. [13], il n’y avait pas de différence
significative d’incidence d’EE selon la localisation de l’EI.
L’atteinte multivalvulaire a aussi été associée à un
risque embolique majoré et à un mauvais pronostic. C’est
le cas de la série de Wallace et al. [22] qui a observé une
atteinte multivalvulaire chez 20 (10 %) des 208 patients
étudiés, et montré qu’elle était associée à une mortalité
plus élevée à 6 mois. Rohmann et al. [12] ont montré que
les atteintes bivalvulaires étaient associées à un risque
d’EE de 50 % et à une mortalité de 10 %. Dans cette série,
les facteurs de risque embolique indépendants étaient la
localisation mitrale, la taille de la végétation supérieure à
10 mm, et l’atteinte bivalvulaire.
Autres marqueurs de risque embolique
échocardiographique
Peu d’études ont décrit l’évolution des végétations
sous traitement. Leur interprétation est délicate, car la
réduction de la taille d’une végétation peut être liée aussi
bien à la guérison de l’endocardite qu’à la migration d’une
partie de la végétation lors d’un EE. En outre, le traitement
chirurgical peut modifier l’histoire naturelle des végéta-
tions. Rohmann et al. [29] ont surveillé l’évolution écho-
graphique par ETO sous traitement antibiotique de 83 pa-
tients et montré que la persistance d’une végétation
volumineuse était associée à un risque embolique majoré.
À l’inverse, Vilacosta et al. [13] ont montré que la plupart
des végétations gardaient la même taille sous traitement
antibiotique, sans signification pronostique. Dans cette
étude, l’augmentation de la taille de la végétation sous
traitement, mais également la réduction de sa taille,
étaient associées à un risque majoré d’EE. On peut donc
conclure que l’augmentation de la taille de la végétation
sous traitement est probablement associée à un risque
embolique majoré, mais que sa stabilité ou sa régression
est d’interprétation plus délicate.
0
2
4
6
8
10
12
14
16
18
20
Mortalité hospitalière (%)
Absence ≤ 10 mm 10-15 mm > 15 mm
18/114
8/76
5/130
6/64
26/190
11/194
p = 0,008
Figure 4.Mortalité hospitalière en fonction de la taille de la végétation dans une population de 384 endocardites infectieuses (d’après Thuny
et al. [23] with permission from Lippincott, Williams and Wilkins).
0 100 200 300 400
Durée de suivi (jours)
1,0
0,8
0,6
0,4
0,2
0
Survie
84 ± 2%
69 ± 4%
L ≤ 15 mm
L > 15 mm
p = 0,001
Figure 5.Survieà1anchez384patients atteints d’endocardite
infectieuse selon la longueur de la végétation (L) (d’après Thuny et al.
[23] with permission from Lippincott, Williams and Wilkins).
Risque embolique des endocardites infectieuses
mt cardio, vol. 1, n° 3, mai-juin 2005
240
Copyright © 2017 John Libbey Eurotext. Downloaded by a robot coming from 88.99.165.207 on 25/05/2017.
 6
6
 7
7
1
/
7
100%