Evolution d`un système au cours d`une transformation chimique I

http://www.abderrazekseddik.sitesled.com/ 4
ème
Sc,M&T
1/6
Evolution d’un système au cours d’une transformation chimique
I/ Définitions
Un système chimique est une portion de l’Univers séparée par des
frontières réelles ou fictives bien déterminées.
Une phase est une portion homogène de l’Univers, qui présente les
mêmes propriétés en tous ses points (même indice de réfraction, même
température, même densité, même couleur, etc…..
Exemple : Solution saturée de sulfate de cuivre
Le système (S) est délimité par les parois du bécher et le
couvercle est constitué de trois phases
Une transformation chimique est tous processus au cours duquel
sont modifiées les quantités de matière de certains ou de tous les constituants
du système où elle se déroule, donnant ainsi à l’apparition des nouveaux
constituants.
II- Caractère rapide et lent des transformations chimiques
1/ Réaction rapide
a. Expérience
Lorsqu’on verse suffisamment de
solution soude sur la solution d’acide
chlorhydrique, la couleur du mélange
passe instantanément du jaune au
bleue.
b. Conclusion
La réaction entre la solution aqueuse d’acide chlorhydrique et la solution
aqueuse de soude est rapide.
c. Définition
Une Transformation chimique est dite rapide si la durée d’évolution du
système entre l’état initial et l’état final est inférieur à la percistance rétinienne
ou au temps de réponse des appareils usuels utilisés pour la suivre.
Autres exemples :
• Les réactions acide-base ;
• Les réactions de précipitation.
Solution
de NaOH
Solution
de HCl +B.B.T
Bleue Jaune
(S)

http://www.abderrazekseddik.sitesled.com/ 4
ème
Sc,M&T
2/6
2/ Réaction lente
On se propose de faire réagir une solution aqueuse d’iodure de potassium (K
+
+
I
-
) sur une solution aqueuse d’eau oxygénée H
2
O
2
en milieu acide.
a. Equation de la réaction
Les couples qui interviennent au cours cette réaction sont :
H
2
O
2
/H
2
O et I
2
/I
-
b. Expérience
Dès qu’on met les solutions en contacte, la
couleur du mélange devient jaune dans le
bécher (1). Cette couleur s’intensifie avec
l’augmentation de la concentration du
diiode. On prélève un échantillon de cette et
on lui ajoute quelques gouttes d’une solution
d’empois d’amidon. Le mélange prend une
couleur bleue.
c. Conclusion
La réaction entre la solution d’eau oxygénée H
2
O
2
et la solution aqueuse
d’iodure de potassium est lente.
d. Définitions
Une Transformation chimique est dite lente si elle se déroule sur des
durées permettant un suivi aisé avec nos sens ou avec les techniques de
mesures habituelles.
• L’étude d’évolution d’une réaction lente est appelée cinétique chimique.
III- Avancement d’une réaction chimique
L’avancement d’une réaction intéresse les réactions lentes
On considère la réaction chique symbolisée par l’équation.
aA + bB cC + dD
H
2
O
2
+ 2H
+
+ 2é 2H
2
O : réduction
2I
-
I
2
+ 2é : oxydation
H
2
O
2
+ 2I
-
+ 2H
+
2H
2
O + I
2
: équation bilan
Empois
d’amidon
Sol de H
2
O
2
+
quelques gouttes
de H
2
SO
4
Sol. de KI
Jaune
Bleue

http://www.abderrazekseddik.sitesled.com/ 4
ème
Sc,M&T
3/6
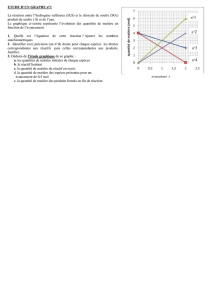
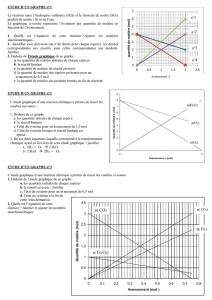
1/ Tableau descriptif d’évolution d’un système
Le tableau ci-dessous décrit l’évolution d’un système chimique ne renfermant
initialement que les réactifs A et B. On peut écrire provisoirement :
Etat du
système Quantité de matière en (mol)
initial n
0
(A)
n
0
(B) 0 0
Intermédiaire
n
(A) = n
0
(A)- n
d
(A) n(B) = n
0
(B) – n
d
(B) n(C)
n(D)
D’après la loi de conservation de la matière, on peut écrire :
Cte=
b
)B(n
=
a
)A(n
=
d
)D(n
=
c
)C(n
dd
. Cette constante est notée x appelée
avancement da la réaction exprimé en (mol). On peut reprendre le tableau
Intermédiaire
n
(A) = n
0
(A)- a.x n(B) = n
0
(B) – b.x c.x
d.x
Final n
f
(A) = n
0
(A)- a.x
f
n(B) = n
0
(B) – b.x
f
c.x
f
d.x
f
2/ Exemple
On reprend l’exemple de la réaction de la solution aqueuse d’iodure de
potassium (K
+
+ I
-
) sur la solution aqueuse d’eau oxygénée H
2
O
2
en milieu
acide et se propose de dresser le tableau descriptif d’évolution du système.
Etat du
système Avanceme
nt Quantité de matière en (mol)
initial 0 n
0
(H
2
O
2
)
n
0
(I
-
) -
-
0
Intermédiair
e x n(H
2
O
2
) = n
0
(H
2
O
2
) -
x n(I
-
) = n
0
(I
-
) –
2x -
-
x
Final x
f
n
f
(H
2
O
2
) = n
0
(H
2
O
2
) -
x
f
n
f
(I
-
) = n
0
(I
-
)-
2x
f
-
-
x
f
Si x = 1, on dit que la réaction a marché 1 fois. Si x = 0,5, on dit que la réaction
a marché 0,5 fois.
Déterminons l’avancement maximal en admettant que la réaction est totale. En
déduire la composition du mélange à l’état final. On Donne :
H
2
O
2
+ 2I
-
+ 2H
3
O
+
4H
2
O + I
2

http://www.abderrazekseddik.sitesled.com/ 4
ème
Sc,M&T
4/6
n
0
(H
2
O
2
) = 0,4 mol et n
0
(I
-
) = 0,1 mol
Lorsque la réaction est terminée (système à l'état final) l'un des réactifs (au
moins) a disparu. Ce réactif est appelé réactif limitant
L'avancement maximal x
max
est atteint lorsque la quantité de réactif limitant est
devenue nulle.
On fait l'hypothèse que chaque réactif est limitant et on calcule x
max
, le réactif
limitant est celui pour lequel x
max
est le plus petit, le premier atteint.
Si l’eau oxygénée est limitant X
max
= 0,4 mol
Si les ions iodures sont le réactif limitant X
max
= 0,05 mol
X
max
= 0,05 mol d’où la composition finale n(I
2
) = 0,05 mol, n(I
-
) = 0 mol
n
f
(H
2
O
2
) = 0,3 mol
Définition
L’avancement x d’une réaction chimique est une grandeur, exprimée en moles,
qui permet de suivre l’évolution de la composition d’un système au cours d’une
transformation chimique.
Remarques
Si les constituants du système chimique constituent une seule phase et le
volume V du milieu réactionnel est constant, on définit l’avancement
volumique y par
V
x
=y exprimé en mol.L
-1
3/ Quelques techniques de détermination de l’avancement x
Dosage
Conductimètrie
pH-mètrie lorsque l’un des réactifs ou produit est l’ion H
3
O
+
IV- Relation entre concentrations molaires des espèces chimiques
1/ Rappel
• Loi de conservation de la matière

http://www.abderrazekseddik.sitesled.com/ 4
ème
Sc,M&T
5/6
Au cours d’une réaction chimique, il ya conservation du nombre d’atome de
chaque espèce chimique
• Concentration molaire
La concentration molaire d’une espèce chimique A dans un mélange de
volume V est notée
[
]
A
.
[ ]
V
A
n
A
=
exprimée en mol. L
-1
.
Exemple
On dissout dans un volume V= 0,5 l d’eau, 0,2 mol de chlorure de plomb
PbCl
2
. on admet que cette quantité se dissout complètement.
On demande de :
• Déterminer la molarité de la solution.
• Déterminer les concentrations molaires des espèces chimiques présentes
dans le mélange autre que les ions H
3
O
+
et OH
-
.
2/ Relation entre concentration molaire
On se propose d’établir des relations entre les concentrations molaires
des espèces chimiques présentes dans le mélange à une date t quelconque.
[
]
[
]
[
]
[ ]
2
I2
0
I
v
x
2
n
I
2
I
0
2
O
2
H
v
x
1
n
2
O
2
H,
v
x
2
I
−
−
=
−
=
−
−=
−
==
H
2
O
2
+ 2I
-
+ 2H
+
2H
2
O + I
2
A t = 0s n
1
n
2
0
A t n
1
-x n
2
-2x x
 6
6
1
/
6
100%