Controverses sur la procréation médicalement assistée en Europe

CABINET Forum Med Suisse No14 2 avril 2003 338
Introduction
Des ovules sont récoltés dans l’Europe entière
pour être fertilisé in vitro, et les embryons qui
en sont issus, en fonction des différentes légis-
lations, sont implantés dans l’utérus dans les
6 jours.
En raison de différentes législations en Europe,
certaines techniques sont reconnues comme in-
dication médicale et considérées comme scien-
tifiquement supérieures dans certains Etats,
alors qu’elles sont interdites dans d’autres, ce
qui, entre autres, signifie que le taux de gros-
sesse par transfert d’embryon varie beaucoup
d’un pays à l’autre (tableau 1).
En illustrant les différences législatives concer-
nant la culture de blastocytes, les diagnostics
préimplantatoires (DPI) et le don d’ovules, nous
montrerons où se situent ces différences,
quelles conséquences elles entraînent pour les
patients en termes de taux de succès, de stress
physique, de charge financière. Nous esquisse-
rons les conseils médico-légaux que pourra
donner un médecin au couple en Suisse.
Culture de blastocytes
Le facteur décisif pour la réussite d’une fertili-
sation in vitro (FIV) avec ou sans injection intra-
cytoplasmatique de spermatozoïdes (IICS) est la
qualité des embryons transférés.
Seuls 40% des ovules fécondés avec 2 pro-nu-
cléus (PN) au maximum atteignent le stade
d’expansion d’un blastocyte au 5ejour après la
ponction folliculaire.
L’évaluation de la qualité de l’embryon n’est
possible que par l’observation de la vitesse de
développement et de la morphologie des diffé-
rents stades embryonnaires.
En Suisse et en Allemagne, les deux pays avec
la législation la plus restrictive sur la procréa-
tion médicalement assistée, seuls 3 ovules choi-
sis au stade pré-nucléus au maximum peuvent
se développer en embryons et doivent être im-
plantés, indépendamment de la qualité bonne
ou mauvaise de leur développement. Une cul-
ture allant au-delà de 2 jours n’a pas de sens,
car une sélection n’est licite à aucun moment.
Les trois premiers cycles de mitoses de l’em-
bryon précoce dépendent de signaux enregis-
trés dans l’ovule. Au 3ejour après la ponction
Controverses sur la procréation
médicalement assistée en Europe
Herbert Zech, Nicolas Zech
Tableau 1. Situation juridique en Europe.
A l’étranger sont autorisées beaucoup de pratiques de procréation médicalement assistée qui sont
strictement interdites en Allemagne.
Maternité Don d’ovule Diagnostic Transfert de
de substitution préimplantatoire blastocytes
Belgique pas interdit oui oui oui
Danemark interdit oui oui oui
Allemagne interdit interdit interdit pas pratiqué
France interdit oui oui oui
Grande-Bretagne oui oui oui oui
Italie pas interdit oui oui oui
Pays-Bas pas interdit oui oui oui
Autriche interdit interdit interdit oui
Espagne interdit oui oui oui
Suède interdit interdit oui oui
Suisse interdit interdit interdit pas pratiqué
Tchéquie interdit oui oui oui
Sources: MPI für ausländisches und internationales Strafrecht, Fribourg. Etat 2001.
Liste des abréviations utilisées:
IICS: injection intra-cytoplas-
matique de spermatozoïdes
FIV: fertilisation in vitro
DPI: diagnostic préimplantatoire
PN: pro-nucléus
PCR: polymerase chain reaction
Institute für Reproduktions-
medizin und Endokrinologie,
Bregenz (A), Meran (I),
Niederuzwil (CH)
Correspondance:
Pr Herbert Zech
Römerstrasse 2
A-6900 Bregenz

CABINET Forum Med Suisse No14 2 avril 2003 339
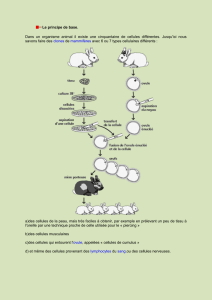
folliculaire, l’embryon se trouve normalement
au stade de 8 cellules, les réserves d’énergie
originaire de l’ovule diminuent, les produits de
l’activation du génome de l’embryon augmen-
tent (figure 1).
La culture de blastocytes offre une possibilité
excellente, simple, non invasive, de choisir les
meilleurs embryons pour le transfert. Elle per-
met d’identifier à temps les embryons les plus
vitaux avec une bonne vitesse de mitoses de
ceux qui souffrent d’un blocage de développe-
ment [1].
Ce blocage de développement peut être dû à
des facteurs paternels (qualité du sperme) ou
maternels (qualité de l’ovule) ou secondaire-
ment à des problèmes cytogénétiques. Il semble
être corrélé avec le moment de l’activation du
génome et/ou avec la production de super-
oxydes toxiques et de radicaux libres pouvant
survenir lors de cultures in vitro.
H. W. Michelmann écrit dans l’éditorial de la
revue «Reproduktionsmedizin» sous le titre
«L’échec programmé» [2]: «Les taux de gros-
sesse par embryon transféré sont, en Alle-
magne et en Suisse, les pays ou la sélection des
embryons est interdite sur base de critères
morphologiques ou biochimiques, si insatisfai-
sants (FIV = 22,6%; IICS = 23,5%), qu’il faut
sérieusement envisager si l’on doit renoncer à
traiter des couples désirant des enfants. Cette
question est justifiée, si l’on compare les taux
allemands et suisses avec les taux obtenus à
l’étranger allant jusqu’à 80% de grossesse par
embryon transféré. Il faut en plus garder à
l’esprit qu’un traitement par IICS coûte jusqu’à
10000 DM pour les couples devant l’assumer
eux-mêmes sans même obtenir un traitement
optimal.»
Cette situation est due à la Loi fédérale sur la
procréation médicalement assistée (LPMA) (en
Suisse) et la Loi sur la protection des embryons
(en Allemagne) avec leurs annexes correspon-
dantes. Ce sont les contraintes de ces légis-
lations qui engendrent les dilemmes évoqués
dans ces deux pays et qui programment les
échecs! Comme le choix de blastocytes en ex-
pansion à partir d’un pool d’embryons en voie
de développement n’est pas possible en Suisse
et en Allemagne, il faudra dans ces deux pays
vivre aussi à l’avenir avec des taux de grossesse
de moins de 30%!
La synchronisation entre l’embryon et la récep-
tivité de l’utérus est optimale lors d’un transfert
au 5ejour. Le nombre des embryons à trans-
férer peut être diminué en raison de leur meil-
leure qualité. En plus des avantages du choix
des meilleurs embryons pour le transfert, la
culture des blastocytes ouvre la possibilité
d’effectuer au 3ejour une biopsie sur plusieurs
cellules dans le cadre du diagnostic préimplan-
tatoire, permettant de déceler des anomalies et
de transférer des embryons normaux après
leur développement au stade de blastocyte [3].
«La règle de trois» en Suisse et en Allemagne
est la suivante:
– culture de seulement 3 zygotes
– développement de 3 embryons au maximum
– transfert au jour 2 ou 3.
Cela signifie:
– Un choix d’embryon parmi une culture de
blastocyte suivi de diagnostic préimplanta-
toire n’est pas permis.
– Une augmentation significative du taux de
grossesse (jusqu’au facteur 2) et du taux
d’implantation (jusqu’à 50% par blastocyte)
avec le transfert de seulement 1–2 blas-
tocytes n’est pas possible.
– Un taux de grossesse de 80% est obtenu avec
le transfert de 1–2 embryons au stade de
blastocytes. Le risque de triplé lors de trans-
fert de 3 embryons est évité, il suffit même
Figure 1.
Développement de l’embryon du
jour 0 au jour 5 avec diminution
des éléments ovulaires et
augmentation des produits
de l’activation du génome de
l’embryon (autorisé à la reproduc-
tion par J. Fertil. Reprod. 2/2001).
(Embryonale-Entwicklung
= Développement de l’embryon)
(Eizellbestandteile
= Eléments ovulaires)
(Embryobestandteile
= Eléments embryonnaires).

CABINET Forum Med Suisse No14 2 avril 2003 340
souvent de transférer un seul embryon. Ce
sera le standard de la technique à l’avenir.
– Pas de réduction du taux d’avortement et du
nombre de cycles de traitement infructueux,
réduisant ainsi le fardeau psychique des pa-
tients (et le fardeau financies).
Diagnostic préimplantatoire (DPI)
La méthode actuellement disponible de DPI
permet d’analyser les globules polaires des
blastomères et de trophoblastes. Elle permet
non seulement d’améliorer le taux de gros-
sesse, mais aussi d’éviter des avortements dans
de nombreux cas [4].
La Loi fédérale sur la procréation médicale-
ment assistée n’autorise pas la biopsie de l’em-
bryon, mais autorise la biopsie des globules
polaires c’est-à-dire la DPI des ovules.
Elle utilise la particularité biologique suivante:
une scission asymétrique de l’ovule survient
dans sa maturation, dans le sens que l’ovule
demeure entier et que chaque fois un set de
chromosomes est rejeté comme globule polaire.
Le premier globule polaire contient un set
double, le deuxième un set simple de chromo-
somes maternels. Leur présence permet d’affir-
mer que les scissions de maturation se sont
bien effectuées. L’avantage de l’analyse des
globules polaires est qu’elle est possible avant
la fertilisation, c’est-à-dire avant la conception
d’un embryon. Son inconvénient est qu’elle ne
permet de déceler que les anomalies mater-
nelles. Elle n’apporte rien en cas d’anomalie
paternelle. Elle ne permet pas non plus d’iden-
tifier des pathologies génétiques apparaissant
lors de la fusion des génomes.
Les aberrations chromosomiques des ovules
sont responsables pour la majorité des pertes
embryonnaires et fœtales [5]. Ces aberrations
peuvent être décelées par l’analyse des globules
polaires.
Le DPI des blastomères permet aussi de déter-
miner le sexe, ce qui peut être utile, par
exemple lors de maladie héréditaire liée au
sexe. Grâce aux méthodes d’analyse génétique
moléculaire, (par ex. PCR) des pathologies
monogénétiques peuvent être décelées tant sur
les globules polaires que sur les blastomères,
avant même le transfert de l’embryon.
L’interdiction suisse de DPI sur embryons incite
déjà dans de nombreux cas les couples concer-
nés à recourir au tourisme médical à l’étranger
et les incitera probablement encore davantage
à l’avenir, quand des techniques améliorées et
simplifiées seront disponibles. Les arguments
avancés par le Conseil fédéral contre le DPI, à
savoir qu’un diagnostic dans cette phase entraî-
nerait une confusion automatique entre une
éventuelle pathologie génétique et le rejet d’une
vie encore non-née, ne sont guère convain-
cants. Comment refuser le DPI, qui n’a pas son
pareil dans la palette des diagnostics préna-
taux, alors que l’avortement sciemment effec-
tué d’embryons sains est permis dans le cadre
de la loi et doit même être pris en charge par
les caisses d’assurance-maladie! L’argument
que le DPI est un jugement de vie ou de mort
pour la vie en éprouvette décrétant si elle mé-
Tableau 2. Quand commence la vie (à protéger)? Différentes perspectives.
La vie commence ...
selon Aristote (384–322 av. J.-C.), l’embryon masculin a une âme 40 jours après la fécondation,
l’embryon féminin après 90 jours
lors de la fusion du pronucléus féminin et masculin
à la première division cellulaire du zygote, quelques heures après la fécondation
à la nidification du blastocyte, le 12e–14ejour après la fécondation
quand la formation de jumeaux n’est plus possible (au max. 2 semaines après la fécondation)
après 4 semaines, quand le cœur bat
après 2 mois, quand le visage du fœtus ressemble à celui d’un primate
8 semaines après la fécondation, des ondes du cerveau, qui ressemblent à des rêves, pouvant être
enregistrées
après 3 semaines, le fœtus ressemblant à un bébé
après 4 mois, les traits individuels du visage devenant perceptibles
après 24 semaines environ, le fœtus étant capable de survivre hors de l’utérus (dans les conditions
optimales) – comparer avec la date tolérée pour l’avortement: seulement jusqu’à la 20e–21esemaine
après 24–27 semaines, le cortex cérébral étant connecté – c.-à-d. la pensée étant théoriquement
possible à partir du 6 emois
à la naissance seulement, présence de l’être humain

CABINET Forum Med Suisse No14 2 avril 2003 341
rite d’être poursuivie ou non est peut-être effi-
cace du point de vue rhétorique; mais les
couples atteints de maladies héréditaires ont de
la peine à comprendre que l’on refuse le diag-
nostic de l’embryon avant même l’implanta-
tion alors qu’un avortement d’une vie beaucoup
plus fermement établie, jusqu’au troisième
mois de grossesse, est autorisé!
La question de savoir quand la vie (devant être
protégée) commence (tableau 2) n’est absolu-
ment pas suffisamment approfondie dans ce
débat, elle n’est même pas abordée!
Don d’ovule
Indications au don d’ovule:
– ménopause précoce (1% environ des fem-
mes en âge de procréer)
– maladies génétiques
– maladies auto-immunes
– état après traitement oncologique.
Le don d’ovule est condamné selon la Loi fédé-
rale sur la procréation médicalement assistée,
alors que le don de spermatozoïdes est autorisé.
La raison de cette mesure discriminante pour
la femme n’est pas mentionnée.
Les ovules et les spermatozoïdes sont équiva-
lents du point de vue biologique. Il est cepen-
dant bien plus difficile de disposer d’ovules, un
seul ovule arrivant à maturité en moyenne lors
de cycles non-stimulés et devant être récolté
par une opération. Des stimulations pour ré-
colter un seul ovule sont éprouvantes tant
physiquement que psychiquement.
Des dons d’ovules seraient possibles dans le
cadre des «egg-sharings». Ils seraient dispo-
nibles quand 2–3 ovules sont récoltés dans le
cadre d’une fertilisation in vitro, et l’un d’entre
eux pourrait être mis à disposition d’une femme
ayant perdu sa fonction ovarienne, par ex.
après un traitement oncologique. Cette procé-
dure serait acceptée socialement, mais elle
demeure cependant interdite légalement.
Ce qui est permis dans la plupart des pays
européens, aux USA et outre-mer, est stricte-
ment interdit par les lois restrictives en Suisse,
en Autriche, en Allemagne et en Suède. Ceci
incite les couples concernés, à l’instar de la
situation pour le transfert de blastocytes, à re-
courir au tourisme médical à travers l’Europe
et outre-mer.
Au vu de ces différentes législations, la question
se pose de savoir quel peuple, quelle nation –
dans quelles circonstances et sous quelles
conditions culturelles – agissent le plus juste-
Tableau 3.
Quel peuple, quelle nation est moralement/éthiquement meilleure?
CH A D I F UK B USA
Don d’ovule –––+++++
Culture de blastocytes – + – +++++
Don de sperme + – (+) +++++
Avortement ++++++++
Peine de mort –––––––+
Euthanasie ––––––(+)–
Lois diverses
dépendant entièrement des lobbys ■démocratie ■
Quintessence
Seul le choix d’embryons à partir d’un grand pool d’ovules fécondés
conduit à une véritable amélioration du taux de grossesse (culture de blasto-
cytes).
Le diagnostic préimplantatoire dans le cadre de l’analyse des globules
polaires donne nettement moins de renseignements que l’analyse de
l’embryon.
L’interdiction du don d’ovules est considérée par beaucoup de femmes
concernées comme une discrimination (par ex. dans le cas de radiations,
chimiothérapie, ablation des ovaires pour une femme en âge d’avoir des
enfants).
Une modification de la Loi fédérale sur la procréation médicalement
assistée (LPMA) et une adaptation aux expériences internationales seraient
déjà appropriées, un an après l’entrée en vigueur de cette loi.
Références
1 Gadner DK, Lane M, Calderane I, Lee-
ton J. Environment of the preimplan-
tation human embryo in vivo: meta-
bolite analysis of oviduct and uterine
fluids and metabolism of cumulus
cells. Fertil Steril 1996;65:349–53.
2 Michelmann HW. Der program-
mierte Misserfolg: Dilemmasituation
der deutschen und schweizerischen
Reproduktionsmedizin. Reproduk-
tionsmedizin 2000;16:181–2.
3 Verlinsky Y, Kuliev A. Preimplan-
tation genetics. J. Assist. Reprod.
Genet. 1998;15:215–8.
4 Viville S, Ray P, Viville B, Handysi
de A, Gerlinger P. Preiimplantation
genetic diagnosis: techniques and
results. Med Sci 1996; 12:1378–88.
5 Baretton GB, Muller M, Wirtz A,
Murken J, Arnholdt H. Numerical
chromosoal aberrations in abortion
tissues: comparison of conventional
and interphase cytogenetics in paraf-
fin sections and nuclear suspensions.
Pathologe 1998;19:120–8.
.
.
.
.
1
/
4
100%