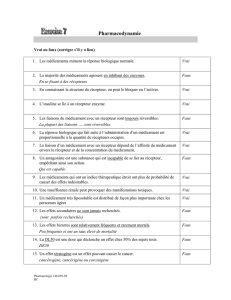
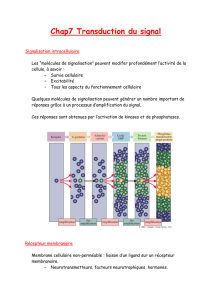
Communication intercellulaire

Communication intercellulaire
1- Introduction à la communication
a- Définitions
Rappel
!
Qu'est-ce que la matière vivante ?
La matière vivante est un ensemble de cellules qui est l'unité la plus petite du vivant, elle
est défini comme un espace clos (=compartiment), ce qui impose des échanges en
permanence entre la cellule et sont environnement pour :
- survivre
- être informer de ce qui ce passe dans les autres cellules.
La cellule ne vit pas dans un environnement stable, et elle ne vie pas seule.
Même les organismes unicellulaires échangent avec d'autres cellules.
Cette communication intercellulaire est indispensable a la vie. Membrane hémiperméable.
Il y a nécessité de communication.
Communiquer, échanger, changer d'état
La communication c'est pas seulement l'émission d'un signal il faut que le signal soit émis
par une cellule A, reconnus, et qu'il change l'état de la cellule B.
→ Toute communication doit être associée à un changement d'état (communication =
dynamique de la différence : gap jonction)
Les communications entre cellules vont avoir pour objet de rompre l'isolement de la
cellule, mettre en relation les cellules par des évènements et conduire ainsi a des
changements d'état.
Information = dynamique qui produit une différence.
C'est un gain, c'est une prise en compte d'information.
Une cellule ne peut pas vivre seule, il y a des échanges (délai de microsecondes), des
messages entre cellules qui vont l'informer des changements de l'environnement, mais
aussi des cellules voisines et éloignées, cette cellule reçoit et émet des messages.
Il n'y a pas d'intentionnalité, de projet, la cellule est simplement un acteur qui émet les
signaux qu'elle sait produire (hormone...). Communications à distances nécessitent des
signaux.
Les cellules communiquent en émettant des substances chimiques, des cellules vont être
capables de réceptionner ces substances grâce à des récepteurs.
Emetteur, message, récepteurs
Les 3 acteurs majeurs de la communication sont : émetteur/message/ récepteur
Il faut deux partenaires : l'émetteur (neurone par exemple) est capable de synthétiser et
de faire passer le message dans le milieu extra cellulaire, ce sont des signaux (molécules
libérées) qui vont acquérir la valeur de message grâce à la cellule réceptrice qui interprète
ce signal.
Le reconnaissance de ce signal par ce récepteur entraine un changement d'état de la
cellule. Et une cellule réceptrice qui va décoder le message, récepteur qui va reconnaitre
le signal.
Ces signaux passent d'une cellule a l'autre par le milieu extra cellulaire.
De l'influence du milieu

Le signal n'est pas émis dans un milieu neutre, il peut être modifié ou dégradé lors de son
passage à l'extra cellulaire, la molécule peut être changée, catalysée devenir active ou
inactive.
Le milieu extra cellulaire est un milieu actif, c'est un élément critique de la communication.
Il y a une pression permanente exercée par le milieu sur les cellules. Il y a peu de perte
dʼinformations.
Le rétro contrôle : un retour nécessaire
Il ne peut pas y avoir de véritable communication sans retour de la cellule réceptrice vers
l'émetteur.
La cellule A va émettre un signal reconnu par B qui va changer son état, et notifier à la
cellule A qu'elle a bien reçu son message (→ Retour nécessaire)
Ex : régulation de la glycémie, le retour à la normale de la glycémie qui entraine la baisse
de sécrétion d'insuline.
Un processus discontinu
Communiquer et exclure. Il faut que la communication soit stable (permanence).
L'émission de signaux et la réception ne sont pas constants. C'est la façon dont l'émission
des signaux va être organisée dans le temps qui est important.
→ La communication est un phénomène discontinu.
Le rapport signal bruit sur un récepteur entraine le contraste (zone silencieuse autour) et
discrimination. Si le bruit est trop important on ne distingue pas le signal (bruit de fond) ce
qui crée de la discrimination.
b- Principes généraux de la communication cellulaire
Communiquer et exclure
Phénomène d'exclusion : L'exclusion permet une meilleur qualité de l'information.
On ne peut pas faire communiquer tout le monde en même temps.
Effet de rapport signal/bruit.
Exemples :
- Hormones du pancréas, l'insuline est capable d'agir sur toutes les cellules.
- Dans le système nerveux central, tous les neurones ne reçoivent pas en même temps la
même information.
Les cellules réceptrices possèdent des récepteurs différents. Il y a pleiotropie, c'est à dire
un signal peut être reconnu par des récepteurs différents, ceci permet la synchronisation
des fonctions.
Permanence et discontinuité
La permanence et la discontinuité jouent un rôle très important au sein du système
nerveux central (potentiel d'action pendant 1sec n'est pas le même message que du
potentiel d'action pendant 5sec).
La langue des cellules nerveuses est le résultat de variations de potentiels d'actions, plus
il y a de potentiels d'actions, plus il y a de neurotransmetteurs libérés.
Mais suivant les variations, je n'aurai pas tout le temps les mêmes variations de potentiels
et donc pas tout le temps la même quantité de neurotransmetteurs.
Signal et bruit, contraste, discrimination

Le récepteur s'il ne connait pas l'hormone ou le neurotransmetteur, il restera silencieux, ce
qui favorise l'aspect de contraste, dont la discrimination. L'effet de contraste est important.
(rapport signal bruit.)
2- Codage et émission du signal
!
a- Synthèse, transport, stockage
Les cellules émettrices synthétisent, stockent et émettent.
La Cellule est un compartiment clos il y a donc discontinuité entre la cellule A et B avec
comme barrage la membrane plasmique.
Toutes les cellules sont formées de membranes lipidiques (membrane plasmique), il y a
des liaisons hydrophiles, et des liaisons hydrophobes. Les molécules hydrophiles ne
peuvent pas traverser cette membrane qui est hydrophobe, il y a donc des phénomènes
pour pouvoir permettre le passage de ces molécules hydrophiles.
Les molécules signales sont soit hydrophiles, soit lipophiles.
Exception: il a des cellules qui sont en continuité (jonctions communicantes) cellules qui
émettent des prolongements (micropores) ou jonctions gap, et qui permettent le transfert
de petites molécules ou ions. → la cellule n'est pas un espace totalement clos ici.
Les ligands hydrophiles
- Par empaquetage et exocytose de ces molécules dans le milieu extra cellulaire puis sur
les cellules réceptrices, il y a des récepteurs capables de transformer le signal en
message.
- Grâce aux jonctions communicantes qui sont associées à des jonctions de pores
membranaires, faites a partir de conexines qui forment un canal ouvert ou fermé, elles ne
laissent passer que des toutes petits molécules, et des ions.
Une cellule peut exciter très rapidement des milliers de cellules qui ainsi travaillent en
même temps.
Les ligand lipophiles :
Ces ligands sortiront et rentreront facilement dans les cellules car elles peuvent traverser
la membrane plasmique hydrophobe mais il faudra des navettes (hydrophiles) pour
transporter la molécules dans le milieu extra cellulaires car elle ne sont pas solubles dans
ce milieu (Milieu EC = hydrophile (sang)).
b- Libération de ces molécules signales
Exocytose
C'est un processus vésiculaire nécessaire pour faire sortir de la cellule les molécules
hydrophiles. La vésicule ne franchit pas directement la membrane.
Seuls les ligands hydrophiles, stockés dans des vésicules de sécrétion, sont libérés par
exocytose. Ce phénomène est contrôlé et dépend notamment de la concentration
calcique.
Le cas des molécules hydrophiles de type peptidique :
Les molécules (protéine) sont synthétisées au niveau de l'AG, puis sont mises dans un
compartiment aqueux. Elles sont ensuite empaquetées dans des vésicules avec des
étiquettes (V-SNAREs).

L'adressage des protéines est rendu possible grâce à la présence de signaux trans
membranaires, les V-SNAREs, qui sont des marqueurs indiquant la destination des
vésicules de sécrétion.
On a la formation de vésicules, qui vont se détacher de l'AG et en fonction de cet
étiquetage, elle vont dans tel ou tel lieu de la cellule (mitochondries, membrane plasmique
… ).
Les cibles spécifiques des V-SNAREs sont les T-SNAREs, situés sur la membrane. Les
molécules s'arriment là où elles peuvent être reconnues.
Mécanisme de l'exocytose :
Les V-SNAREs des vésicules, s'encrent dans les T-SNAREs de la membrane plasmique
ou de membranes intracellulaires (et pas ailleurs). Ce complexe (V-SNAREs + T-SNAREs)
recrute des cofacteurs :
- Des SNAPs : consolident la liaison du complexe
- Le NSF : ATPase nécessaire pour amorcer le processus de fusion des membranes
(elles sont capables d'hydrolyser de l'ATP et de libérer de l'énergie localement).
→ Ces deux molécules sont des molécules d'attachement. Ces deux molécules modifient
la conformation du complexe V-SNAREs T-SNAREs et l'interaction du complexe devient
alors très étroite, ce qui favorise le rapprochement de la vésicule, près de la membrane
sans fusion grace a la synaptotagmine. Cʼest un mécanisme dʼexocytose controlé.
La synaptotagmine vésiculaire ne participe pas à l'adressage mais participera au
processus d'exocytose lors de la fusion (molécule calcique dépendante. La concentration
cellulaire en calcium est faible)
La synaptotagmine, empêche la fusion totale, en effet lors de l'exocytose on ne perce pas
totalement la membrane.
Il faut un signal calcique, il va y avoir une brutale modification de la concentration intra
cellulaire grâce à des canaux calciques qui s'ouvrent pour laisser rentrer le calcium, la
concentration en calcium va être augmentée par 100. Le calcium se fixe sur les
synaptotagmine (protéine calcique dépendante) ce qui entraine une modification de sa
conformation et permettre la fusion de cet ensemble. Puis, il y a une dissociation des
phospholipides, le contenu des vésicules est libéré dans le milieu extra cellulaire.
Processus dʼexocytose controlé : calcium dépendant (émission dʼun signal discontinu). Et
une exocytose constitutive qui ne possède pas ces systèmes de controle, on a une
libération de facon permanente.
Endocytose
Après la libération du contenu de la vésicule, la membrane vésiculaire est totalement
incorporée a la membrane plasmique, les synaptotagmines ont une disposition trans-
membranaire.
La synaptotagmine recrute des molécules de clathrine, et se lient à elles, ce qui entraine
une déformation de la membrane car les clathrines forment des angles les unes avec les
autres et imposent progressivement une plicature a la membrane et la re-formation d'une
pré-vésicule grâce à la dynéine, il y a fission de la membrane.
Les clathrines se détachent des synaptotagmines et ainsi, la vésicule néoformée, migre
vers l'intérieure de la cellule, et les synaptotagmines sont de nouveau disponibles.
!
Shedding (effeuillage)
Ce macrophage est capable de synthétiser des protéines qui ne sont pas empaquetées
dans des vésicules mais sous forme de protéines trans membranaires (ex : TNF), ces

molécules sont sous forme de précurseur (molécule amphiphile) avec leur pôle hydrophile
vers l'extérieur.
On a un clivage par une protéase (enzyme), qui est capable de séparer le pôle hydrophile
du pôle hydrophobe de cette molécule. Le fragment issu du clivage est une molécule
informative comme par exemple le TNF alpha.
=> C'est un processus d'effeuillage, on a avec des phénomènes des molécules sécrétées
à partir de molécules trans membranaires, on a des molécules signales libérées dans le
milieu extra-cellulaire.
c- Inactivation
!
- Dégradation et recapture
Après avoir agi sur leurs cibles, les peptides et les amines vont être dégradés
enzymatiquement, ce qui aboutit à leur inactivation. Les mécanismes dʼinactivation
permettent ainsi de limiter le temps dʼaction de la molécule signal.
On en distingue principalement deux : la dégradation enzymatique et la recapture.
Exemple de la terminaison nerveuse : avec la libération de dopamine, molécule
hydrosoluble stockée dans des vésicules, il y a des neurones qui ont des récepteurs pour
cette dopamine. (fusion membranaire, libération de dopamine dans lʼespace EC, une
partie va etre recapturée par la cellule émettrice : système de cotransport inactivation du
signal)
La liaison de toute ces molécules signales avec leur récepteur se fait par affinité.
Les molécules sont recaptées par la cellule qui les a émises, pour etre restockées et
réutilisées.
Quand la concentration en dopamine chute : récupération
La majorité des molécules de dopamine sont récupérées.
Dans les conditions normales, la récupération.
Dans le cas de prise de cocaïne : La cocaïne bloque la recapture de la dopamine dans le
neurone pré synaptique. De ce fait, la dopamine libre demeure dans la fente synaptique
bcp plus longtemps.
Des enzymes : monoaminoexydases vont dégrader cette dopamine directement dans la
fente synaptique.
Pour des peptides on va avoir des peptidases qui vont dégrader le peptides en segments
+/- courts.
Un peptide de 15 aa peut etre découpés en fragments plus courts qui peuvent avoir une
autre activité.
- Shedding
Des enzymes (protéases) dans le milieu extra-cellulaire qui vont dégrader le récepteur,
elles peuvent aussi se fixer sur des récepteurs couplés au TNF.
d- Transfert du signal
On peut agir localement ou a distance
- Agir localement
Système autocrine : c'est un mode de transfert à proximité, la cellule peut agir avec des
cellules similaires et sur elle même, ceci permet une synchronisation et un auto contrôle
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
1
/
20
100%