Deux stress pour un coeur

CAS CLINIQUE
OBSERVATION
Madame M., 75 ans, est épileptique depuis 1953. Sous Gardé-
nal
®
,ses crises comitiales sont exceptionnelles, toujours provo-
quées par des contrariétés familiales. À la suite d’une dispute,
une nouvelle crise généralisée conduit la patiente aux urgences,
où elle présente une douleur rétrosternale à type d’oppression,
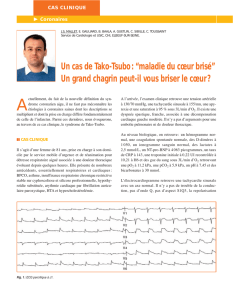
avec un électrocardiogramme (ECG) qui évolue vers un aspect
de nécrose myocardique en latéral haut (ondes Q en D1 et VL
avec ondes T négatives) et en antéroseptal (aspect QS en V1 et
V2 avec ondes T négatives) (figure 1). Le pic de troponine atteint
3 ng/ml.
La patiente est alors dirigée en cardiologie, où la coronarographie
réalisée en urgence est normale. La ventriculographie gauche met
en évidence une altération de la fonction systolique (fraction
d’éjection ventriculaire gauche [FEVG] = 41 %) en relation avec
une ballonnisation apicale du ventricule gauche (figures 2 a et b).
L’échocardiographie transthoracique effectuée le jour même
(figure 3) confirme une akinésie des deux tiers apicaux du ven-
tricule gauche avec une cinétique respectée au niveau de la col-
lerette basale ; la FEVG est estimée à 35 %, la pression artérielle
pulmonaire systolique à 50 mmHG, avec une élévation de la pres-
sion télédiastolique du ventricule gauche. On ne met pas en évi-
dence d’obstruction dynamique intraventriculaire gauche.
En unité de soins intensifs cardiologiques, où la patiente est ini-
tialement prise en charge, sous anticoagulation efficace, bêtablo-
quant et inhibiteur de l’enzyme de conversion (IEC), l’évolution
est rapidement favorable, sans instabilité hémodynamique. La sur-
veillance ECG objective la repousse des ondes R en latéral haut
et en antéroseptal avec la persistance d’ondes T négatives. L’écho-
cardiographie transthoracique contrôlée au cinquième jour est nor-
malisée (cinétique ventriculaire gauche homogène et normale,
FEVG = 55 %) (figure 4). Le dosage des normétanéphrines uri-
naires au deuxième jour d’hospitalisation est augmenté
(2 587 nmol/24 h, pour une normale < 2 183 nmol/ 24 h).
La Lettre du Cardiologue - n° 391 - janvier 2006
28
Deux stress pour un cœur
●
C. Adams, M. Goudjil, T. Carrères, B. Gallet, J.P. Saudemont*
* Service de cardiologie, CH Victor-Dupouy, Argenteuil.
Figure 1. ECG à la phase aiguë. Aspect évocateur de nécrose myocardique transmurale en latéral haut (D1 et aVL) et en antéroseptal (V1 et V2).

La Lettre du Cardiologue - n° 391 - janvier 2006
29
CAS CLINIQUE
Le diagnostic retenu est un
syndrome du tako-tsubo
survenu
dans le contexte d’un double stress, émotionnel (dispute) et phy-
sique (crise comitiale, elle-même consécutive au premier stress).
La patiente quitte le service sous bêtabloquant et IEC, également
motivés par une hypertension artérielle ancienne.
COMMENTAIRES
Décrit pour la première fois en 1990 (1),le
syndrome du tako-
tsubo, ou ballonnisation apicale transitoire du ventricule
gauche
,n’est pas une pathologie anecdotique : il concernerait 1 %
des patients admis au Japon pour suspicion d’infarctus du myo-
carde, et Bybee et al. (2) estiment que cette cardiopathie était res-
ponsable de 2,2 % des syndromes coronaires aigus avec sus-déca-
lage de ST adressés en 2002 et 2003 à la Mayo Clinic de Rochester.
La majorité des patients concernés sont des
femmes
(de 82 % à
100 % selon les séries), dont l’âge moyen se situe entre 62 et
75 ans. Le symptôme révélateur le plus habituel est une
douleur
thoracique
,souvent décrite comme une constriction rétroster-
nale. Il peut aussi s’agir de dyspnée, plus rarement de lipothymie,
voire de syncope.
Ces symptômes surviennent dans le
contexte habituel d’un
stress aigu,
émotionnel ou physique (3). À l’instar de notre
patiente, Tsuchihashi et al. (4) signalent trois cas de syndrome
du tako-tsubo après une crise d’épilepsie.
La
présentation clinique initiale
peut être marquée par des
complications graves : insuffisance cardiaque, œdème aigu pul-
monaire ou choc cardiogénique pouvant requérir une contre-pul-
sion par ballon intra-aortique (une défaillance cardiaque est obser-
vée pour 3 % à 46 % des patients selon les séries analysées par
Bybee [5]), plus exceptionnellement arythmies auriculaires ou
ventriculaires, troubles conductifs pouvant expliquer une syn-
cope initiale, accident embolique systémique en présence d’un
thrombus intraventriculaire gauche, rupture ventriculaire gauche.
Ces complications sévères mettent en jeu le pronostic vital à la
phase aiguë de la pathologie, avec une mortalité hospitalière de
1% pour la série de 88 patients de Tsuchihashi (4).
Figures 2 a et b.Ventriculographie gauche en OAD (systole [a] et diastole [b]).
En systole, déformation caractéristique du ventricule gauche avec ballonni-
sation des segments moyens et apicaux et hyperkinésie des segments basaux.
a
b
Figure 3. Échocardiographie transthoracique. Coupe apicale 4 cavités.
Ballonnisation des deux tiers apicaux du ventricule gauche avec FEVG
abaissée (35 %).
Figure 4. Échocardiographie transthoracique. Coupe apicale 4 cavités.
Cinq jours après le premier examen, normalisation de la cinétique et de la
fonction ventriculaire gauche (FEVG = 55 %).

La Lettre du Cardiologue - n° 391 - janvier 2006
30
Différentes anomalies de l’ECG
ont été rapportées : le plus
souvent, l’ECG initial présente un sus-décalage de ST dans les
dérivations précordiales, fréquemment associé à des ondes T
négatives ; parfois, seule l’inversion diffuse et ample des ondes
T est observée. Des ondes Q dans les dérivations V1 à V3, un
microvoltage des dérivations standard et un allongement de l’es-
pace QT sont également signalés (3).Toutes ces modifications de
l’ECG sont évocatrices d’une pathologie coronaire, d’autant
qu’elles apparaissent dans le contexte d’une douleur thoracique
rétrosternale. Par comparaison avec les infarctus du myocarde,
l’inversion des ondes T et l’allongement de l’espace QT, d’au-
tant plus important que les ondes T sont profondes, sont plus mar-
qués pour le tako-tsubo (6).
Au stade aigu de la pathologie,
l’échocardiographie trans-
thoracique
peut aider au diagnostic en objectivant la déforma-
tion caractéristique du ventricule gauche : importants troubles de
la cinétique avec ballonnisation des deux tiers apicaux du ven-
tricule respectant sa portion basale hyperkinétique. Ces anoma-
lies de cinétique segmentaire ne correspondent pas à des terri-
toires vasculaires coronaires et leur étendue est disproportionnée
par rapport à la faible ascension enzymatique (seuls 7 patients
sur 88 de la série de Tsuchihashi [4]ont un pic de créatines phos-
phokinases [CPK] > 1 000 UI/l). Face à une douleur thoracique
associée à un sus-décalage du segment ST, ces constatations sont
donc atypiques pour retenir le diagnostic d’infarctus du myo-
carde. En outre, l’échocardiographie authentifie certaines com-
plications : obstruction intraventriculaire gauche, thrombus api-
cal... Enfin, elle sert de référence non invasive pour le suivi
ultérieur. En fonction de leur disponibilité rapide, les explora-
tions scintigraphiques et l’IRM, qui confirme la présence d’un
myocarde viable, peuvent aussi participer au diagnostic et au
suivi du syndrome du tako-tsubo.
Cependant, le plus souvent, la présentation initiale explique
le recours à une coronarographie d’emblée face à la suspi-
cion d’infarctus du myocarde
. Cet examen constate
l’absence
de lésion coronaire significative
; de rares cas de spasmes mul-
tifocaux ont été décrits (3).
La ventriculographie gauche met
en évidence l’aspect caractéristique de ballonnisation api-
cale ventriculaire gauche
avec une hypokinésie sévère ou une
akinésie des segments moyens et apicaux du ventricule gauche,
le respect des segments basaux hyperkinétiques, une fraction
d’éjection réduite et, parfois, une obstruction intraventriculaire
gauche (12 patients sur 72, soit 18 %, avec gradient > 30 mmHg
pour Tsuchihashi [4]).
La prise en charge initiale justifie
une surveillance en unité de
soins intensifs
sous scope et les traitements administrés visent
à gérer les complications de la phase aiguë. Une anticoagulation
efficace est logique compte tenu de l’importance des troubles
cinétiques ventriculaires gauches et de la description de throm-
bus in situ et d’évènements thromboemboliques.
Passées l’instabilité initiale et les éventuelles complications sévères,
le suivi authentifie à brève échéance (de quelques jours à
quelques semaines) la normalisation de la cinétique et de la
fonction systolique ventriculaire gauche
en imagerie (contrôles
de ventriculographie gauche ou d’échocardiographie, examens
scintigraphiques, ou IRM), la fraction d’éjection ventriculaire
gauche passant de 41 % à 64 % dans la série de Tsuchihashi (4).
Par rapport au stade initial de la pathologie,Abe et al. (7) objec-
tivent la disparition des anomalies échocardiographiques après un
délai de 18 jours en moyenne. Des récidives sont mentionnées
dans 0 % à 8 % des cas (5),2,7 % pour Tsuchihashi (4).
Parmi les hypothèses physiopathologiques avancées pour tenter
d’expliquer le syndrome du tako-tsubo, l’implication des artères
coronaires, le rôle d’une obstruction intraventriculaire gauche,
une myocardite sont en définitive peu probables. En fait, les publi-
cations les plus récentes convergent vers
la relation entre syn-
drome du tako-tsubo et cardiopathies catécholaminergiques
.
La publication de Sharkey et al. (3) regroupe 22 patientes origi-
naires d’Amérique du Nord, atteintes du syndrome du tako-
tsubo : la présentation de ces patientes est très proche de celle
des sidérations myocardiques non ischémiques rapportées lors de
pathologies non cardiaques, des phéochromocytomes, des hémor-
ragies subarachnoïdiennes. Wittstein et al. (8) ont comparé les
taux de catécholamines plasmatiques pour 13 patients atteints du
syndrome du tako-tsubo et pour 7 patientes hospitalisées à la suite
d’un infarctus du myocarde en classe Killip III : lors des deux
premiers jours d’évolution, les patients ayant un syndrome du
tako-tsubo ont des taux de catécholamines plasmatiques deux à
trois fois supérieurs à ceux des témoins ayant un infarctus du
myocarde, et 7 à 34 fois plus élevés que les valeurs normales.
Ueyama et al. (9, 10) ont publié deux travaux réalisés sur des rats
femelles : le développement du syndrome du tako-tsubo a pu être
prévenu par blocage préalable des récepteurs cardiaques α- et β-
adrénergiques, et il est démontré que l’activation de ces récep-
teurs constituait le trigger initial des modifications moléculaires
induites au niveau du coeur par le stress. Une augmentation bru-
tale (et probablement transitoire) des catécholamines circulantes
expliquerait le syndrome du tako-tsubo par le biais d’anomalies
de la vasomotricité coronaire ou d’une toxicité directe sur les
myocytes. La localisation des troubles de la cinétique segmen-
taire respectant la base du ventricule gauche peut correspondre
à une réponse exacerbée de sa portion apicale à la stimulation
sympathique (11), expliquée en partie par une plus forte densité
de récepteurs adrénergiques et/ou une réponse accrue à la sti-
mulation adrénergique. Des différences régionales de vasculari-
sation myocardique, la structure même de la pointe ventriculaire
gauche, plus sujette à perdre son élasticité, ont été également citées
pour tenter de comprendre la déformation caractéristique du ven-
tricule gauche. Enfin, il reste à expliquer la prédominance du syn-
drome du tako-tsubo chez des femmes ménopausées : une sup-
plémentation en estradiol atténue la réponse pathologique du
ventricule gauche au stress chez des rats femelles ovariectomi-
sées (12). Pourraient intervenir des altérations de la fonction endo-
théliale après la ménopause, liées à la diminution de l’imprégna-
tion estrogénique, et des troubles de la microcirculation en réponse
aux stimuli catécholaminergiques.
CONCLUSION
L’évolution récente des connaissances permet de mieux définir
le syndrome du tako-tsubo et de proposer des
critères diagnos-
tiques
(5, 13) (tableaux I et II). Avant toute exploration hémo-
dynamique, sont particulièrement évocateurs le contexte de stress,
CAS CLINIQUE

La Lettre du Cardiologue - n° 391 - janvier 2006
31
CAS CLINIQUE
la discordance entre les anomalies ECG et échographiques éten-
dues et la faible élévation enzymatique. Il est cependant difficile
d’éliminer à ce stade le diagnostic d’infarctus du myocarde, et
seule la coronarographie authentifiera l’absence de lésion coro-
naire significative. L’hypothèse actuellement retenue est une
car-
diopathie catécholaminergique se manifestant par une sidé-
ration myocardique réversible dont le pronostic est
favorable une fois passées la phase aiguë et ses complica-
tions potentiellement sévères
.
En dehors de la prise en charge classique des complications ini-
tiales, les mécanismes physiopathologiques impliqués pourraient
conduire à des traitements plus spécifiques pour gérer la phase
aiguë et s’opposer aux récidives. Sur des études animales, le blo-
cage des récepteurs adrénergiques et la supplémentation estro-
génique sont en effet susceptibles de limiter cette réponse patho-
logique au stress. ■
Bibliographie
1. Satoh H, Tateishi H, Uchida T et al. Takotsubo-type cardiomyopathy due to
multivessel spasm. In: Kodama K, Haze K, Hon M, eds. Clinical aspect of myo-
cardial injury: from ischemia to heart failure (in Japanese). Tokyo:
Kagakuhyouronsya Co, 1990;56-64.
2. Bybee KA, Prasad A, Barsness GW et al. Clinical characteristics and throm-
bolysis in myocardial infarction frame counts in women with transient left ven-
tricular apical ballooning syndrome. Am J Cardiol 2004;94:343-6.
3. Sharkey SW, Lesser JR, Zenovich AG et al. Acute and reversible cardiomyo-
pathy provoked by stress in women from the United States. Circulation
2005;111:472-9.
4. Tsuchihashi K, Ueshima K, Uchida T et al., for the Angina Pectoris-
Myocardial Infarction Investigations in Japan. Transient left ventricular apical
ballooning without coronary artery stenosis: a novel heart syndrome mimicking
acute myocardial infarction. J Am Coll Cardiol 2001;38:11-8.
5. Bybee KA, Kara T, Prasad A et al. Systematic review: transient left ventricu-
lar apical ballooning: a syndrome that mimicks ST-segment elevation myocardial
infarction. Ann Intern Med 2004;141:858-65.
6. Kurisu S, Inoue I, Kawagoe T et al. Time course of electrocardiographic
changes in patients with tako-tsubo syndrome: comparison with acute myocardial
infarction with minimal enzymatic release. Jpn Circ J 2004;68:77-81.
7. Abe Y, Kondo M, Matsuoka R, Araki M, Dohyama K, Tanio H. Assessment of
clinical features in transient left ventricular apical ballooning. J Am Coll Cardiol
2003;41:737-42.
8. Wittstein IS, Thiemann DR, Lima JAC et al. Neurohumoral features of myo-
cardial stunning due to sudden emotional stress. N Engl J Med 2005;352:539-48.
9. Ueyama T, Kasamatsu K, Hano T,Yamamoto K, Tsuruo Y, Nishio I. Emotional
stress induces transient left ventricular hypocontraction in the rat via activation
of cardiac adrenoceptors: a possible animal model of “tako-tsubo” cardiomyo-
pathy. Circ J 2002;66:712-3.
10. Ueyama T, Senba E, Kasamatsu K et al. Molecular mechanism of emotional
stress-induced and catecholamine-induced heart attack. J Cardiovasc Pharmacol
2003;41(Suppl.1):S115-S118.
11. Mori H, Ishikawa S, Kojima S et al. Increased responsiveness of left ventri-
cular apical myocardium to adrenergic stimuli. Cardiovasc Res 1993;27:192-8.
12. Ueyama T, Hano T, Kasamatsu K, Yamamoto K, Tsuruo Y, Nishio I. Estrogen
attenuates the emotional stress-induced cardiac responses in the animal model of
Tako-tsubo (ampulla) cardiomyopathy. J Cardiovasc Pharmacol 2003;42 (Suppl.1):
S117-S119.
13. Abe Y, Kondo M. Apical ballooning of the left ventricle: a distinct entity?
Heart 2003;89:974-6.
Critères majeurs
1. Ballonnisation réversible de la portion apicale du ventricule gauche
avec segments basaux hypercontractiles
2. Anomalies électrocardiographiques de ST-T mimant un infarctus du
myocarde aigu
Critères mineurs
1. Stress physique ou émotionnel pour facteur déclenchant
2. Élévation modérée des enzymes cardiaques
3. Douleur thoracique
Critères d’exclusion
Sidération myocardique ischémique
Hémorragie subarachnoïdienne
Phéochromocytome
Myocardite aiguë
Cardiopathie rythmique
Tableau I. Critères diagnostiques du syndrome du tako-tsubo (13).
1. Akinésie ou dyskinésie transitoire des segments apicaux et moyens du
ventricule gauche dont l’étendue ne correspond pas à un territoire coro-
naire
2. Absence de coronaropathie sténosante ou d’évidence angiographique
de rupture de plaque aiguë
3. Apparition d’anomalies électrocardiographiques (soit sus-décalage du
segment ST, soit inversion des ondes T)
4. Absence :
✓de traumatisme crânien récent
✓d’hémorragie intracérébrale
✓de phéochromocytome
✓de coronaropathie sténosante
✓de myocardite
✓de cardiomyopathie hypertrophique
Tableau II. Critères nécessaires pour le diagnostic du syndrome du
tako-tsubo proposés par la Mayo Clinic (5).
1
/
4
100%