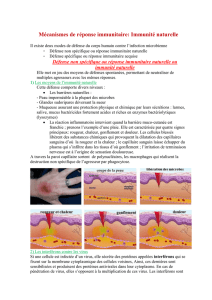
Phases de la réponse immune anti-infectieuse - Sante.univ

Spécifique
Inductible
Mémoire
T spécifiques
Non spécifique/ spécifique
Inductible
Pas de mémoire
Pas de T spécifiques
Non spécifique
Innée
Pas de mémoire
Pas de T spécifiques
T cytotoxiques (CD8)
IFN-!
IFN " et # (type 1)
NK activé par IL-12
NK
Réponse aux
virus
Activation des
macrophages par les
Th1 (IFN-!)
Activation des
macrophages par NK
IL-1, IL-6, TNF-", IL-12
Macrophages
Réponse aux
bactéries
intracellulaires
IgG-FcR
(opsonisation)
complément (voie
classique IgG, IgM)
MBL, CRP
Ac T-indépendents
Complément
Phagocytes
Complément (voies
alterne + lectines)
Réponse aux
pathogènes
extracellulaires
IgA muqueuses
IgE sur mastocytes
Inflammation locale
Inflammation locale
(C5a)
TNF-" local
Peau, epithelia
Fonctions
barrières
Retardée (96-100h)Précoce (4-96h)Immédiate (0-4h)
Phases de la réponse immune anti-infectieuse

Rôle et source des interférons "/#
dans l’immunité anti-virale

Interférons de type 1
IFN de type I : IFN-" = une famille de 14 protéines
IFN-# = une seule protéine
Cellules productrices d’IFN-"/#:
• Produits en petite quantités par de nombreuses en réponse à une infection
virale
• Produits en très grandes quantité par une population de cellules
dendritiques immatures dites plasmacytoïdes après infection virale
Fonctions de IFN-"/#:
! Induit un état de résistance à la réplication virale dans toutes les cellules
exprimant le récepteur à l’IFN (activation RNAse endogène, kinases, MX)
! Augmente l’expression des antigènes de classe I et la présentation de
peptide viraux
! Active les cellules NK, les cellules dendritiques
! Favorise l’activation des lymphocytes B et T

Les cellules dendritiques plasmacytoïdes
ou « Interferon-producing cells »
- Morphologie: plasmacytoïde
- Localisation: organes lymphoïdes et sang
- Fonctions relativement conservées entre espèces
- Malgré leur rareté, les pDC immatures constituent la
source majeure d’IFN de type I dans l’organisme lors d’une
infection virale
- Répertoire d’expression de TLR limité: TLR 7 et 9
- Recrutement rapide dans les ganglions lymphatiques en
cas d’infection
- Transformation en cellule présentatrice d’antigène
professionnelle après maturation induite par pathogènes

Cellules dendritiques plasmacytoïdes: morphologie
Lymphocyte
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
1
/
36
100%