Étude de la dynamique du système racinaire des plantules de

Article scientifique
Étude de la dynamique
du système racinaire des plantules
de certaines espèces arbustives
autochtones de la Tunisie aride
Farah Ben Salem
Azaiez Ouled Belgacem
Mohamed Neffati
Laboratoire d’écologie pastorale,
institut des régions arides,
route Djorf, km 22,
4119 Médenine,
Tunisie
<Nef[email protected]>
Résumé
Le présent travail a porté sur l’étude de la dynamique du système racinaire de trois
arbustes autochtones présentant un grand intérêt économique et écologique en
Tunisie aride (Acacia raddiana Savi., Ceratonia siliqua L. et Juniperus phoenicea
L.), et cultivés dans des rhizotrons dans le but de maîtriser la culture de leurs plants en
pépinière. Les résultats obtenus montrent que le développement du système racinaire
des trois espèces étudiées est rapide, dès les premiers mois suivant leur germination
(au mois de novembre), même si la croissance du système racinaire d’A. raddiana
est affectée par les basses températures hivernales. Un tel comportement, qui, dans
les conditions naturelles, constitue l’une des caractéristiques adaptatives de ces
espèces aux conditions d’aridité climatique, doit être pris en compte en cas de culture
de leurs plants dans des pépinières.
Mots clés : arbuste, croissance racinaire, Tunisie, zone aride.
Abstract
Study of root system dynamics of some local arid Tunisian shrubs
The present study was carried out to clarify the root dynamics of three local shrubs
(Acacia raddiana Savi., Ceratonia siliqua L. and Juniperus phoenicea L.) of the
Tunisian arid zone presenting high economic and ecological interest in southern
Tunisia. Plants were cultivated in rhizotrons. The main results show rapid root
development of the three species from the first months following germination (month
of November), even though the growth of the Acacia raddiana rooting system was
negatively influenced by the low winter temperatures. Such behaviour constitutes, in
natural conditions, one of the adaptive characteristics to hard climatic conditions of
the species studied and should be, therefore, taken into account when raising
seedlings in nurseries.
Key words: arid zone, root growth, shrub, Tunisia.
L
a pression animale et humaine crois-
sante exercée depuis plusieurs décen-
nies sur le couvert végétal de la Tuni-
sie aride, s’est soldée par une régression
considérable de certaines espèces pasto-
rales ainsi qu’une dégradation souvent
irréversible, notamment du milieu physi-
que [1]. Cet effet dégradant de la popula-
tion est amplifié par la sévérité des condi-
tions pédoclimatiques.
Dans les situations où la dégradation des
parcours a atteint le seuil d’irréversibilité et
Tirés à part : M. Neffati
Sécheresse 2008 ; 19 (2) : 123-8
doi: 10.1684/sec.2008.0127
Sécheresse vol. 19, n° 2, avril-mai-juin 2008 123
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

où la reconstitution de l’écosystème par
une simple mise en défens n’est plus possi-
ble, la réaffectation [2] par plantation
d’arbustes fourragers s’impose. Il y a lieu
cependant de mentionner que la plupart
des tentatives de resemis des parcours par
des espèces herbacées introduites [3, 4] et
des arbustes exotiques [5] ont été vouées à
l’échec en raison de la mauvaise adapta-
tion de ces espèces. Zaafouri a démontré
que dans les zones dont la pluviométrie est
comprise entre 150 et 200 mm, la réussite
des plantations est tributaire de leur locali-
sation dans les situations les plus favora-
bles (sol profond, apport d’eau de ruissel-
lement). Or, dans ces conditions, les
agriculteurs considèrent comme prioritai-
res les cultures vivrières, céréalières et
arboricoles. Dans les contextes écologi-
ques les plus défavorables, représentant la
majeure partie des superficies des systè-
mes écologiques, en Tunisie steppique, ce
même auteur fait remarquer que les espè-
ces autochtones sont les plus performan-
tes. En zones arides, seules ces espèces
peuvent en effet durablement conserver le
sol et constituer des réserves fourragères
sur pied pendant les années de disette.
La réussite des plantations est tributaire du
choix d’un matériel végétal adapté à la
nature du milieu édaphique, aux techni-
ques de culture des plants en pépinière qui
sont fortement liées à la connaissance de
l’architecture racinaire, des travaux
d’entretien et de sauvegarde et des techni-
ques de conduite et de gestion des planta-
tions [6].
L’utilisation des espèces autochtones pour
la réhabilitation des zones dégradées de
la Tunisie présaharienne nécessite plu-
sieurs informations précises sur les condi-
tions de leur installation et sur les modali-
tés de leur propagation [5].
C’est dans ce cadre que nous nous som-
mes proposés d’étudier trois espèces
arbustives autochtones — Acacia rad-
diana Savi (AR), Ceratonia siliqua L. (CS)
et Juniperus phoenicea L. (JP) — connues
pour leurs usages multiples en Tunisie méri-
dionale et leur rusticité face aux actions
anthropozoïques. Il s’agit, en effet, d’espè-
ces très prometteuses pour la réhabilitation
des milieux dégradés. Elles sont de ce fait
de plus en plus utilisées dans les program-
mes de reboisement par les services fores-
tiers de la Tunisie centrale et méridionale,
où leur réintroduction révèle un grand inté-
rêt économique et écologique.
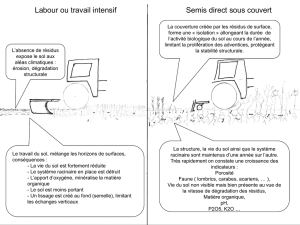
Matériel et méthode
L’étude de la cinétique de croissance du
système racinaire a été réalisée dans des
rhizotrons de différentes dimensions
depuis 125 ans : [7-21]. Cette méthode
nous permet de visualiser certaines carac-
téristiques morphologiques du système
racinaire telles que la vitesse de crois-
sance radiculaire, les ramifications des
racines secondaires et leur positionnement
sur la racine principale [21].
Les pots utilisés sont des rhizotrons, rectan-
gulaires, de 96 cm de hauteur et de
50 × 15 cm de section et ayant un côté
vitré. Ils sont remplis d’un mélange sablo-
limoneux et placés inclinés à 10° par
rapport à la verticale dans des fosses où il
est possible de protéger la face vitrée de la
lumière. Cette face vitrée, qui permet lors
des observations régulières (tous les
3 jours) de visualiser une partie du sys-
tème racinaire et, donc, de suivre son
développement, est protégée contre la
lumière par des plaques de polystyrène de
9 cm d’épaisseur. Les rhizotrons sont pla-
cés en plein champ et exposés directement
aux rayons de soleil [8, 10, 12, 13].
Des graines des espèces cibles en prove-
nance de la banque de semences de l’ins-
titut des régions arides de Médenine ont
été utilisées après différents traitements
considérés comme efficaces à la levée de
leur dormance et/ou inhibitions [4, 22].
Ces graines sont traitées à l’acide sulfuri-
que concentré à 95 % pendant 45 minu-
tes pour J. phoenicea, 1 heure pour
A. raddiana et 2 heures pour C. siliqua.
Les graines bien immergées sont remuées
à l’aide d’une spatule. Elles sont ensuite
retirées, égouttées à l’aide d’un tamis, puis
lavées à l’eau courante pendant 10 à
15 minutes. Le semis a eu lieu le 23
novembre 2003, à proximité de la face
vitrée, dans 6 rhizotrons à raison de
2 rhizotrons par espèce et de 16 graines
par rhizotron réparties en quatre poquets.
Un arrosage a été effectué juste après le
semis. Par la suite, ils ont été effectués de
façon à maintenir le sol dans les rhizotrons
à un niveau proche de la capacité au
champ. Après émergence, seules 4 plantu-
les ont été conservées au niveau de cha-
que bac (8 plants par espèce). Il s’agit des
plantules situées loin des deux côtés et
proches de la face vitrée. Au niveau de
cette face, une feuille plastique transpa-
rente a été fixée. Sur cette feuille ont été
tracés, tous les trois jours, les changements
observés au niveau du développement des
racines. Les racines nouvelles et l’allonge-
ment des racines plus anciennes sont repé-
rés sur ce calque (marqués de feutre per-
manent avec changement de couleur
après chaque observation) [21].
Parallèlement au suivi du système raci-
naire, des mesures ont été effectuées sur la
partie aérienne des trois espèces étudiées.
L’apparition des feuilles et la ramification
de la partie aérienne ont été relevées. Afin
de comparer les différents paramètres et
descripteurs de croissance suivis chez ces
espèces (LCPA : longueur cumulée de la
partie aérienne ; LCPR : longueur cumulée
de la partie racinaire ; NbRS : nombre
des racines secondaires ; LRS : longueur
des racines secondaires ; NbF : nombre
des feuilles), nous avons procédé à des
analyses statistiques telles que l’analysis of
variance (Anova) et le test de Student-
Newman-Keuls.
Suite à la mort, sous l’effet du froid, de la
totalité des plants d’A.raddiana semés au
mois de novembre 2003 (AR1), nous
avons été contraints de reconduire l’essai
en effectuant un second semis au mois
d’avril 2004 (AR2). Les résultats présentés
dans le cadre de ce travail sont ceux
relatifs aux deux dates de semis. La
période d’observation qui a débuté au
semis était de 4 mois pour AR1, 2 mois
pour AR2 et six mois pour CS et JP.
La moyenne des températures mensuelles,
minimales nocturnes et journalières, au
cours de la période d’étude est rapportée
au tableau 1.
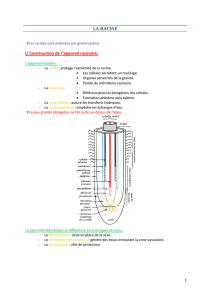
Résultats
Longueur cumulée des racines
et de la partie aérienne
Rappelons que la longueur cumulée des
racines et de la partie aérienne est obte-
Tableau I.Valeurs mensuelles moyennes des températures (°C) minimales nocturnes et journalières enregistrées pendant la période d’observation
(année biologique 2003–2004).
Automne Hiver Printemps
Septembre Octobre Novembre Décembre Janvier Février Mars Avril Mai
Température minimale nocturne 23,7 19,0 10,5 8,5 4,8 7,5 12,1 12,7 13,2
Température moyenne journalière 31,9 25,2 19,2 12,9 10,4 16,1 16,6 20,1 20,9
124 Sécheresse vol. 19, n° 2, avril-mai-juin 2008
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

nue, pour chaque date, par addition de la
valeur enregistrée lors de la mesure aux
valeurs enregistrées lors des mesures pré-
cédentes.
L’examen de la figure 1, illustrant la lon-
gueur cumulée de la partie visualisée des
racines et de la partie aérienne des trois
espèces étudiées, durant la période com-
prise entre le mois de novembre (date de
semis) et la fin du mois de mai, montre
que :
–A. raddiana se caractérise par une
croissance radiculaire rapide pendant
toute la période automnale (1,37 cm/j) et
faible durant la période hivernale
(0,15 cm/j). De même, la croissance de la
partie aérienne est faible, voire nulle pen-
dant la période hivernale (brûlures des
feuilles, puis mort de la totalité des plants).
À cet effet, nous avons été contraints de
reconduire l’essai en semant au mois
d’avril de nouveaux plants d’A. raddiana
(AR2). Ces plants ont présenté une crois-
sance radiculaire régulière et rapide pen-
dant la première quinzaine d’avril
(1,44 cm/j) et relativement faible mais
toujours régulière durant le reste de la
période d’observation (1 cm/j). La partie
aérienne montre également un développe-
ment très régulier et rapide à partir du
6
e
jour après le semis pour atteindre
12 cm au bout de 2 mois ;
–C. siliqua présente une croissance régu-
lière des deux parties, aérienne et souter-
raine, avec une légère supériorité de la
partie aérienne au cours de la période
hivernale. Le ralentissement de la crois-
sance du pivot est compensé par le déve-
loppement des ramifications secondaires
et tertiaires. Ces ramifications atteignent la
même longueur cumulée que celle du pivot
vers la fin du mois de février (105
e
jour
après semis), et cela malgré un développe-
ment tardif par rapport à la racine princi-
pale ;
–J. phoenicea est caractérisée par une
croissance régulière (0,66 cm/j) de son
système racinaire dès la germination (à
partir du 24
e
jour après le semis). La partie
aérienne émerge dès que la radicule
atteint 8,4 cm de longueur et continue son
développement lentement en comparaison
avec la partie souterraine.
Il est à signaler que les trois espèces pré-
sentent une différence hautement significa-
tive (p< 0,001) au niveau de la crois-
sance de leurs parties racinaires et
aériennes.
Les rapports d’allométrie entre la partie
racinaire et la partie aérienne des espèces
étudiées varient de 5,9 chez C. siliqua à
6,1 pour J. phoenicea et de 7 à 8,9 pour
A. raddiana semée en avril et en novem-
bre respectivement (figure 2).
Acacia raddiana (AR1)
80
60
40
20
0
20
Longueur cumulée (cm)
Longueur cumulée (cm)
Longueur cumulée (cm)
Longueur cumulée (cm)
Acacia raddiana (AR2)
80
60
40
20
0
20
Ceratonia siliqua (CS)
80
60
40
20
0
20
Juniperus phoenicea (JP)
80
60
40
20
0
20
Nombre de jours depuis le semis en rhizotron
Partie aérienne Partie racinaire
27 54 81
3
66 123 17712
66 123 177
12
27 543
Figure 1
.
Longueur cumulée des racines et des parties aériennes des jeunes plants des espèces
étudiées pendant la période d’observation en fonction du nombre de jours.
Sécheresse vol. 19, n° 2, avril-mai-juin 2008 125
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Ramification des racines
Il y a lieu de signaler que les trois espèces
étudiées présentent un pivot plus ou moins
long et des ramifications secondaires.
Le système racinaire d’A. raddiana s’est
très peu ramifié, du moins, au début de
l’essai pour la première date de semis.
À la deuxième date de semis (avril),
A. raddiana n’a développé ses ramifica-
tions qu’à 14 cm de profondeur. La distri-
bution des racines secondaires le long de
la racine principale se produit d’une façon
homogène à partir de cette profondeur
pour augmenter de vitesse dès le
deuxième mois d’observation (mai 2004).
C. siliqua montre des ramifications qui
prennent naissance à partir des couches
superficielles du sol (à partir de 12 cm du
collet) et augmentent aussi bien en nombre
qu’en longueur avec la profondeur [23].
Chez J. phoenicea, en revanche, les rami-
fications du système racinaire sont moins
importantes et ne se développent qu’à
partir de 8 cm de profondeur. De telles
caractéristiques permettent à ces espèces
de survivre même lorsque les précipita-
tions sont espacées dans le temps (cas de
C. siliqua) et de valoriser les petites pluies
dès le stade jeune (cas de J. phoenicea).
Cependant, les espèces étudiées présen-
tent une différence hautement significative
(p< 0,003) au niveau du nombre et de la
longueur des racines secondaires.
D’ailleurs, l’examen de la figure 3, qui
illustre le nombre de racines secondaires
des espèces étudiées développées au
cours de la période d’observation, montre
que pour C. siliqua, AR2 et J. phoenicea,
l’émission de ces racines est importante au
début du cycle végétatif, mais diminue
considérablement pendant la saison sèche
(avril, mai). Cela est fortement influencé
par l’interaction entre l’environnement et
le facteur génétique [24].
Il y a lieu de rappeler que le nombre de
racines secondaires a été déterminé par le
comptage de l’ensemble des racines
issues de la racine principale et de ses
réitérations.
Au cours de notre étude, nous avons
observé que le système racinaire des trois
espèces a conservé sa structure primaire
au sens de Canon [25] ; racine principale
et ramifications secondaires. Selon la clas-
sification du système racinaire adoptée
par Bendali [26], ce mode de ramification
est dit « distale ».
Discussion
La différence mise en évidence au niveau
de la croissance des systèmes racinaires
des espèces étudiées peut être expliquée
par la différence de réaction de ces trois
espèces au facteur thermique (tableau I).
Plus tolérante au froid [23], C. siliqua a
poursuivi régulièrement sa croissance raci-
naire (0,96 cm/j), même au cours de la
période hivernale. La croissance du sys-
tème racinaire d’AR1 est restée très lente
(0,15 cm/j) et peu ramifiée durant toute la
période hivernale. Cela pourrait être éga-
lement imputé aux basses températures
Acacia raddiana (AR1)
0
2
4
6
8
10
12
0
P. racinaire/P. aérienne
P. racinaire/P. aérienne
P. racinaire/P. aérienne
P. racinaire/P. aérienne
Acacia raddiana (AR2)
0
1
2
3
4
5
6
7
8
Ceratonia siliqua (CS)
0
1
2
3
4
5
6
7
Juniperus phoenicea (JP)
0
2
4
6
8
Nombre de jours depuis le semis en rhizotron
9 1827364554637284
09
18 27 36 45 54 66
12 4830 66 84 105 123 177 195141 159 213
12 4830 66 84 105 123 177 195141 159 213
Figure 2
.
Rapport d’allométrie entre les parties aériennes et racinaires chez les trois espèces
étudiées au cours de la période d’observation.
AR1 : A. raddiana semée au mois de novembre ; AR2 : A. raddiana semée au mois d’avril.
126 Sécheresse vol. 19, n° 2, avril-mai-juin 2008
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

ayant caractérisé cette période. Les plants
d’AR2 présentent une vitesse de crois-
sance importante après augmentation des
températures au début du printemps
(1,44 cm/j), et moyenne à faible pendant
le reste de la période d’observation. Il est
à signaler que ce ralentissement de la
vitesse de croissance a pour contrepartie
une croissance des racines secondaires de
l’ordre de 0,6 cm par jour. Chez AR1, le
développement des racines secondaires à
partir de 5 cm de profondeur lui permet de
valoriser les petites pluies. Alors que,
l’absence de racines secondaires au
niveau des couches superficielles de subs-
trat d’AR2 n’est qu’un argument d’appui
pour expliquer la stratégie d’échappement
à la sécheresse adoptée par A. raddiana
[27]. Dans les conditions naturelles, de
telles caractéristiques permettent à ces
espèces de survivre même lorsque les pré-
cipitations sont espacées dans le temps
(cas de C. siliqua) et de valoriser les peti-
tes pluies dès leurs jeunes stades (cas
d’A. raddiana et de J. phoenicea). La
croissance régulière du système racinaire
de CS et très rapide de JP pendant toute la
période hivernale prouve bien que ces
deux espèces montagneuses tolèrent le
froid.
Il semble par conséquent qu’une espèce à
grande vitesse d’élongation du système
racinaire (cas d’espèces étudiées) peut
rapidement atteindre une couche plus pro-
fonde et plus humide, ce qui améliore ses
chances de survie [27-30]. La ramification
du système racinaire des espèces étudiées
semble être efficace pour l’extraction de
l’eau sur des profondeurs importantes,
mais aussi latéralement et en superficie à
l’aide de ces réitérations distales. Il est
cependant intéressant de signaler que ces
arbustes autochtones pouvant survivre
dans des milieux à pluviométrie moyenne
annuelle très faible (50 mm/an) [25] doi-
vent être sûrement dotés d’un système raci-
naire à capacité d’extraction d’eau très
élevée.
Conclusion
Réalisée dans des rhizotrons, cette étude a
pour objectif de suivre la dynamique du
système racinaire de trois arbustes autoch-
tones (A. raddiana Savi., C. siliqua L. et
J. phoenicea L.) présentant un grand inté-
rêt économique et écologique en Tunisie
aride. Les résultats de cette étude montrent
que le semis d’A. raddiana au mois d’avril
est préconisé puisqu’il garantit un bon
développement des plants en pépinière au
cours d’une période plus courte, ce qui
influe par la suite sur la réussite des plants
après transplantation. C. siliqua L. et
J. phoenicea L. semblent plus tolérantes au
froid et un semis d’automne est par consé-
quent préconisé. La diminution d’émission
de racines secondaires engendre une
diminution d’apparition de feuilles chez
les trois espèces étudiées, ce qui se traduit
probablement par un ralentissement de la
perte d’eau par évapotranspiration qui est
l’une des stratégies adaptatives aux condi-
tions climatiques des régions arides. ■
Références
1. Aidoud A, Le Floc’h E, Le Houérou HN. Les
steppes arides du Nord de l’Afrique. Sécheresse
2006 ; 17 : 19-30.
2. Aronson J, Floret C, Le Floc’h E, Ovalle C,
Pontanier R. Restoration and rehabilitation of
degraded ecosystems in arid and semi arid
regions. I. A view from the South. Restor Ecol
1993 ; 1 : 8-17.
3. Chaieb M. Influence des réserves hydriques du
sol sur le comportement comparé de quelques
espèces végétales de la zone aride tunisienne.
Thèse de doctorat, université des sciences et tech-
niques du Languedoc (USTL), Montpellier 1989.
4. Neffati M. Caractérisation morphobiologique
de certaines espèces végétales nord-africaines.
Implications pour l’amélioration pastorale. Thèse
de doctorat, université de Gent, Belgique, 1994.
5. Zaafouri MS. Contraintes du milieu et réponse
de quelques espèces arbustives exotiques intro-
duites en Tunisie présaharienne. Thèse de docto-
rat, université de droit, d’économie et de scien-
ces. Aix–Marseille-III, 1993.
6. Zaafouri MS, Akrimi N, Floret C, Le Floc’h E,
Pontanier R. Les plantations sylvopastorales en
Tunisie présaharienne. Sécheresse 1994 ; 5 :
265-75.
7. Bates GH. A device for the observation of root
growth in the soil. Nat (London) 1937 ; 139 :
966-7.
8. Berntson GM, Woodward FI. The root system
architecture and development of Senecio vulgaris
in elevated CO
2
and drought. Funct Ecol 1992 ;
6 : 324-33.
9. Box Jr. JE. Modern methods for root investiga-
tions. In : Waisel Y, Eshel A, Kafkafi U, eds. Plant
Roots–The Hidden Half. New York : Marcel Dec-
ker, 1996.
10. Dieffenbach A, Gottlein A, Matzner E. In situ
soil solution chemistry in an acid forest soil as
influenced by growing roots of Norway spruce
(Picea abies L. [Karst.]). Plant Soil 1997 ; 192 :
57-61.
11. Misra RK. Root and shoot elongation of
rhizotron-grown seedlings of Eucalyptus nitens
and Eucalyptus globules in relation to tempera-
ture. Plant Soil 1999 ; 206 : 37-46.
12. Zhou ZC, Shangguan ZP. Advances on the
responses of root dynamics to increased atmos-
pheric CO
2
and global climate change. Agr Sci
in China 2006 ; 5 : 161-8.
13. Bakker MR, Kerisit R, Verbist K, Nys C.
Effects of liming on rhizosphere chemistry and
growth of fine roots and shoots of sessile oak
(Quercus petraea). Plant Soil 1999 ; 217 : 243-
55.
14. Dieffenbach A, Matzner E. In-situ soil solu-
tion chemistry in the rhizosphere of mature
Norway spruce (Picea abies L. [Karst.]). Plant Soil
2000 ; 222 : 149-61.
15. Lorenzen B, Brix H, Mendelssohn IA,
Mckee KL, Miao SL. Growth, biomass allocation
and nutrient use efficiency in Cladium jamai-
cense and Typha domingensis as affected by
phosphorus and oxygen availability. Aquat Bot
2001 ; 70 : 117-33.
16. Schlesinger WH, Lichter J. Limited carbon
storage in soil and litter of experimental of forest
plots under increased atmospheric CO
2
.Nature
2001 ; 411 : 466-9.
17. Pregitzer KS, DeForest JL, Burton AJ. Fine
root architecture of nine North American trees.
Ecolog Manag 2002 ; 72 : 293-309.
18. He JS, Bazzaz FA. Density dependent res-
ponses of reproductive allocation to elevated
atmospheric CO
2
in Phytolacca americana L.
New Phytol 2003 ; 157 : 229-39.
19. Luo YQ. Uncertainties in interpretation of iso-
tope signals for estimation of fine root longevity :
theoretical considerations. Global Chan Biol
2003 ; 9 : 1118-29.
0
5
10
15
20
25
30
Novembre
Période d'étude (mois)
Nb. de racines secondaires
AR1
CS
JP
AR2
Décembre Janvier Février Mars Avril Mai
Figure 3. Nombre de racines secondaires des espèces cibles au cours de la période d’étude.
AR1 : A. raddiana semée au mois de novembre ; AR2 : A. raddiana semée au mois d’avril ; CS : C. siliqua ;
JP : J. phoenicea.
Sécheresse vol. 19, n° 2, avril-mai-juin 2008 127
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.
 6
6
1
/
6
100%