revue générale Rôle des N-glycanes dans les fonctions des

revue générale
Rôle des N-glycanes dans les fonctions
des glycoprotéines d’enveloppe
du virus de l’hépatite C
Role of N-linked glycans in the functions
of hepatitis C virus envelope glycoproteins
A. Goffard
M. Lazrek
L. Bocket
A. Dewilde
D. Hober
Service de virologie,
UPRES-EA3610, CHRU Lille,
Faculté de médecine,
Université Lille 2, Lille
<a-gof[email protected]>
Article reçu le 13 septembre 2006,
accepté le 22 février 2007
Résumé.Le virus de l’hépatite C (VHC) est un virus enveloppé dont l’enve-
loppe virale est constituée d’une bicouche lipidique dans laquelle sont ancrées
deux glycoprotéines d’enveloppe, E1 et E2. Ces glycoprotéines subissent de
nombreuses modifications co- et post-traductionnelles à l’issue desquelles elles
acquièrent leur conformation définitive. La N-glycosylation se déroule dans le
réticulum endoplasmique et passe par la reconnaissance d’un motif spécifique
d’acides aminés de type Asparagine-X-Sérine/Thréonine-Y. Les glycoprotéines
E1 et E2 du VHC sont des protéines transmembranaires de type I qui s’assem-
blent pour former des hétérodimères non-covalents. Au cours de leur synthèse,
les glycoprotéines E1 et E2 traversent le réticulum endoplasmique dans lequel
elles subissent différentes modifications dont la N-glycosylation. La glycopro-
téine E1 porte 4 ou 5 sites potentiels de N-glycosylation et la glycoprotéine E2
en porte 10 ou 11 en fonction des génotypes viraux. La glycoprotéine E1 de
génotype 1a est glycosylée sur 4 de ces 5 sites potentiels et la glycoprotéine E2
sur les 11 sites potentiels. Les N-glycanes portés par E1 et E2 jouent un rôle
majeur dans la mise en conformation des glycoprotéines et dans la formation
des hétérodimères E1E2. Certains N-glycanes portés par E2 sont par ailleurs
impliqués dans les interactions avec CD81, récepteur potentiel du VHC et
d’autres portés par E1 et E2 jouent un rôle dans l’entrée virale.
Mots clés :virus de l’hépatite C, glycoprotéines d’enveloppe, N-glycanes,
entrée virale
Abstract.Hepatitis C virus (HCV) is an enveloped virus and encodes two
envelope glycoproteins, E1 and E2. E1 and E2 are transmembrane type I
proteins with a N-terminal ectodomain and C-terminal anchor. During their
synthesis, E1 and E2 ectodomains are targeted in the endoplasmic reticulum
lumen where they are modified by N-linked glycosylation. After their synthe-
sis, E1 and E2 assemble as a non-covalent heterodimer. The N-linked glycosy-
lation is based on the recognition of specific asparagine residue in the context
of the consensus sequence Asn-X-Ser/Thr. E1 contains potentially 4 or 5
N-linked glycosylation sites and E2 up to 11. Recent data indicated that some
glycans of glycoproteins E1 and E2 play a major role in protein folding and
heterodimer formation. Some N-linked glycans of E2 were involved in interac-
tions with CD81, a putative cellular receptor for HCV. It appeared that
N-linked glycans of E1 and E2 played an important role of in the viral entry.
Key words:hepatitis C virus, envelope glycoproteins, N-linked glycans, viral
entry
Tirés à part : A. Goffard
abc
Ann Biol Clin 2007 ; 65 (3) : 237-46
doi: 10.1684/abc.2007.0125
Ann Biol Clin, vol. 65, n° 3, mai-juin 2007 237
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Le virus de l’hépatite C (VHC) a été découvert en 1989.
C’était le premier agent infectieux découvert à l’aide
d’outils de biologie moléculaire, sans isolement préalable
de particules virales. Depuis, de nombreuses recherches
ont permis une meilleure connaissance du virus, de sa
physiopathologie et des pathologies qu’il entraîne. Cepen-
dant, la prise en charge de patients infectés chroniquement
par le VHC, malgré une certaine efficacité, se heurte à un
certain nombre de difficultés : lourdeur des traitements,
apparition de résistances aux antiviraux, patients non-
répondeurs... Dans cette synthèse, nous verrons que les
travaux portant sur la caractérisation des glycoprotéines
de l’enveloppe virale pourraient ouvrir de nouvelles pers-
pectives thérapeutiques.
Le VHC appartient à la famille des Flaviviridae, au genre
Hepacivirus. Il existe 6 génotypes différents (numérotés
de1à6)etdenombreux sous-types (1a, 1b, 1c, 2a, 2b,
etc.). Le VHC est un virus enveloppé avec un génome de
type ARN simple brin de polarité positive. L’ARN géno-
mique présente un seul cadre de lecture ouvert qui est
transcrit en une polyprotéine organisée en deux régions :
la région N-terminale qui code les protéines structurales
du virus (protéines F, C, E1, E2) et la région C-terminale
qui code les protéines non-structurales (protéines NS2,
NS3, NS4A, NS4B, NS5A et NS5B) (figure 1). Un petit
peptide, p7, codé dans une région située entre E2 et NS2,
n’a pas encore trouvé une place définitive parmi les protéi-
nes structurales ou non-structurales. La polyprotéine est
clivée par des protéases cellulaires (de type signal pepti-
dase et signal peptide peptidase) et virales (NS2-3 et NS3-
4A) pour donner 10 protéines matures. L’enveloppe virale
est constituée d’une bicouche lipidique dans laquelle sont
ancrées les glycoprotéines d’enveloppe E1 et E2. Elles
sont produites par clivage protéolytique du précurseur du
VHC par une peptidase signal d’origine cellulaire (revue
dans [1]). Les clivages co-traductionnels aux sites C/E1,
E1/E2 et NS2/NS3 produisent E1 et un précurseur de E2,
E2p7NS2. Après clivage, ce précurseur produit E2, p7,
E2p7 et NS2 [2].
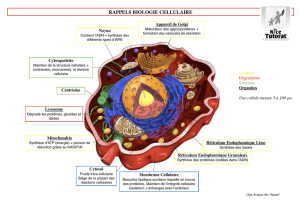
Principes de la N-glycosylation
Au cours de leur passage dans le réticulum endoplasmique
et l’appareil de Golgi, les protéines immatures subissent
différentes modifications co- et post-traductionnelles telles
que la formation de ponts disulfures, la N- et la
O-glycosylation, le clivage de peptide signal, les interac-
tions avec les protéines chaperons, etc. À l’issue de ces
transformations, les protéines seront sous leur forme mature
et correctement repliées. La N-glycosylation passe par la
reconnaissance d’un motif spécifique de type Asparagine-
X-Sérine/Thréonine-Y où X et Y désignent des acides ami-
nés dont la nature a son importance comme nous le verrons
plus loin. Les N-glycanes ont une structure commune for-
mée d’un noyau pentasaccharidique, le trimannosyl-di-N-
acétylchitobiose (figure 2
). La N-glycosylation s’effectue à
la face luminale du réticulum endoplasmique. La synthèse
TRADUCTION
CADRE OUVERT DE LECTURE
5’NC
NS5B
NS5ANS4BNS3 NS2
C E1 E2
3’NC
NS
4A
P
7
Figure 1. Organisation génomique du VHC. L’ARN génomique
possède un seul cadre ouvert de lecture (en rose) encadré de
deux régions non codantes (en vert) à partir duquel un précur-
seur est synthétisé. Les sites de clivages de la ou des signal
peptidases cellulaires sont représentés par des flèches rouges.
Le site d’action de la signal peptide peptidase est individualisé en
orange (SPP). Les sites de clivages par les protéinases virales
sont représentés par des flèches courbes bleues. L’auto-clivage
entre les protéines NS2/3 est représenté par une courbe en
pointillés. Les protéines structurales sont dessinées en rouge et
les protéines non-structurales en violet.
Asn-X-Ser/Thr-Y C
N
Glucosidase I
Glucosidase II
Figure 2. Noyau commun des N-glycanes. L’oligosaccharide est
ajouté sur le résidu Asn d’une protéine naissante pour former le
noyau commun des N-glycanes. Les résidus glucoses (triangle
rouge) et mannoses (rond rose) terminaux sont clivés par des
enzymes du réticulum endoplasmique (glucosidases et mannosi-
dase) (d’après [40]). Les carrés bleus représentent des résidus
N-acétylglucosamines.
revue générale
Ann Biol Clin, vol. 65, n° 3, mai-juin 2007238
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

des oligosaccharides commence à la face cytosolique du
réticulum endoplasmique. Un transporteur lipidique mem-
branaire, le dolichol, présent à la face cytosolique du réti-
culum endoplasmique porte une chaîne oligosaccharidi-
que constituée de 5 mannoses et 2 N-acétylglucosamines
(Man
5
GlcNac
2
) qui forme le précurseur glycanique. Sous
l’action d’une flipase, le dolichol-Man
5
GlcNac
2
est trans-
loqué vers le côté luminal du réticulum endoplasmique.
Dans le réticulum endoplasmique, le précurseur glycani-
que va subir quelques modifications avant d’être transféré
“ en bloc ” sur une chaîne polypeptidique en cours de
synthèse (figure 3). Le transfert est assuré par une enzyme
cellulaire, l’oligosaccharyltransférase (OST) qui reconnaît
un motif consensus spécifique, le séquon Asn-X-
Ser/Thr-Y, sur la chaîne polypeptidique naissante. L’oli-
gosaccharide est transféré sur le résidu Asn du séquon.
Tous les séquons potentiels ne sont pas glycosylés avec la
même efficacité. En effet, la présence d’un résidu thréo-
nine est un meilleur substrat pour l’OST que les résidus
sérine [3]. Par ailleurs, la nature des acides aminés X et Y
constituant le séquon peut influencer l’efficacité du trans-
fert de l’oligosaccharide. Ainsi, la présence d’un résidu
proline en position X empêche la N-glycosylation. De
même, des résidus tryptophane, leucine, phénylalanine,
glutamine ou asparagine en position X modifient l’effica-
cité de transfert sur le résidu asparagine [4]. Enfin, la
présence d’un résidu proline, tryptophane ou glutamine en
position Y est peu favorable au transfert de l’oligosaccha-
ride (tableau 1) [5]. Le précurseur glycanique transféré
sur la protéine naissante va subir différentes étapes de
maturation qui commencent dans le réticulum endoplas-
mique et se terminent dans l’appareil de Golgi. Au cours
de cette longue maturation, les N-glycosylprotéines
acquièrent une grande diversité glycanique (figure 3). Les
cytosol
cytosol
Golgi
dolichol
flipase OST Ms
M2NAcGlcTf
Transfert du glycane Maturation
Maturation Glycosylation terminale
RE
M1
Figure 3. Biosynthèse des protéines N-glycosylées (d’après [40]). La N-glycosylation démarre à la face cytosolique du réticulum
endoplasmique par l’addition de sucres sur le dolicholphosphate. Quand deux N-acétylglucosamines et cinq mannoses ont été ajoutés,
l’oligosaccharide est transloqué à la face luminale du réticulum endoplasmique par une flipase et sept sucres supplémentaires sont
ajoutés sur le précurseur lipidique. Trois résidus glucose sont ajoutés et l’oligosaccharyltransférase (OST) catalyse le transfert du
noyau oligosaccharidique sur un résidu asparagine de la protéine naissante. Les trois résidus glucose sont alors éliminés par les
glucosidases I et II et les résidus mannoses sont éliminés par une ou plusieurs mannosidases du réticulum endoplasmique (Ms). Une
fois que la protéine est correctement repliée, elle quitte le réticulum endoplasmique (flèche rouge) et elle est transportée dans l’appareil
de Golgi où plusieurs mannoses sont retirés (M1). L’addition d’un résidu N-acétylglucosamine (NAcGlcTf) est suivie par l’élimination de
deux mannoses supplémentaires (M2). Les étapes suivantes ajoutent différents sucres terminaux tels que des résidus galactose,
fucose, N-acétylglucosamine, etc. La protéine mature peut alors gagner son compartiment cellulaire de destination (flèche rouge).
Protéines d’enveloppe du VHC
Ann Biol Clin, vol. 65, n° 3, mai-juin 2007 239
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

N-glycanes jouent un rôle important au cours de la syn-
thèse des protéines virales et dans les interactions entre le
virus et son hôte. Ainsi, les glycanes peuvent être impli-
qués dans la stabilité et le repliement des protéines virales
et dans l’assemblage des particules virales. Ils peuvent
aussi jouer un rôle dans les interactions entre le virus et les
cellules hôtes, dans l’entrée virale ou dans l’immunogéni-
cité des protéines virales.
Mise en conformation
des glycoprotéines
dans le réticulum endoplasmique
Dans le réticulum endoplasmique, parallèlement à la
N-glycosylation, les N-glycosylprotéines acquièrent leur
conformation définitive (conformation secondaire, ter-
tiaire et quaternaire). La mise en conformation des
N-glycosylprotéines est un phénomène dynamique assisté
par des protéines résidentes du réticulum endoplasmique,
des protéines chaperons. L’interaction des protéines
immatures avec les protéines chaperons de mise en
conformation va éviter qu’elles ne s’engagent trop vite
dans une voie de sécrétion, faciliter l’assemblage des pro-
téines oligomériques et éviter leur engagement dans une
voie de dégradation. L’immunoglobulin heavy chain bin-
ding protein (BiP ou grp78) et la peptide disulfure isomé-
rase (PDI) sont des protéines chaperons qui interviennent
essentiellement lors de la mise en conformation des pro-
téines. Elles interagissent transitoirement avec les protéi-
nes naissantes jusqu’à leur mise en conformation correcte
qui favorise alors la dissociation des complexes formés
avec la protéine chaperon [6]. À côté des protéines chape-
rons qui interviennent dans la mise en conformation des
protéines, trois protéines ont été décrites comme étant
spécifiques des N-glycosylprotéines : la calnexine (CNX),
la calréticuline (CRT) et l’ERp57. La CNX est une pro-
téine transmembranaire de type I, résidente du réticulum
endoplasmique qui reconnaît spécifiquement les
N-glycosylprotéines [7]. La CRT est un analogue soluble
de la CNX présente dans la lumière du réticulum endo-
plasmique. La calnexine et la calréticuline interagissent
avec le co-chaperon ERp57. L’ERp57 (ou grp58 ou ER60)
est une protéine soluble résidente du réticulum endoplas-
mique ayant des homologies avec la PDI (revue dans [8]).
Elle est généralement associée à la CNX ou à la CRT.
L’association de la protéine immature avec la CNX ou la
CRT permet sa rétention dans le réticulum endoplasmique
jusqu’à ce qu’elle ait acquis sa conformation définitive et
terminé sa maturation. Une fois qu’elles sont correctement
repliées et maturées, les glycoprotéines se dissocient des
p
rotéines chaperons et quittent le réticulum endoplasmique.
Les glycoprotéines E1 et E2 du VHC
Les glycoprotéines E1 et E2 sont des protéines transmem-
branaires de type I avec un ectodomaine N-terminal
N-glycosylé et un ancrage membranaire hydrophobe
carboxy-terminal. Au cours de leur maturation dans le
réticulum endoplasmique, les protéines E1 et E2 s’assem-
blent pour former des hétérodimères. Deux voies d’assem-
blage permettent la formation des hétérodimères : une
voie dite “ productive ” qui aboutit à la formation des
hétérodimères E1E2 non-covalents et une voie dite “ non
productive ” qui aboutit à la formation d’agrégats hétéro-
gènes liés par des ponts disulfures [2, 9]. Les complexes
non-covalents se replient lentement après leur association
àlaCNX(figure 4) [9, 10]. Cet hétérodimère pourrait être
la forme de pré-bourgeonnement du complexe E1E2 pré-
sent à la surface des particules virales [11]. Le repliement
de E1 est dépendant de la co-expression de E2, alors que
E2 atteint un état conformationnel avancé en l’absence de
E1 [12]. Par ailleurs, l’interaction entre les domaines
transmembranaires de E1 et de E2 est indispensable au
repliement de E1, en même temps que l’expression de E2
[11]. L’interaction des deux domaines transmembranaires
pourrait stabiliser la protéine E1 immature et rapprocher
les ectodomaines de E1 et de E2, favorisant le repliement
de E1. Par ailleurs, la glycoprotéine E1 influence égale-
ment le repliement de E2 [13, 14]. La mise en conforma-
tion de E1 et de E2 est contrôlée par les protéines chape-
rons du RE : la CNX s’associe plutôt aux hétérodimères
non covalents [10], alors que la CRT et la BiP interagis-
sent préférentiellement avec les agrégats liés de façon
covalente [10, 15].
Tableau 1. Nature des acides aminés (AA) influençant l’efficacité
de la N-glycosylation.
Asn-X-Ser/Thr-Y
Contexte favorable
en X [4]
Contexte favorable
en Y [5]
Petit acide aminé Glycine
AA chargés
positivement
Lysine, Arginine,
Histidine
Arginine
AA portant
un résidu hydroxy
Sérine, Thréonine Sérine, Thréonine
Contexte défavorable
en X [4]
Contexte défavorable
en Y [5]
Proline Proline
AA hydrophobes
de grande taille
Leucine, Phénylalanine,
Tryptophane, Tyrosine
Tryptophane
AA chargés
négativement
Acide glutamique, Acide
aspartique
Acide glutamique
La nature des acides aminés qui constituent le séquon peut modifier les
conditions locales et influencer l’activité de l’oligosaccharyltransférase
[4, 5]. En général, la présence d’un résidu sérine en troisième position
rend le séquon plus sensible à la structure des acides aminés en X et en
Y. L’influence d’un résidu cystéine en position X ou Y dépend de son
implication éventuelle dans la formation d’un pont disulfure.
revue générale
Ann Biol Clin, vol. 65, n° 3, mai-juin 2007240
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Variabilité des sites de N-glycosylation
de E1 et E2 en fonction
du génotype viral
Les glycoprotéines E1 et E2 portent de nombreux motifs
de N-glycosylation : 4 ou 5 pour E1 et 10 ou 11 pour E2
en fonction des génotypes viraux. Une analyse portant sur
768 séquences de E1 a identifié jusqu’à 6 sites potentiels
de N-glycosylation [16]. Cinq de ces sites, en positions
196, 209, 234, 305 et 325, apparaissent conservés sur plus
de 96 % des séquences (figure 5). Le site en position 325
présente un résidu tryptophane en position X et un résidu
proline en position Y (Asn-Trp-Ser-Pro). Ces deux résidus
induisent théoriquement un contexte conformationnel qui
rend le séquon inaccessible pour l’OST [5]. Ces données
ont été vérifiées expérimentalement lors d’un travail qui a
montré que ce site n’est pas glycosylé [17]. Un site, en
position 250, est présent uniquement sur les séquences de
E1 de génotypes 1b et 6. L’occupation de ce site a été
confirmée par les données expérimentales [2]. L’analyse
de 388 séquences de E2 a permis d’identifier 11 sites
potentiels de N-glycosylation [16]. Globalement, tous les
sites présents sont conservés sur au moins 99 % des
séquences (figure 5). Certains auteurs ont noté une petite
variabilité locale de certains séquons dont la position du
résidu asparagine peut varier de quelques acides aminés
E1 E1 E1
E2
calnexine
E2E2
321
Figure 4. Repliement de E1 et E2 en présence de la CNX. Les ectodomaines des glycoprotéines E1 et E2 sont orientées dans la
lumière du réticulum endoplasmique (1). Les complexes E1E2 se replient lentement après leur association à la CNX (2). Cet
hétérodimère pourrait être la forme de pré-bourgeonnement des glycoprotéines d’enveloppe (3).
383353
99%
99% 96% 32%
718
417 423 430 448 476 532 540 556 576 623 658
196 209 234 253 305
192
384
99%
746
100% 99% 75% 100% 100%100%99% 89%
Figure 5. Niveaux de conservation des sites potentiels de glycosylation de E1 et de E2. Les sites potentiels de glycosylation de E1 (en
haut) et de E2 (en bas) sont représentés en rouge. Les numéros des sites correspondent aux positions sur la souche H de génotype
1a de référence. Les pourcentages de conservation sont indiqués en dessous de chaque site. Les domaines transmembranaires sont
figurés en jaune pour E1 et en rouge pour E2.
Protéines d’enveloppe du VHC
Ann Biol Clin, vol. 65, n° 3, mai-juin 2007 241
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%