Traitement de la fonction du membre supérieur du patient

Traitement
de
la
fonction
du
membre
supérieur
du
patient
hémiparétique.
Synthèse
de
recommandations
dans
le
cadre
de
l'accident
vasculaire
cérébral
Management
of
upper
extremity
function
in
patients
with
hemiparesis
after
stroke.
Synthesis
of
recommendations
Haute
École
de
Santé
Vaud
(HESAV),
21,
avenue
de
Beaumont,
1011
Lausanne,
Suisse
Reçu
le
19
décembre
2011
;
reçu
sous
la
forme
révisée
le
22
juin
2012
;
accepté
le
2
septembre
2012
Emmanuelle
Opsommer
Sylvie
Ferchichi
Mots
clés
AVC
Membre
supérieur
Recommandations
Réhabilitation
Keywords
Stroke
Upper
limb
Recommendations
Rehabilitation
Auteur
correspondant.
E
Opsommer,
Haute
École
de
Santé
Vaud
(HESAV),
21,
avenue
de
Beaumont,
1011
Lausanne,
Suisse.
Adresse
e-mail
:
emmanuelle.opsommer@
hesav.ch
RÉSUMÉ
Objectif.
–
Présenter
les
recommandations
pour
la
pratique
clinique
(RPC)
de
la
thérapie
par
contrainte,
la
réalité
virtuelle,
la
thérapie
miroir
et
la
pratique
mentale
comme
adjuvant
aux
thérapies
conventionnelles
pour
le
traitement
du
membre
supérieur
parétique
suite
à
un
accident
vasculaire
cérébral
(AVC).
Méthode.
–
Une
revue
de
la
littérature
des
RPC
pour
l'AVC
dans
les
bases
de
données
PEDro,
PubMed,
Cinahl
et
OTSeeker
et
des
revues
systématiques
sur
ces
thérapies
dans
la
base
de
données
Cochrane
Library.
Résultats.
–
Sur
base
des
RPC
obtenues,
ces
quatre
thérapies
présentent
un
intérêt
pour
améliorer
la
fonction
du
membre
supérieur,
avec
différents
niveaux
de
preuve.
Conclusion.
–
Sous
certaines
conditions,
ces
thérapies
peuvent
être
proposées
comme
adju-
vant
aux
thérapies
conventionnelles.
Niveau
de
preuve.
–
Non
adapté.
©
2012
Elsevier
Masson
SAS.
Tous
droits
réservés.
SUMMARY
Objective.
–
To
present
the
clinical
practice
guidelines
on
constraint-induced
movement
therapy,
virtual
reality,
mirror
therapy
and
mental
practice
for
the
treatment
of
the
paretic
upper
limb
poststroke
based
on
a
comprehensive
review.
Method.
–
We
searched
PEDro,
Pubmed,
Cinahl
and
OTseeker
databases
for
guidelines
and
the
Cochrane
Library
for
systematic
reviews
on
these
therapies.
Results.
–
According
to
the
guidelines
found,
these
four
therapies
are
appropriate
to
improve
the
upper
limb
function,
but
with
various
levels
of
evidence.
Conclusion.
–
Under
specified
conditions,
these
therapies
could
be
used
as
adjuvant
to
conven-
tional
therapies.
Level
of
evidence.
–
Not
applicable.
©
2012
Elsevier
Masson
SAS.
All
rights
reserved.
Kinesither
Rev
2013;13(133):25–31 Savoirs
/
Contribution
originale
©
2012
Elsevier
Masson
SAS.
Tous
droits
réservés.
http://dx.doi.org/10.1016/j.kine.2012.09.011
25

INTRODUCTION
Dans
les
pays
industrialisés,
l'accident
vasculaire
cérébral
(AVC)
représente
la
cause
la
plus
fréquente
d'handicap
acquis
à
l'âge
adulte.
C'est
aussi
l'une
des
affections
neurologiques
le
plus
couramment
traitée
par
les
physiothérapeutes
et
les
recommandations
pour
la
pratique
clinique
(RPC)
concernant
l'AVC
soulignent
l'importance
de
leurs
rôles
dans
la
prise
en
charge
du
patient
dans
sa
globalité
[1].
Suite
à
un
AVC,
jusqu'à
85
%
des
patients
présentent
une
hémiparésie,
une
déficience
de
la
perception
sensorielle
et
de
la
fonction
motrice
du
mem-
bre
supérieur
au
stade
aigu.
Six
mois
post-AVC,
seulement
5
%
à
20
%
de
ces
patients
montreront
une
récupération
fonctionnelle
complète
et
pour
30
%
à
60
%,
le
bras
parétique
restera
non
fonctionnel
[2].
Ces
déficiences
limitent
les
acti-
vités
et
restreignent
la
participation
dans
les
situations
de
la
vie
quotidienne.
Le
travail
des
thérapeutes
est
ainsi
amplement
orienté
vers
la
récupération
de
la
fonction
ou
sa
compensation
par
des
thérapies
adaptées
[3].
Selon
la
perspective
du
patient
victime
d'AVC,
une
étude
qualitative
observe
que
le
pro-
gramme
de
physiothérapie
se
concentre
essentiellement
sur
les
exercices
des
membres
inférieurs
et
de
rééducation
à
la
marche
[4].
Toutefois,
certains
patients
souhaitent
donner
une
plus
grande
priorité
à
la
récupération
du
bras
et
de
la
main
[5].
Durant
ces
dernières
années,
de
nombreuses
RPC
sont
appa-
rues
[1,6,7]
et
malgré
une
variabilité
considérable,
leur
qualité
tend
à
s'améliorer
par
l'utilisation
notamment
d'outil
tel
que
la
grille
AGREE
II
lors
de
leur
développement
[8].
Actuellement,
parmi
les
éléments
cruciaux
pour
des
pratiques
optimales,
citons
:
l'initiation
précoce
du
traitement
(en
phase
aiguë)
avec
une
augmentation
progressive
du
niveau
d'activité
;
des
thérapies
actives
et
spécifiques
aux
activités
de
la
vie
quotidienne
avec
une
intensité
élevée
;
un
programme
structuré
proposé
par
une
équipe
interdisci-
plinaire
spécialisée
en
neuroréhabilitation
;
combler
le
besoin
d'informations
du
patient
et
des
aidants
[1].
Lors
d'une
lésion
cérébrale,
on
envisage
de
stimuler,
contrôler
et
orienter
la
plasticité
naturelle
du
cerveau
par
le
biais
d'exer-
cices
thérapeutiques
adaptés
aux
besoins
individuels
du
patient
dans
une
atmosphère
stimulante
d'apprentissage.
Tou-
tefois,
en
ce
qui
concerne
la
rééducation
du
membre
supérieur,
le
manque
de
preuves
d'efficacité
des
interventions
reste
saillant
[1].
Les
auteurs
d'une
revue
systématique
ont
identifié
19
catégories
d'interventions
thérapeutiques
visant
la
récupé-
ration
motrice
post-AVC
[3].
Parmi
elles,
celles
applicables
en
physiothérapie
tant
en
clinique
qu'en
ambulatoire
dont
les
coûts
d'acquisition
restent
à
portée
d'un
indépendant
ou
d'une
petite
structure
ont
été
retenues
ci-après.
Ainsi,
les
quatre
interventions
répondant
à
ces
critères
sont
la
thérapie
par
contrainte,
la
réalité
virtuelle,
la
thérapie
par
miroir
ou
la
pratique
mentale
par
imagerie
motrice.
Elles
ont
aussi
été
choisies
car
elles
ont
le
potentiel
de
per-
mettre
d'appliquer
des
concepts
pertinents
pour
la
neuroréha-
bilitation
dont
la
répétition
de
tâches
significatives
avec
une
intensité
élevée,
la
rétroaction
directe
aux
patients
et
l'aug-
mentation
progressive
de
la
difficulté
de
la
tâche.
Par
ailleurs,
une
réorganisation
au
niveau
cortical
a
également
été
décrite
pour
ces
quatre
thérapies
[1].
Dans
le
courant
actuel
de
pra-
tique
probante,
il
reste
tout
à
fait
indispensable
de
démontrer
l'efficacité
des
interventions
thérapeutiques.
L'objectif
de
cet
article
est
de
présenter
une
revue
compréhensive
des
inter-
ventions
susceptibles
de
contribuer
à
l'amélioration
de
la
fonc-
tion
du
membre
supérieur
chez
des
patients
présentant
une
hémiparésie
post-AVC
comme
adjuvants
aux
thérapies
conventionnelles.
MÉTHODE
Une
revue
systématique
exhaustive
est
au-delà
du
cadre
de
cet
article.
L'intention
était
d'en
utiliser
les
principes
généraux
et
techniques
pour
fournir
une
revue
compréhensive
[9].
D'une
part,
une
recherche
organisée
et
structurée
des
RPC
sur
la
neuroréhabilitation
dans
le
cadre
de
l'AVC
chez
l'adulte
a
été
effectuée
dans
les
bases
de
données
PEDro,
PubMed,
Cinahl
et
OTSeeker
par
une
co-auteure
jusqu'en
décembre
2011,
avec
les
termes
stroke,
cerebrovascular
accident,
guideline,
practice
guideline,
treatment
guideline.
Les
RPC
ont
été
rete-
nues
sur
base
des
critères
suivants
:
des
patients
adultes
(>
18
ans)
post-AVC
;
les
interventions
présentes
dans
la
RPC
;
l'année
de
publication
(2010
ou
2011)
;
accessible
en
texte
intégral.
En
outre,
les
RPC
devaient
être
rédigées
en
français
ou
en
anglais.
Une
recherche
manuelle
sur
des
sites
spécifiques
aux
RPC
a
aussi
été
réalisée
:
National
Guideline
Clearinghouse
(États-Unis),
National
Institute
for
Health
and
Clinical
Excel-
lence
(Royaume-Unis),
Haute-Autorité
de
santé
(France)
et
G-
I-N
International
Guideline
Library.
L'évaluation
de
la
qualité
des
RPC
a
été
réalisée
à
l'aide
de
la
grille
AGREE
II
[8].
La
grille
AGREE
est
un
outil
permettant
d'évaluer
la
qualité
des
RPC
en
estimant
sa
rigueur
méthodologique
et
la
transpa-
rence
du
processus
d'évaluation.
Elle
fournit
de
même
un
cadre
pour
les
groupes
désireux
d'élaborer
des
RPC
en
déter-
minant
quelle
information
intégrer
dans
les
recommandations.
D'autre
part,
la
base
de
données
The
Cochrane
Library
a
été
consultée
depuis
les
premières
publications
jusqu'en
décem-
bre
2011
avec
les
termes
stroke
et
ensuite
avec
des
termes
spécifiques
aux
quatre
interventions
dans
les
titres
des
revues
systématiques.
Une
seconde
consultation
de
cette
base
de
données
a
été
réalisée
en
juin
2012.
RÉSULTATS
Parmi
les
511
articles
retrouvés
sur
la
période
considérée,
une
sélection
sur
les
titres
puis
les
textes
intégraux
a
permis
d'identifier
quatre
RPC
répondant
aux
critères
posés.
Il
s'agit
des
recommandations
du
Scottish
Intercollegiate
Guidelines
Network
[1],
du
National
Stroke
Foundation
[10],
des
New
Zealand
clinical
guidelines
[11]
et
de
l'American
Stroke
Asso-
ciation
[12].
Les
bases
de
données
ont
été
consultées
dans
ces
RPC
jusqu'en
2009
[1],
août
2009
[10,11]
et
mars
2009
[12].
Pour
chacune
de
ces
RPC,
les
cadres
de
référence
y
sont
précisément
décrits
;
à
savoir
les
cadres
du
processus
de
développement,
d'évaluation
de
la
qualité
des
études
et
de
formulation
des
recommandations.
Toutefois,
le
grade
des
recommandations
diffère.
Une
évaluation
de
la
qualité
de
ces
RPC
a
été
réalisée
avec
la
grille
AGREE
II
par
le
ASHA's
E.
Opsommer,
S.
Ferchichi
Savoirs
/
Contribution
originale
26

National
Center
for
Evidence-Based
Practice.
Les
RPC
[1,10–
12]
sont
considérées
respectivement
comme
hautement
recommandées
et/ou
recommandées
avec
réserve
[13].
En
effet,
cette
dernière
RPC
ne
permet
pas
d'identifier
sur
quelles
études
reposent
les
recommandations
formulées
[12].
Le
Tableau
I
propose
les
recommandations
formulées
dans
ces
quatre
RPC
à
l'égard
des
interventions
retenues
et
le
type
de
preuve
sur
lequel
elles
reposent.
Par
ailleurs,
la
recherche
de
revues
systématiques
avec
le
terme
stroke
dans
la
base
de
données
The
Cochrane
Library
a
produit
298
résultats.
Parmi
ceux-ci,
52
revues
ou
protocoles
de
revues
étaient
en
lien
avec
les
interventions
thérapeutiques
du
champ
de
la
physiothérapie
ou
de
l'ergothérapie.
La
lecture
des
titres
a
permis
d'en
sélectionner
quatre
concernant
les
interventions
retenues
[14–17].
La
seconde
consultation
de
cette
base
de
données
a
produit
un
résultat
supplémentaire
:
la
revue
systématique
de
Thieme
et
al.,
2012
[18]
finalisée
sur
base
du
protocole
[16]
;
elle
porte
sur
la
thérapie
par
le
miroir.
Ces
revues
systématiques
incluent
des
RCT
ou
quasi-RCT.
Les
bases
de
données
ont
été
consultées
dans
ces
revues
systématiques
Cochrane
jusqu'en
juin
2008
pour
la
CIMT
[14],
mars
2010
pour
la
réalité
virtuelle
[15],
novembre
2009
pour
la
pratique
mentale
[17]
et
juin
2011
pour
la
thérapie
par
miroir
[18].
En
cela,
elles
offrent
des
résultats
d'études
plus
récents
que
les
RPC
à
l'exception
des
recommandations
pour
la
CIMT
incluant
la
revue
Cochrane
de
2009
[14].
Sur
base
de
ces
documents,
chaque
intervention
est
à
présent
définie
et
leur
efficacité
présentée
ci-dessous
(Tableau
II).
La
thérapie
par
contrainte
ou
par
contrainte
induite
(CIMT)
Cette
thérapie
se
définit
par
l'utilisation
forcée
du
bras
paré-
tique
durant
les
activités
de
la
vie
quotidienne
et
des
sessions
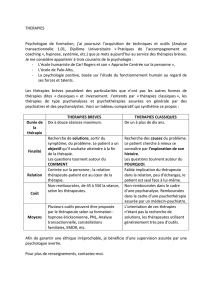
Tableau
I.
Les
recommandations
et
grades
de
recommandations
(entre
crochets)
issus
de
recommandations
pour
la
pratique
clinique
(RPC)
concernant
la
thérapie
par
contrainte,
la
réalité
virtuelle,
la
thérapie
par
miroir
et
la
pratique
mentale
par
imagerie
motrice
pour
le
traitement
de
la
fonction
du
membre
supérieur
parétique
après
un
accident
vasculaire
cérébral
(AVC).
Thérapie
RPC
SIGN
2010
Écosse
NSF
2010
Australie
Andrews
et
al.
(2010)
Nouvelle-Zélande
Bates
et
al.
(2010)
États-Unis
d'Amérique
Thérapie
par
contrainte «
Peut
être
envisagée
pour
les
personnes
sélectionnées
avec
soin
ayant
au
moins
10
degrés
d'extension
des
doigts
;
l'équilibre
et
la
cognition
intacts
»
[B]
«
Permet
d'augmenter
la
quantité
de
pratique
»
«
Pourrait
être
commencée
dans
la
première
semaine
pour
des
patients
sélectionnés
avec
soin,
cependant,
au
début
une
intensité
élevée
peut
être
nocive
»
[C]
«
Recommandée
pour
les
personnes
ayant
au
moins
10
degrés
d'extension
de
deux
doigts,
du
pouce
et
du
poignet
»
[A]
Réalité
virtuelle
Preuve
insuffisante
«
D'autres
développements
sont
nécessaires
(essais
plus
grands
et
solides
sont
nécessaires)
»
«
D'autres
études
sont
nécessaires
»
«
Considérer
la
réalité
virtuelle
comme
un
contexte
de
pratique
»
[C]
Thérapie
par
miroir
Non
mentionnée
«
À
utiliser
en
complément
d'autres
approches
»
[C]
«
Peut
être
utilisée
en
complément
d'autres
interventions
»
[C]
Preuve
insuffisante
[I]
Pratique
mentale
«
Peut
être
considérée
comme
un
complément
à
la
pratique
normale
pour
améliorer
la
fonction
du
membre
supérieur
après
un
AVC
»
[D]
«
À
utiliser
en
complément
d'autres
approches
»
[B]
«
Peut
être
utilisée
en
complément
d'autres
interventions
»
[B]
«
Considérer
la
pratique
mentale
avec
des
tâches
fonctionnelles
répétées
et
intenses
»
[B]
Grades
des
recommandations
pour
Scottish
Intercollegiate
Guidelines
Network
(SIGN).
A.
Repose
sur
un
ensemble
de
preuves
comprenant
principalement
des
méta-
analyses,
revues
systématiques
de
la
littérature
et
essais
contrôlés
randomisés
avec
un
faible
risque
de
biais.
B.
Repose
sur
un
ensemble
de
preuves
(revues
systématiques
de
qualité
élevée,
études
de
cas
ou
de
cohorte)
directement
applicables
à
la
population
cible.
C.
Repose
sur
un
ensemble
de
preuves
(études
de
cas
ou
de
cohorte
bien
menées
avec
un
faible
risque
de
biais
et
une
probabilité
modérée
de
relation
causale)
directement
applicables
à
la
population.
D.
Repose
sur
des
rapports
de
cas,
des
séries
de
cas,
des
avis
d'experts.
GPP.
Repose
sur
l'expérience
clinique
des
membres
du
groupe
de
développement
des
recommandations.
Grades
des
recommandations
pour
National
Stroke
Foundation
(NSF)
et
Andrews
et
al.
(2010).
A.
Ensemble
de
preuves
auquel
on
peut
faire
confiance
pour
guider
la
pratique.
B.
Ensemble
de
preuves
auquel
on
peut
faire
confiance
pour
guider
la
pratique
dans
la
plupart
des
situations.
C.
Ensemble
de
preuves
fournissant
un
certain
soutien
pour
la
recommandation
mais
des
précautions
doivent
être
prises
pour
son
application.
D.
Ensemble
de
preuves
faible
et
la
recommandation
doit
être
appliquée
avec
prudence.
V
ou
GPP.
Recommandation
basée
sur
l'expertise
clinique
ou
l'avis
d'experts.
Grades
des
recommandations
de
Bates
et
al.
(2010).
A.
Forte
recommandation
aux
cliniciens
de
proposer
l'intervention
aux
patients
admissibles.
B.
Recommandation
aux
cliniciens
de
proposer
l'intervention
aux
patients
admissibles.
C.
Aucune
recommandation
pour
ou
contre
la
prescription
systématique
de
l'intervention
n'est
faite.
D.
Recommandation
de
ne
pas
prescrire
l'intervention
pour
les
patients
asymptomatiques.
I.
La
conclusion
est
que
les
preuves
sont
insuffisantes
pour
recommander
ou
ne
pas
prescrire
l'intervention.
Kinesither
Rev
2013;13(133):25–31 Savoirs
/
Contribution
originale
27

d'exercices
spécialement
conçues
tout
en
contraignant
celle
du
bras
plus
fort
par
une
écharpe
ou
une
mitaine
(contrainte
jusqu'à
90
%
du
temps
de
veille).
Ces
thérapies
par
usage
forcé
reposent
sur
un
entraînement
intensif
:
plusieurs
heures
par
jour
(jusqu'à
7
h/jour)
;
sept
jours
par
semaine
pendant
deux
semaines.
Des
versions
modifiées
avec
moins
de
temps
de
contrainte
et
d'exercices
par
jour
mais
durant
une
plus
longue
période
sont
également
proposées
[14].
Durant
les
sessions
d'exercices,
l'apprentissage
de
gestes
et
de
mouve-
ments
du
membre
supérieur
parétique
viserait
à
vaincre
la
non-utilisation
acquise
(learned
non-use)
en
obligeant
la
per-
sonne
à
utiliser
son
membre
parétique
[14].
Cet
apprentissage
se
base
sur
un
conditionnement
opérant
avec
renforcement
positif
verbal
(félicitations)
et
shaping
ou
façonnement.
Ainsi
pour
l'apprentissage
d'un
comportement
(ici
un
mouvement),
le
façonnement
consiste
à
renforcer
les
approximations
suc-
cessives
du
comportement
à
acquérir
et
à
offrir
de
fréquentes
rétroactions
(feedback)
au
patient.
À
ce
jour,
des
tâches
fonc-
tionnelles
ou
des
activités
de
la
vie
quotidienne
de
complexité
croissante
sont
utilisées
dans
la
majorité
des
études
et
l'acqui-
sition
d'une
tâche
se
fait
par
petites
étapes
progressives.
La
revue
Cochrane
de
Sirtori
et
al.
[14]
incluant
619
patients
engagés
dans
19
essais
contrôlés
randomisés
(RCT)
souligne
l'impact
modéré
et
statistiquement
significatif
de
la
CIMTsur
le
handicap
(mesure
de
l'indépendance
fonctionnelle
ou
indice
de
Barthel)
et
la
fonction
motrice
du
bras.
Toutefois,
la
per-
sistance
de
l'effet
à
trois
et
six
mois
après
le
traitement
n'est
pas
encore
établie
[14].
Ces
résultats
se
rapportent
essentiel-
lement
à
des
personnes
adultes
atteintes
d'un
AVC,
ayant
la
capacité
d'étendre
activement
les
articulations
métacarpopha-
langiennes
et
interphalangiennes
d'au
moins
108,
et
le
poignet
d'au
moins
208,
sans
problème
d'équilibre
(incluant
la
marche),
ni
troubles
cognitifs
majeurs
ni
douleur
excessive
au
niveau
du
bras
(score
<
4
sur
une
échelle
visuelle
analogique)
et
sans
spasticité
excessive
(score
<
2
sur
l'échelle
d'Ashworth
ou
Ashworth
modifiée).
Une
généralisation
à
toute
la
population
de
patients
atteints
d'AVC
demeure
ainsi
limitée.
Par
consé-
quent,
avant
d'entreprendre
cette
thérapie
tout
en
respectant
les
préférences
du
patient,
plusieurs
éléments
seraient
alors
à
considérer
tels
que
les
modalités
pratiques
de
l'intervention
incluant
la
spécification
de
la
région
anatomique
placée
sous
contrainte,
la
durée
de
la
pose
de
la
contrainte
et
la
durée
quotidienne
de
pratique
des
tâches
[14].
Ainsi,
une
contrainte
de
la
main
a
donné
des
résultats
significatifs
alors
qu'avec
une
Tableau
II.
Synthèse
des
aspects
cliniques
d'interventions
thérapeutiques
pour
le
membre
supérieur
parétique
post-
AVC.
Interventions
Population
concernée
Ressources
en
matériel
Intérêt
pour
améliorer
Thérapie
par
contrainte
[14]
Capacité
à
effectuer
activement
au
moins
108
d'extension
dans
articulations
MP
et
IP,
208
d'extension
du
poignet
;
absence
de
problèmes
d'équilibre
;
absence
de
troubles
cognitifs
majeurs
;
absence
de
douleur
excessive
du
MS
(<
4
sur
EVA)
;
absence
de
spasticité
excessive
(<
2
sur
Ashworth).
Stades
subaigu
et
chronique
S'assurer
au
préalable
de
l'adhérence
du
patient
à
l'intensité
de
traitement
et
à
la
durée
journalière
de
la
contrainte
Écharpe/mitaine
Formation
préalable
à
la
CIMT
Autonomie
dans
AVQ
Fonction
motrice
du
MS
Réalité
virtuelle
[15]
Membre
légèrement
à
modérément
parétique.
À
éviter
chez
des
patients
épileptiques
À
évaluer
chez
des
patients
aphasiques,
apraxiques,
avec
déficits
visuels,
chez
les
personnes
phobiques
à
l'informatique
Stades
subaigu
et
chronique
Préférer
les
systèmes
avec
immersion
partielle
pour
limiter
l'apparition
d'effets
secondaires
(nausées,
maux
de
tête)
Matériel
informatique,
écran,
logiciel,
plateforme,
manette.
.
.
(système
commercial
aussi
efficace
que
système
spécialisé)
Autonomie
dans
AVQ
Fonction
motrice
du
MS
Thérapie
par
miroir
[18]
Patiente
avec
parésie
sévère
et
modérée
À
éviter
chez
des
patients
avec
troubles
cognitifs,
notamment
déficits
d'attention
et
de
traitement
de
l'information,
aphasie,
démence
Stades
subaigu
et
chronique
Miroir
Autonomie
dans
AVQ
Fonction
motrice
du
MS
Pratique
mentale
[17]
Capacité
à
effectuer
une
imagerie
motrice
qui
peut
être
évaluée
par
chronométrie
mentale,
rotation
d'images
ou
questionnaires
A
éviter
chez
des
patients
avec
lésion
pariétale
gauche
Possible
au
stade
subaigu,
mais
plus
souvent
étudié
au
stade
chronique
Pas
indispensable
(si
besoin,
cartes,
support
audio/vidéo)
Fonction
motrice
du
MS
MP
:
métacarpophalangienne
;
IP
:
interphalangienne
;
MS
:
membre
supérieur
;
EVA
:
échelle
visuelle
analogique
;
CIMT
:
constraint-induced
movement
therapy
;
AVQ
:
activité
de
la
vie
quotidienne.
E.
Opsommer,
S.
Ferchichi
Savoirs
/
Contribution
originale
28

contrainte
conjointe
du
bras
et
de
la
main
l'amélioration
de
la
fonction
du
membre
supérieur
par
rapport
au
groupe
témoin
est
non
significative
[14].
Sur
base
des
études
incluses
dans
cette
revue,
la
durée
de
pratique
des
tâches
(
30
h)
amélio-
rant
la
fonction
motrice
du
bras
dans
le
groupe
CIMT
par
rapport
au
groupe
témoin
est
répartie
selon
une
pratique
hebdomadaire
d'1
h
30
à
deux
heures
par
jour,
cinq
jours
par
semaine
durant
trois
semaines
[14].
Enfin,
l'efficience
de
la
CIMT
reste
à
évaluer.
En
effet,
les
coûts
associés
à
la
CIMT
pourraient
être
très
élevés
étant
donné
l'intensité
et
le
temps
engagé
par
les
thérapeutes
[1].
La
réalité
virtuelle
(RV)
La
RV
est
l'utilisation
de
matériel
informatique
et
de
logiciels
permettant
de
simuler
un
environnement,
appelé
virtuel,
sem-
blable
au
monde
réel.
Cette
approche
relativement
récente
en
neuroréhabilitation
permet
à
l'utilisateur
d'interagir
avec
des
objets
dans
diverses
situations
(sport
en
extérieur,
déplace-
ment
dans
une
salle
de
bain,
marche
dans
la
rue.
.
.).
Diverses
applications
de
la
RV
en
autorisent
actuellement
l'usage
comme
outil
de
traitement
notamment
pour
la
récupération
fonctionnelle
du
membre
supérieur
post-AVC
[15].
À
cette
fin,
divers
systèmes
de
RV
sont
spécifiquement
conçus
mais
l'usage
détourné
de
consoles
de
jeux
vidéo
interactives,
une
alternative
moins
onéreuse,
a
également
été
adopté
par
les
milieux
cliniques.
Le
sentiment
pour
l'utilisateur
d'être
présent
dans
cet
environnement
simulé,
appelé
présence,
peut
être
influencé
par
plusieurs
facteurs.
Parmi
ceux-ci,
cer-
tains
sont
liés
aux
caractéristiques
du
système
(par
exemple
la
façon
dont
est
représenté
l'utilisateur
dans
l'environnement
virtuel),
de
l'utilisateur
(par
exemple
son
âge,
ses
expériences
précédentes
avec
la
RV,
son
handicap.
.
.)
et
d'autres
enfin
à
celles
de
l'environnement
virtuel
et
de
la
tâche
qui
y
sera
effectuée
(par
exemple
la
signification
de
la
tâche).
Quant
au
degré
d'immersion,
second
concept
clé
de
la
RV,
il
repose
sur
la
qualité
des
technologies
utilisées
et
réfère
à
la
mesure
dans
laquelle
l'utilisateur
se
perçoit
dans
un
environnement
virtuel
plutôt
que
dans
le
monde
réel
[15].
En
fonction
du
degré
d'immersion
et
des
caractéristiques
de
l'utilisateur,
certains
participants
peuvent
présenter
des
effets
secondaires
tels
que
des
nausées,
des
perturbations
oculaires,
une
instabilité
posturale,
des
maux
de
tête
et
de
la
somnolence
[15].
C'est
une
raison
pour
laquelle
le
type
de
système
préférentiellement
utilisé
en
neuroréhabilitation
est
plutôt
un
système
avec
immersion
partielle
pour
lequel
la
prévalence
des
effets
secon-
daires
est
considérée
comme
minimale
[15].
Le
transfert
d'informations
du
système
de
RV
à
l'utilisateur
(output)
peut
s'effectuer
selon
diverses
modalités
:
le
plus
souvent
visuelles
et
auditives
et
accessoirement
tactiles
et
vestibulaires.
Les
images
virtuelles
peuvent
ainsi
être
présentées
via
un
dispo-
sitif
posé
sur
la
tête
de
l'utilisateur
ou
plus
fréquemment
via
un
système
de
projection,
un
écran
plat
ou
un
simple
moniteur
d'ordinateur
placé
en
face
de
l'utilisateur.
La
présence
d'autres
feedbacks
auditifs
ou
tactiles
renforcent
encore
le
degré
d'immersion
et
offrent
à
l'utilisateur
des
expériences
plus
pro-
ches
de
celles
du
monde
réel.
Recevant
ainsi
des
informations
sur
l'environnement
simulé
par
le
système
de
RV,
l'utilisateur
doit
encore
avoir
la
possibilité
d'interagir
avec
les
objets
pré-
sentés
dans
cet
environnement
virtuel.
Ainsi,
le
transfert
d'informations
de
l'utilisateur
vers
le
système
(input)
prend
diverses
formes
:
l'utilisateur
se
comporte
de
manière
naturelle
et
c'est
le
système
qui
via
des
capteurs
spéciaux
(par
caméras)
suit
les
actions
de
l'utilisateur
et
y
répond
en
conséquence
;
l'utilisateur
interagit
avec
le
monde
virtuel
par
des
moyens
indirects
comme
les
touches
d'un
clavier
d'ordinateur,
la
souris
ou
une
manette
de
jeu
[15].
La
récente
revue
systématique
Cochrane
relève
à
ce
sujet
un
effet
modéré
de
l'utilisation
de
la
RV
sur
la
fonction
du
bras
et
les
activités
de
la
vie
quotidienne
par
rapport
à
la
même
dose
d'un
traitement
conventionnel
[15].
Dans
cette
revue,
huit
études
concernant
l'entraînement
du
membre
supérieur
pour
un
total
de
225
patients
post-AVC
ont
été
incluses,
dont
cinq
ciblaient
des
patients
au
stade
chronique
et
deux
des
patients
au
stade
subaigu
concluant
pour
ces
deux
stades
à
un
effet
significatif
[15].
La
RV
permettrait
d'obtenir
une
plus
grande
amélioration
de
la
fonction
du
membre
supérieur
que
les
interventions
thérapeutiques
conventionnelles
;
l'ampleur
de
l'effet
restant
toutefois
modéré
[15].
En
revanche,
l'éventuel
bénéfice
pour
la
force
de
préhension
n'a
pas
été
démontré.
Il
en
va
de
même
pour
la
fixation
de
la
dose
de
RV
la
plus
efficace
et
le
type
de
programme
de
RV
à
proposer
aux
patients
[15].
Enfin,
selon
une
étude
incluse
dans
la
revue
Cochrane,
les
personnes
du
groupe
RV
présentaient
à
six
mois
des
performances
au
niveau
de
la
fonction
du
membre
supérieur
significativement
plus
élevées
que
le
groupe
témoin
[15].
La
thérapie
par
miroir
La
thérapie
par
miroir
consiste
à
placer
un
miroir
dans
le
plan
sagittal
entre
les
membres
supérieurs
du
patient
de
manière
à
bloquer
la
vision
du
membre
atteint
et
à
utiliser
l'image
réfléchie
du
membre
non
atteint
afin
de
lui
donner
l'impression
de
bouger
normalement
le
bras
atteint.
Elle
a
été
initialement
exploitée
avec
des
patients
souffrant
de
douleur
du
membre
fantôme.
Elle
permet
de
résoudre
le
conflit
entre
l'intention
motrice
du
patient
et
le
feedback
sensoriel,
de
moduler
la
douleur
du
membre
fantôme,
d'améliorer
la
fonction
et
d'aug-
menter
la
discrimination
tactile
chez
des
patients
souffrant
du
syndrome
douloureux
régional
complexe
[16].
Les
feedbacks
sensoriels,
tout
d'abord
visuels
et
également
proprioceptifs
sont
cruciaux
pour
les
habiletés
motrices,
cela
remodelant
l'intégration
sensorimotrice.
Dans
la
thérapie
par
miroir,
les
illusions
visuelles
de
mouvements
du
membre
supérieur
paré-
tique
compenseraient
les
afférences
proprioceptives
réduites
voire
absentes
après
un
AVC
et
permettraient
de
rétablir
une
certaine
congruence
entre
la
perception
sensorielle
et
la
fonc-
tion
motrice.
La
thérapie
par
miroir
incorpore
ainsi
des
compo-
santes
visuelles,
somesthésiques
et
motrices.
Enfin,
une
hypothèse
explicative
de
la
thérapie
par
le
miroir
reposerait
sur
l'activation
de
neurones
«
miroir
»
corticaux.
Il
n'y
a
tou-
tefois
pas
de
preuves
directes
(enregistrements
cellulaires)
de
l'existence
de
ces
neurones
chez
l'être
humain
mais
des
données
d'imagerie
cérébrale
en
suggèrent
l'existence
[16].
Selon
une
revue
Cochrane
de
2012
incluant
13
études
pour
un
total
de
506
patients,
la
thérapie
par
miroir
a
un
effet
significatif
sur
la
fonction
motrice
du
membre
supérieur
post-AVC
et
les
activités
de
la
vie
quotidienne
à
la
fin
de
la
phase
d'intervention
par
rapport
aux
autres
interventions
[18].
En
outre,
cette
thérapie
aurait
aussi
un
effet
significatif
à
long
terme
sur
la
fonction
du
membre
supérieur,
observé
dans
les
études
avec
un
suivi
à
six
mois
[18].
Kinesither
Rev
2013;13(133):25–31 Savoirs
/
Contribution
originale
29
 6
6
 7
7
1
/
7
100%