laboratoire genhotel

Les variations de nombre de
copies
Les variations de nombre de copies (CNV)
se définissent comme étant des séquences
supérieures à 1 kb et qui sont présentes en
plusieurs copies dans le génome d’une
population donnée. Pour que ces CNV
soient considérés comme des
polymorphismes, il faut que leur
fréquence soit supérieure à 1%.
Notre étude porte sur des CNVs d’un gène
candidat fonctionnel dans la PR
appartenant à la famille des Glutathions
S-Transfèrases (GST): le gène GSTM1. Ce
dernier est connu pour avoir un rôle dans
la protection contre les métabolites
toxiques émis par le tabac ainsi que dans
la survie des lymphocytes et la protection
de la moelle osseuse. Le gène GSTM1 est
caractérisé par l’apparition d’une délétion
complète du gène avec un fréquence de
50% dans la population Caucasienne. Ce
phénomène est le résultat d’un mécanisme
appelé Recombinaison Homologue Non-
Allélique (NAHR) et qui induit
simultanément la complète délétion du
gène sur un brin et une duplication sur
l’autre brin (Figure 2).
Les variants de Nombre de copies (CNVs) des gènes de la famille des Glutathion S-Transférase
dans la Polyarthrite Rhumatoïde:
MS Ben Kilani (1), L Michou (2), T Bardin (3) & F Cornélis (1;3), E Petit-Teixeira (1)
(1) Laboratoire Genhotel-EA3886, Université Evry-Val d'Essonne, Evry, France (2) Service de Rhumatologie, CHU Laval,
Québec, Canada(3) Fédération de Rhumatologie, CHU Lariboisière, AP-HP, Paris, France
Introduction
La polyarthrite rhumatoïde (PR) est une maladie auto-immune systémique caractérisée par une arthrite chronique, destructive et invalidante. C’est le plus fréquent
des rhumatismes inflammatoires chroniques avec une prévalence de 1% au sein de la population adulte.
Cette maladie est caractérisée par la présence d’auto-anticorps dirigés soit contre des IgG (Facteur Rhumatoïde) soit contre des peptides modifiés par citrullination
(ACPA).
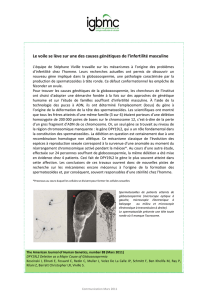
La PR est une maladie multifactorielle, avec un facteur environnemental confirmé, l’exposition au tabac. Le gène HLA-DRB1, et plus précisément les allèles qui
codent l’épitope partagé « SE », est le facteur génétique majeur associé à un risque élevé dans la PR. D’autres facteurs génétiques de faible contribution ont été
identifiés, l’ensemble n’expliquant que partiellement la composante génétique de cette maladie. Il est donc important d’étudier d’autres variations du génome dans
la PR (Figure 1).
Figure 1: Les différents facteurs
impliqués dans le phénotype
d’une maladie complexe. D’après
Beckmann JS et al., 2007.
GenHotel-EA3886
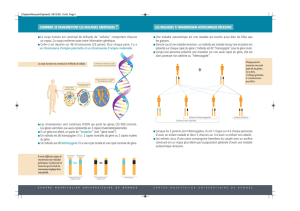
Figure 2:Mécanisme de la recombinaison homologue dans la
région de GSTM1. D’après McLellan RA et al., 1997.
Objectifs
Notre but est de déterminer les variants de nombre de copies
(CNV) du gène GSTM1 en relation avec l’exposition au tabac
et le gène HLA-DRB1 dans la PR. La transmission des CNVs
est étudié au sein des familles trios constituées chacune d’un
patient et ses deux parents sains.
Résultats
La délétion du gène GSTM1 dans l’échantillon testé a
une fréquence de 52%, ce qui concorde avec la
fréquence décrite dans la littérature. De façon
intéressante, nous avons trouvé une fréquence élevée de
génotypes avec 2 copies (36%) situées sur le même brin
(Figure 2). Ce résultat est validé par une amplification
spécifique de la jonction de la région délétée.
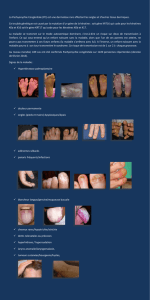
Par ailleurs, un nombre de copies égale à 5 a été observé
chez des patients (Figure 3), ce qui a été confirmé par
l’analyse de transmission familiale.
Figure 3: Distribution des CNVs chez 240 patients PR
Patients
Contrôles
Au moins une délétion
GSTM1
186
176
GSTM1 +/+
5
15
OR= 3,17 (1,13 – 8,9)
Tableau 1: Distribution des génotypes de
GSTM1
entre les patients et les
contrôles
Patients & Méthodes
240 patients atteints de PR, dont la consommation de tabac est connue, font
partie de cette étude. La présence/absence du gène GSTM1
(GSTM1+/GSTM1-) est révélée par une PCR qui amplifie la jonction de la
région délétée. Cette amplification permet la distinction entre GSTM1+/- et
GSTM1+/+. Ensuite, l’analyse CNV est complétée pour les patients GSTM1+
par quantification en utilisant une sonde spécifique fluorescente Taqman®
(Applied Biosystems). Les résultats sont analysés en fonction de la
consommation ou non de tabac (TE+/TE-) et du génotypage HLA-DRB1 par
Odds Ratio (OR) et intervalle de confiance à 95% (IC 95%).
Enfin, les deux parents sains de 191 patients de familles trios ont été
génotypés et une analyse familiale a été réalisée avec le Test de Déséquilibre
de Transmission (TDT) et l’évaluation du Risque Relatif des Génotypes
(GRR, les contrôles étant constitués à partir des allèles parentaux non
transmis aux patients)
L’investigation de la relation entre les CNVs du gène GSTM1 et l’exposition au tabac ne montre pas
de relation significative.
Nous avons ensuite stratifié les patients selon l’exposition au tabac et analysé la relation entre la
présence/absence du gène GSTM1 et les allèles « SE » du gène HLA-DRB1, associés à la PR. Cette
stratification n’as pas permis de mettre en évidence une interaction entre ces deux gènes.
Le calcul du Risque Relatif aux Génotypes (GRR) révèle un risque élevé associé à la PR lorsqu’il y a
au moins une délétion du gène GSTM1 (Tableau 1).
Conclusion
Notre étude est la première qui a entrepris l’analyse des CNVs du gène GSTM1 au sein de familles
trios ce qui nous a permis de mettre en évidence un risque significatif associé à la PR lorsque le
génotype comporte au moins une délétion du gène GSTM1.
Aucune relation n’a été observée entre la délétion de GSTM1, le facteur génétique majeur de la
PR, HLA-DRB1, et le facteur environnemental, exposition au tabac, au sein des patients.
Une étude préliminaire faite sur le gène GSTT1, un autre membre de la famille GST, au sein des
patients PR révèle, comme pour GSTM1, que le gène peut être présent avec un nombre de copies
supérieur à deux.
La caractérisation des CNVs est une étape indispensable dans la découverte de nouveaux facteurs
génomiques de maladies complexes tel que la Polyarthrite Rhumatoïde.
1
/
1
100%