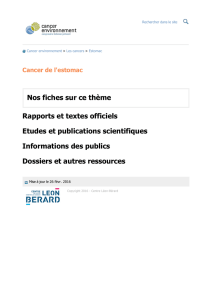
Les cancers superficiels de l`estomac

130 Cancérodig. Vol. 3N°2-2011 -130-135
DOI 10.4267/2042/41562
©aln.editions
DOSSIER THÉMATIQUE :LECANCER DE L’ESTOMAC
Les cancers superficiels de l’estomac
Superficial cancer of the stomach
Romain Coriat1,2,Ariane Chryssostalis1,Stanislas Chaussade1,2
1. Service de Gastroentérologie, Hôpital Cochin, GHU Ouest
2. Université Paris Descartes
AP-HP,27, rue du Faubourg Saint-Jacques, F-75014 Paris
❚Résumé
Le cancer superficiel de l’estomac est un cancer limité àla
muqueuse ou àlasous-muqueuse (T1). L’ absence d’invasion de
la musculairemuqueuse diminue le risque d’envahissement
ganglionnaireetpermetd’envisageruntraitement endoscopique.
Le risque de métastases ganglionnaires est corrélé àlataille de la
tumeur,àl’envahissement en profondeur de la lésion et àl’aspect
endoscopique de la lésion.
Le traitement endoscopique consiste àréaliser,après repérage
de la lésion, une dissection sous-muqueuse de celle-ci, et cela
afin de permettreune résection en monobloc. Cette technique,
limitée àcertains centres, permet d’envisager un traitement curatif
endoscopique de ces tumeurs et doit êtresuivie d’une surveillance
rapprochée endoscopique.
Mots-clés
Cancers superficiels de l’estomac, ESD, Dissection, Endoscopie
❚Abstract
Early gastric cancer corresponds to amucosa or submucosa carci-
noma (T1). The absence of invasion of muscularis mucosa reduces
the risk of lymph node and thereforeendoscopic treatment could
be considered. The risk of lymph node metastases is correlated
with tumor size, invasion depth of the lesion and the endoscopic
appearance of the lesion. Endoscopic treatment is performed after
locating the lesion. Endoscopic submucosal dissection allows en
bloc resection. This technique is limited to some centers and could
be considered as acurative endoscopic treatment. This therapy
has to be followed by aclose surveillance endoscopy.
Keywords
Early gastric cancer,ESD, Dissection, Endoscopy
❚Introduction
Le cancer superficiel de l’estomac est un cancer défini par son
atteinte limitée àlamuqueuse ou àlasous-muqueuse, quel que soit
son statut ganglionnaire(cancer classé T1). Dans les cancers super-
ficiels de l’estomac, le risque de métastase ganglionnaireest de
l’ordrede15à20 %etles paramètres associés àcette atteinte
ganglionnairedoivent êtrebien connus pour permettreuntraitement
endoscopique. Seul 1%des cancers superficiels de l’estomac
bénéficie d’un traitement endoscopique en France. Leur pronostic
est excellent après traitement chirurgical et le développement des
techniques d’endoscopie pourrait permettred’éviter des chirurgies.
Les indications du traitement endoscopique sont bien codifiées et
doivent êtrediscutées en réunion de concertation pluridisciplinaire.

Cancérodig. Vol. 3N°2-2011 131
japonais. Cette classification permet de faireladistinction entre
les lésions polypoïdes (type I), les lésions planes (type II) et les
lésions ulcérées (type III) (Fig. 1). Parmi les lésions planes, on
distingue les lésions planes légèrement surélevées (type IIa), les
lésions complètement planes (type IIb) et les lésions planes
légèrement déprimées (type IIc). La répartition de ces lésions
parmi les cancers superficiels de l’estomac est fournie par les
séries japonaises (Tableau 1). On peut ainsi voir que les lésions IIc
représentent près de 78 %des cancers superficiels et que les
lésions IIa représentent environ 17 %des cancers superficiels,
soulignant l’importance de l’examen soigneux de la paroi
gastrique au cours de l’endoscopie pour détecter ces anomalies
de relief et de couleur de la muqueuse.
Le diagnostic repose sur la pratique de biopsies qui ne néces-
sitent pas d’êtretrès nombreuses. Il aeneffet été démontré que
la performance diagnostique de 2biopsies et de 4biopsies sont
respectivement de 90 %etde95%.
❚Bilan d’extension
Le bilan d’extension comporte un examen complet de l’ensemble
de la muqueuse gastrique en utilisant des techniques de
chromoendoscopie virtuelle (NBI, FICE) ou des colorants tels que
l’indigo carmin associé ou non àdel’acide acétique. Ces
techniques permettent de retrouver des lésions synchrones dans
15 %des cas et de déterminer la lésion avec plus de précision
que l’endoscopie de routine [5,6].
Le bilan d’extension comporte une échoendoscopie qui permet,
avec précision, de différencier les lésions T1 des lésions T2.
L’échoendoscopie peut êtrenormale au cours des cancers
superficiels de l’estomac, et l’utilisation de mini-sondes
de 20 ou 30 MHz apu, dans des mains entraînées, distinguer
les lésions atteignant la muqueuse de la sous-muqueuse.
Néanmoins, cette technique est peu diffusée, en France, et
expose àdes risques de sur-oudesous-évaluation de l’exten-
sion en profondeur des cancers superficiels. L’échoendoscopie
❚Épidémiologie des cancers
superficiels de l’estomac
Les cancers superficiels de l’estomac sont rares en France [1]. Ils
représentent environ 5à10 %del’ensemble des cancers de
l’estomac mais l’incidence de ces cancers diagnostiqués àun
stade précoce n’augmente pas, la majorité des cancers de
l’estomac étant diagnostiqués àunstade avancé [2] et cela
malgré les progrès de l’endoscopie et la description des aspects
endoscopiques du cancer superficiel de l’estomac par les auteurs
japonais.
Les cancers superficiels de l’estomac voient leur incidence
augmentée avec l’âge et sont plus fréquents chez l’homme que
chez la femme. Ces chiffres d’incidence contrastent avec ceux
rapportés dans les études japonaises ou coréennes où la
fréquence des cancers superficiels aprogressivement augmenté
pour atteindre40% des cancers réséqués vers 1985.
Actuellement, en Asie, l’incidence des cancers superficiels de
l’estomac dépasse celle des cancers gastriques invasifs dans
certains centres de dépistage. Ces chiffres ne sont pas unique-
ment dus àune politique de dépistage de ce cancer qui est
beaucoup plus fréquent dans ces pays mais ils sont surtout la
conséquence de la reconnaissance, par les endoscopistes
japonais ou coréens, de ces cancers (description du Pit Pattern,
apport de la chromoendoscopie). Les formes dépistées en
France [2] sont le plus souvent ulcérées, ce qui explique la part
tout àfait anecdotique du traitement endoscopique des cancers
superficiels de l’estomac en France.
❚Diagnostic
Il n’existe pas de signe clinique particulier du cancer superficiel
de l’estomac et celui-ci doit êtrerecherché au cours de toute
endoscopie digestive haute. Au Japon, seuls 20 %des cancers
superficiels de l’estomac sont retrouvés au cours d’un examen de
dépistage.
Certaines situations pathologiques identifiées exposent àun
risque plus élevé de cancer de l’estomac et constituent des
populations àrisque. Ainsi, le risque de cancer de l’estomac est
plus élevé au cours de la polypose adénomateuse familiale, après
gastrectomie partielle, au cours de la maladie de Biermer mais
surtout au cours de la gastrite chronique. Ainsi,une étude
hollandaise récente amis en évidence qu’après une première
endoscopie digestive haute, le risque cumulé de cancer de
l’estomac, à10ans, était inférieur à1%encas de gastrite
atrophique ;de1,5 %encas de métaplasie intestinale ;de4%en
cas de dysplasie de bas grade ;etde31%encas de dysplasie
de haut grade [3].
Les aspects endoscopiques du cancer superficiel de l’estomac
doivent êtrebien connus. Toute anomalie du relief ou toute modi-
fication localisée de la muqueuse gastrique doit êtreanalysée et
doit êtrebiopsiée. Les anomalies du relief sont àlabase de la
classification de Paris [4] qui s’est fortement inspirée des travaux
Figure 1
Aspect endoscopique :laclassification japonaise
Hauteur >2.5 mm
Profondeur <1.2mm
Lambert Retal. Superficial Neoplastic Lesions in the Digestive Tract –Endoscopy 2005: 37: 570-578

132 Cancérodig. Vol. 3N°2-2011
spécifique de 99 %pour les cancers superficiels intramuqueux
et 95 %pour les cancers T1 atteignant la sous-muqueuse [7].
Sous l’influence des endoscopistes japonais, il aété suggéré que
le traitement local par endoscopie pouvait suffiredans certains
cas. Ce traitement endoscopique intéresse environ 50 %des
cancerssuperficiels de l’estomac au Japon. Deux techniques
sont, àl’heure actuelle, utilisées:lamucosectomie endosco-
pique (EMR) et la dissection endoscopique (ou ESD). Ces traite-
ments locaux font l’impasse sur le curage ganglionnaire, ce qui a
conduit les endoscopistes japonais àidentifier les facteurs de
risque de métastases ganglionnaires.
Facteurs prédictifs du risque ganglionnaire
dans les cancers superficiels de l’estomac
Dans les cancers superficiels de l’estomac, l’atteinte ganglion-
naireest, dans 70 %des cas, proximale. Dans les cancers
intramuqueux, le risque ganglionnaireest considéré comme très
faible, de l’ordrede1à3%.Dans les cancers superficiels
Lésion IIa +IIc
Lésion IIc (78 %des cas)
Tableau 1. Aspects endoscopiques des cancers superficiels de l’estomac
Cancers superficiels de l’estomac
Sous-type (n =2098)
0–I 3%
0–IIa 17 %
0–IIb <1%
0–IIc 78 %
0–III <1%
est plus précise dans le staging ganglionnaireque le TDM abdo-
minal et doit êtreréalisée dans tous les cas de cancers superfi-
ciels.
❚Traitement
Initialement, le traitement de référence était la chirurgie qui donne
des taux de survie de plus de 95 %à10ans avec une survie

Cancérodig. Vol. 3N°2-2011 133
–
aux cancers superficiels bien différenciés intramuqueux de plus
de 2cm;
–aux cancers intramuqueux présentant une érosion ou une
ulcération de moins de 3cm;
–aux cancers intramuqueux peu différenciés ou présentant des
cellules indépendantes de moins de 3cm;
–àcertains cancers superficiels de l’estomac envahissant la
partie superficielle de la sous-muqueuse (sm1 ou envahis-
sement de moins de 500 µm) sous réserve qu’il s’agisse d’une
tumeur bien différenciée de petite taille (< 3cm) et en l’absence
d’emboles vasculaires et/ou lymphatiques. Ces conditions et la
rareté de ces lésions en France font qu’il est absolument
indispensable que ces patients soient pris en charge dans des
centres spécialisés et qu’une collaboration étroite existe entre
l’endoscopiste et l’anatomopathologiste.
❙Le traitement chirurgical
Il s’agit du traitement de référence et il n’est pas différent des
cancers invasifs de l’estomac. Il comporte une gastrectomie
totale ou des 4/5 et un curage ganglionnaireD1,5. Le curage
ganglionnaireest identique àcelui des cancers invasifs. Les résul-
tats sont excellents avec unemortalité postopératoiredemoins
de 5%etune survie sans récidive de plus de 90 %àdeux ans.
Ce traitement peut êtreeffectué par voie laparoscopique lorsque
cette technique est maîtrisée. Les résultats sont excellents avec
des taux de survie sans récidive de plus de 95 %.
❙Le traitement endoscopique
La 1re étape est d’identifier les marges latérales du cancer.Cette
1re étape est parfois difficile et l’aide de la chromoendoscopie
électronique (NBI et FICE) [11,12] est démontrée pour permettre
une exérèse R0. Un marquage avec le plasma ARGON ou un
bistouri est indispensable. D’autres colorations par l’indigo
carmin, le cristal violet ou un mélange d’acide acétique et d’indigo
carmin ont été aussi proposées [13].
atteignant la sous-muqueuse, An et al.[8] ont montré, dans une
série de 1043 patients opérés entre2002 et 2005 que le risque
de métastases ganglionnaires était de 20 %etque les facteurs de
risque de métastases ganglionnaires étaient la taille de la tumeur,
la profondeur de l’invasion dans la sous-muqueuse, la différen-
ciation de la tumeur,l’existence d’une infiltration lymphatique ou
l’existence d’une infiltration périnerveuse. Toutes ces données
peuvent êtreobtenues par l’endoscopie et l’examen anatomo-
pathologique d’une pièce de résection endoscopique. En analyse
multivariée, 2facteurs indépendants sont apparus, àsavoir la
taille de la tumeur et l’existence d’une invasion lymphatique
(Tableau 2). Lorsqu’il existait un envahissement lymphatique ou
périnerveux, le risque de métastases ganglionnaires était de plus
de 40 %. L’existence de cellules indépendantes n’apparaissait
pas comme un facteur indépendant de métastases ganglion-
naires même si ce critèreaété retrouvé dans d’autres séries de la
littérature. Ces études soulignent l’importance d’avoir un examen
histologique soigneux de la pièce de résection endoscopique.
Dans le tableau n° 2, on peut voir que lorsque la taille du cancer
superficiel est <1cmetqu’il n’existe pas d’infiltration lympha-
tique, le risque de métastase ganglionnaireest nul ;que lorsque
la taille de la tumeur est <2cmetqu’il n’existe pas d’invasion
lymphatique, le risque de métastase ganglionnaireest
de 1,3 %. Entre2cmet3cmetlorsque l’invasion lymphatique
est absente, le risque de métastase ganglionnaireest de l’ordre
de 3à7%enfonction de l’infiltration dans la sous-muqueuse.
Dès qu’il existe une invasion lymphatique, et même si les
tumeurs sont de petite taille, le risque de métastase ganglion-
naireest important. Dans le travail d’An et coll. [8], 88 %des
patients ayant des métastases ganglionnaires étaient N1,
8%étaient N2 mais 4%étaient N3. Tous les cancers superfi-
ciels N3 avaient une invasion lymphatique sur la pièce de
gastrectomie. Ces résultats plaident pour les auteurs japonais
sur la réalisation d’un curage D2 dans les cancers superficiels
de l’estomac. Ces constatations, issues de travaux sur des
pièces de résection chirurgicales, nécessitent une coopération
étroite avec l’anatomopathologiste et sont àlabase des
recommandations japonaises sur le traitement endoscopique
des cancers superficiels de l’estomac.
Les recommandations actuelles rapportées par Gotoda et coll. [9]
distinguent les indications validées du traitement endoscopique à
savoir :
–des cancers limités àlamuqueuse ;
–des cancers bien différenciés ;
–des cancers dont la taille est de moins de 2cmpour des
lésions IIa ou de moins de 1cmpour des lésions IIc ;
–l’absence d’érosions ou d’ulcérations ;
–l’absence d’emboles veineux ou lymphatiques àl’examen de
la piècederésection endoscopique ;
–letraitement endoscopique était contre-indiqué si la tumeur
était peu différenciée ou comportait des cellules indépendantes.
Ces critères ont été étendus récemment àlasuite des travaux de
Gotoda et coll. [10] :
Tableau 2. Incidence de l’envahissement ganglionnaire métastatique en
fonction de la présence d’embole lymphatique, de la taille tumorale et de
l’invasion de la sous-muqueuse
Aspect endoscopique
de la lésion Sm1 Sm2 Sm3
Absence d’embole lymphatique (n =706)
Taille
(cm)
<1 0% 10 %0%
1à<2 1,7 %11,1 %11,1 %
2à<4 3,6 %4,1 %7,3 %
≥49%15,9 %11,6 %
Présence d’emboles lymphatiques (n =337)
Taille
(cm)
<1 0% 50 %0%
1à<2 22,2 %33,3 %33,3 %
2à<4 50 %28,3 %40,7 %
≥484,6 %42,4 %57,7 %

134 Cancérodig. Vol. 3N°2-2011
On peut signaler que dans cette série, les cancers superficiels
étaient le plus souvent de type muqueux, leur diamètre<15mm
et le plussouvent de type différencié. Néanmoins,comptetenu
de l’existenced’une métaplasie intestinale associée, il est forte-
ment recommandé de rechercher et d’éradiquer l’
Helicobacter
pylori
après une mucosectomie endoscopique ou une dissection
endoscopique d’un cancer superficiel de l’estomac.
Au total, le cancer superficiel de l’estomac est une entité peu
fréquente dans notrepays, du fait d’une reconnaissance insuffi-
sante des aspects endoscopiques par les gastroentérologues. Un
traitement endoscopique est possible, dans certains cas, dans
des centres spécialisés après discussion au cours de la réunion
de concertation pluridisciplinaireetaprès analyse soigneuse de la
pièce de résection. La dissection endoscopique est la technique
de choix d’exérèse des cancers superficiels de l’estomac. Dans
les autres cas, la chirurgie donne d’excellents résultats.
❚Références
1. Benhamiche AM, FaivreJ,Tazi MA, Darsouni R, Villing AL,
Couillault C. Superficial cancer of the stomach: evolution of their
characteristics over a20year period in one population.
Gastroenterol Clin Biol 1998;22:13-8.
2. Arsene D, Chomontowski J, Pottier D, Rougereau A, Launoy G,
Gignoux M. Epidemiology and prognosis of gastric carcinomas at
the province of Calvados. A10-year study.Gastroenterol Clin Biol
1995;19:797-803.
3. de Vries AC, van Grieken NC, Looman CW,Casparie MK, de
Vries E, Meijer GA, et al. Gastric cancer risk in patients with
premalignant gastric lesions: anationwide cohort study in the
Netherlands. Gastroenterology 2008;134:945-52.
4. Update on the Paris classification of superficial neoplastic lesions
in the digestive tract. Endoscopy 2005;37:570-8.
5. Kadowaki S, Ta naka K, To yoda H, Kosaka R, Imoto I, Hamada Y,
et al. Ease of early gastric cancer demarcation recognition: a
comparison of four magnifying endoscopy methods. JGastro-
enterol Hepatol 2009;24:1625-30.
6. Mouri R, Yoshida S, Tanaka S, Oka S, Yoshihara M, Chayama K.
Evaluation and validation of computed virtual chromoendoscopy in
early gastric cancer.Gastrointest Endosc 2009;69:1052-8.
7. Gotoda T. Endoscopic resection for premalignant and malignant
lesions of the gastrointestinal tract from the esophagus to the
colon. Gastrointest Endosc Clin NAm2008;18:435-50, viii.
8. An JY,Baik YH, Choi MG, Noh JH, Sohn TS, Kim S. Predictive
factors for lymph node metastasis in early gastric cancer with
submucosal invasion: analysis of asingle institutional experience.
Ann Surg 2007;246:749-53.
9. Soetikno R, Kaltenbach T, YehR,Gotoda T. Endoscopic mucosal
resection for early cancers of the upper gastrointestinal tract. JClin
Oncol 2005;23:4490-8.
10. Gotoda T, Iwasaki M, Kusano C, Seewald S, Oda I. Endoscopic
resection of early gastric cancer treated by guideline and expanded
National Cancer Centrecriteria. Br JSurg 2010;97:868-71.
11. Okada K, Fujisaki J, Kasuga A, Omae M, Hirasawa T, Ishiyama A,
et al. Diagnosis of undifferentiated type early gastric cancers by
magnification endoscopy with narrow-band imaging. JGastro-
enterol Hepatol 2011. [Epub ahead of print].
La 2eétape est de déterminer la taille de la tumeur (< 1cm
ou >2cmou3cm) et son aspect endoscopique en se servant
de la classificationdeParis. La techniqued’exérèseendosco-
pique va certes dépendredel’expérience de l’opérateurmais il
est fortement recommandé, au-delà de 2cmvoirede1cmpour
les endoscopistes japonais, de privilégier la dissection endosco-
pique. De même, lorsqu’il existe une érosion ou une ulcération et
quel que soit le diamètredelalésion (> 1cm), il est recommandé
d’utiliser l’ESD qui permet de réaliser une résection en bloc de la
lésion dans un pourcentage de cas plus important et qui permet
de mieux détecter un envahissement vasculaireoulympha-
tique [14]. Au-delà de 2cm, il est bien démontré que la dissection
endoscopique permet d’obtenir plus d’exérèse R0 et en seul
fragment, gage d’un examen anatomopathologique de qualité.
Dans les tumeurs de plus de 2cm, le taux de récidive de la muco-
sectomie endoscopique varie de 5à25%surtout si les marges
de résections sont atteintes ou si la mucosectomie est effectuée
en plusieurs fragments [14].
Dans les séries japonaises et coréennes, les résultats sont très
concordants. Le taux de résection mono bloc de la dissection
et le taux de résection R0 sont proches de 95 %[15,16]. Dans
une série de 1000 patients ayant bénéficié d’une dissection
endoscopique, le taux d’hémorragie digestive retardée, d’hémor-
ragie retardée abondante, de perforation et de chirurgie après
dissection sont de respectivement 15,6 %;0,6 %;1,2 %et
0,2 %. Le taux de résection complète est lié àlataille de la lésion,
sa localisation (taux de résection moins important pour les lésions
de l’estomacproximal), l’existence d’une cicatrice et l’existence
d’un cancer peu différencié. Les taux de survies à5ans, bruts
sans récidive et spécifiques, étaient de 97,1 %et100 %, témoi-
gnant de l’efficacité de la dissection endoscopique [16] dans
cette série qui comportait aussi des patients avec les critères
élargis d’indications de la dissection endoscopique proposés par
Gotoda. Dans l’étude d’Isomoto, la mortalité était nulle et le taux
de perforations de 4,5 %. Ces perforations étaient plus impor-
tantes dans le groupe appartenant aux critères élargis et toutes
ces perforations étaient traitées de façon conservatrice avec
fermeturepar des clips. Après dissection endoscopique, le
facteur de risque local le plus souvent retrouvé est celui d’une
exérèse incomplète. L’exérèse incomplète est, elle-même, asso-
ciée àune localisation de la partie haute de l’estomac pour une
taille >3cm[17].
❙Suivi après résection endoscopique
d’un cancer superficiel de l’estomac
Après une résection endoscopique, une surveillance endosco-
pique régulièreest indispensable. Les recommandations
japonaises préconisent une endoscopie de surveillance
à6,12, 24 et 36 mois après le traitement endoscopique ;l’éradi-
cation d’
Helicobacter pylori
,lorsqu’il est retrouvé, est indispen-
sable. Lors d’études récentes, il aété démontré que l’éradication
d’
Helicobacter
permettait de diminuer de plus de 2/3 les risques
de cancers métachrones [18]. Le risque de cancer métachrone
était, à3ans, de 9,6 %etde3,6 %dans le groupe éradication.
 6
6
1
/
6
100%